Oszillierende Reaktionen der Ascorbinsäure
Experimente:
Versuch: Die oszillierende Reaktion des Ascorbinsäure/Cer/Bromat-Systems
Versuch: Oszillierende Reaktion des Oxalsäure/Cer/Bromat-Systems
Die Erscheinung der Periodizität ist für biologische Systeme eine lange bekannte
und bereits vielfach untersuchte Eigenschaft. Grundlage rhythmischer biologischer
Prozesse sind letztlich oszillierende chemische Reaktionen, so dass dieses Gebiet
gleichermaßen für den Chemie- wie für den Biologieunterricht relevant ist.
Die am besten untersuchte chemische Oszillation ist die Belousov-Zhabotinskii-Reaktion: Hierbei wird Citronensäure mit Kaliumbromat in schwefelsaurer Lösung in Gegenwart von Cer(IV)-sulfat als Katalysator oxidiert bzw. bromiert. Die Reaktion zeigt einen rhythmischen Farbwechsel zwischen Gelb (Ce4+ sowie Br2) und Farblos (Ce3+). Die Reaktionsteilnehmer lassen sich durch eine Reihe anderer Stoffe ersetzen. Statt Citronensäure eignet sich Malonsäure und (last but not least) auch die Ascorbinsäure [24] (-> Versuch).
Im Gegensatz zu den anderen, oben angesprochenen oszillierenden Reaktionen kann die Reaktion mit der Ascorbinsäure nicht visuell verfolgt werden, da die Lösung aufgrund starker Bromentwicklung konstant braun gefärbt bleibt. Aus diesem Grunde wird eine Redoxmessung mit den üblichen Redoxelektroden (Pt-Blech gegen Hg / HgS04) vorgenommen; an das Spannungsmessgerät sollte ein Schreiber angeschlossen werden.
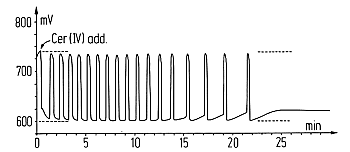
Das folgende Bild zeigt das Ergebnis einer solchen Messung. Die Gesamtdauer der Oszillation beträgt nur 25-30 Minuten, die maximale Schwingungszahl ist 25-28. Die Amplitude beträgt etwa 150 mV.

Oszillation des Ascorbinsäure-Cer-Bromat-Systems.
Elektroden: Platin gegen Quecksilber(II)-sulfat [24]
Über den Mechanismus des Ascorbinsäure/Bromat/Cer-Systems ist wenig bekannt.
Offenbar wird Ascorbinsäure langsam abgebaut zum Beispiel durch Abspaltung von
Oxalsäure. Diese kann selbst als Substrat bzw. Reduktionsmittel in der
Belousov-Zhabotinskii-Reaktion dienen. Dies zeigt sich daran, dass während der Oszillation in
großen Mengen Kohlenstoffdioxid gebildet wird. Der geschwindigkeitsbestimmende
Abbau macht sich auch in einem bemerkenswert konstanten Redoxpotential
während der Oszillation bemerkbar.
Weitere Texte zum Thema „Ascorbinsäure“