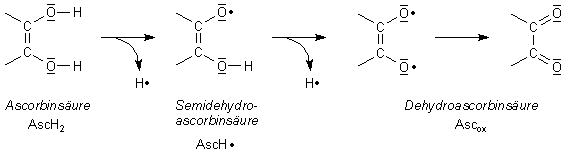
Ascorbinsäure bildet Radikale und ist das Antiklopfmittel der Zelle
Die genaue Untersuchung des Reaktionsmechanismus bei der Ascorbinsäureoxidation ergab Hinweise darauf, dass die Wasserstoffatome der Endiolgruppe einzeln abgespalten werden. Deshalb bilden sich intermediär Radikale. Das sind Atome oder Verbindungen mit freien, ungepaarten Elektronen. So entsteht aus der Ascorbinsäure AscH2 die radikalische Semidehydroascorbinsäure AscH·. Bei der Abspaltung des zweiten H-Atoms entsteht ein Biradikal, das sich elektronisch zur Dehydroascorbinsäure Ascox umlagert.

Es sei daran erinnert, dass auch der Sauerstoff ein (allerdings stabiles) Biradikal ist!
Vitamin C als Radikalfänger
In der Möglichkeit zur Radikalbildung ist auch der Wirkungsbereich für Vitamin C als
Radikalfänger im Organismus zu erkennen. Radikale eliminierende Stoffe nennen
wir Scavenger (engl. Straßenkehrer).
(Wir kennen diese Scavenger auch als Antiklopfmittel in
der Treibstofftechnologie.)
Hier sind die Hintergründe: Durch den Stoffwechsel einer aeroben Zelle kommt es zur Bildung des Superoxid-Ions O2¯, das zugleich ein Radikal ist, das Superoxidradikal. Deshalb schreibt man es genau: O2·¯. Dieses stammt aus molekularem Sauerstoff, der bei der Endreaktion der Atmungskette statt vier nur ein Elektron erhalten hat. Das so gebildete, sehr toxische Radikal reagiert mit der Ascorbinsäure unter Bildung von Wasserstoffperoxid.
O2·¯ + H+ + AscH2 ———> H2O2 + AscH·
Bei den Reaktionen kann zusätzlich das Hydroxyl-Radikal HO· entstehen. Es bildet sich ebenfalls bei Einwirkung von harten Strahlungen, wie sie beim radioaktiven Zerfall auftreten. Auch dieses Radikal wird durch Ascorbinsäure unschädlich gemacht.
HO· + AscH2 ———> H2O + AscH·
Was passiert mit den so gebildeten Ascorbylradikalen? Sie reagieren miteinander zu Ascorbinsäure und Dehydroascorbinsäure. (Dies ist eine Diproportionierungsreaktion.)
2 AscH· ———> AscH2 + Ascox
Durch diese Reaktionen wird verhindert, dass die Sauerstoff-Radikale wichtige Moleküle wie zum Beispiel die DNA oder Proteine sowie empfindliche Moleküle in den Biomembranen angreifen können. Ascorbinsäure spielt also in den Zellen die gleiche Rolle, die die Antiklopfmittel in den Motoren spielen.
Das ebenfalls giftige Wasserstoffperoxid wird durch das sehr effektive Enzym Katalase abgebaut.
Das Superoxidradikal O2·¯ wird übrigens auch durch das Enzym Superoxid-Dismutase umgesetzt.
2 O2·¯ + 2 H+ ———> H2O2 + O2
Ascorbinsäure kann ihre Sauerstoff zehrende Tätigkeit auch in lipophilem Gewebe ausspielen. Grund ist, dass ihr Radikalmechanismus am besten in unpolarem Milieu abläuft. Das macht man sich auch bei der Konservierung fetter Nahrungsmittel wie Wurst zunutze.
Weitere Texte zum Thema „Ascorbinsäure“