
DŁnnschichtchromatographie (DC)
Experimente
Versuch: Herstellung einer DŁnnschichtchromatographie-Platte
Versuch: DŁnnschichtchromatographie von Inhaltsstoffen in GewŁrzen
Versuch: DŁnnschichtchromatographie von Aminosšuren
Die DŁnnschichtchromatographie (abgekŁrzt DC) ist eine Verteilungschromatographie. Als stationšre
Phase dient feinkŲrniges Kieselgel oder Aluminiumoxid. Diese Masse strich man ursprŁnglich auf groŖen Glasplatten
aus (-> Versuch). Das war ein Alltagsgeschšft fŁr Chemiker. Heute nutzt man
kšufliche Platten mit Plastik oder Aluminium als Tršgermaterial fŁr die stationšre Phase.
Die DC funktioniert im Prinzip wie die Papierchromatographie, trennt aber schšrfer. Die stationšre Phase ist resistenter gegen bestimmte LŲsemittelgemische sowie gegen spezielle Nachweisreagenzien.

Bild 1: Das Bild zeigt das Chromatogramm der Farbstoffmischung eines braunen Filzstiftes auf einer selbst
hergestellten DC-Platte
(Foto: Steffi)
Die DC ist eine wichtige Analysen-Methode. Mit ihr ist es mŲglich, eine sehr geringe Menge eines
Gemischs sehr genau und schnell zu analysieren. So nutzen Lebensmittelchemiker diese Methode, um z. B.
ein GewŁrz-Gemisch genauer zu untersuchen (-> Versuch).
An der Auftrennung eines Aminosšuregemischs kann man das Prinzip der Trennung mit Hilfe der DC
besonders gut erlšutern (-> Versuch).
Die Polaritšten der verschiedenen Aminosšuren sind je nach Beschaffenheit ihres Rests verschieden. Hier sind
drei Beispiele:
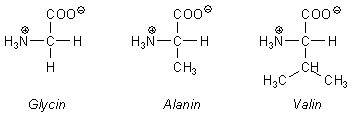
Wir nehmen an, dass (wie im Versuch) die hier verwendete Kieselgel-Folie polar ist, das Laufmittel unpolar. Wir erhalten folgendes Chromatogramm:

Bild 2: Chromatogramm eines Aminosšuregemischs sowie von Vergleichssubstanzen:
V (Valin), A (Alanin) und G (Glycin).
Die Anfšrbung erfolgte mit Ninhydrin
(Foto: Steffi)
Weniger polare Aminosšuren (wie z. B. Valin) werden kaum an der polaren stationšren Phase fixiert, sondern
bleiben eher im Laufmittel gelŲst und werden deshalb mit dem Laufmittelstrom weiter transportiert, wšhrend die
polareren Aminosšuren (z. B. Glycin, Alanin) durch Wechselwirkung mit dem polaren Kieselgel festgehalten werden.
Man erkennt am Chromatogramm: Glycin ist deutlich polarer als das Alanin und wandert deshalb nur ganz wenig.
Dem Bild entnimmt man weiter, dass die Analyse-Mischung die Aminosšuren Valin und Glycin enthielt.
Weitere Texte zum Thema ĄChromatographieď