Wie man in der Chemie elektrische Leitfähigkeiten misst
Experimente:
Versuch 1a: Leitfähigkeitstitrationen mit einfachem Messgerät
Leitfähigkeiten misst man, indem man durch das zu untersuchende System einen
definierten elektrischen Strom fließen lässt und den Widerstand ermittelt. Das
Verfahren heißt "Konduktometrie", das Gerät "Konduktometer" (lat. ducere, leiten).
Eine Leitfähigkeitsmesszelle für Elektrolytlösungen oder -schmelzen besteht im Wesentlichen aus zwei platinierten Platinelektroden mit definierter Größe und konstantem Abstand. Denn die Leitfähigkeit ist von der Länge und dem Querschnitt des Leiters (hier des Elektrolyten) abhängig. Die Geometrie einer Zelle beschreibt die Zellkonstante.
cz = Länge/Querschnitt (1/cm)
Diesen Wert ermittelt man (wenn überhaupt nötig) anhand von KCl-Eichlösungen bekannter Leitfähigkeit experimentell. Meistens misst man nur die Veränderungen der Leitfähigkeit. Das ist zum Beispiel bei Leitfähigkeitstitrationen (-> Versuch) oder bei der Verfolgung der Güte von Ionenaustauscherwasser der Fall.
Ein gutes Leitfähigkeits-Messgerät arbeitet mit Wechselstrom bis zu 5000 Hz. Wechselstrom ist notwendig, damit es während der Messung nicht zu einer Elektrolyse kommt.
Der Kehrwert des Widerstands ist der Leitwert (Siemens, veraltet auch mho oder Reziproke ohm), aus dem die Leitfähigkeit berechnet werden kann. Letzteres ist nur dann notwendig, wenn man an Absolutwerten interessiert ist. Die berechnete Größe ist die molare Leitfähigkeit. Darunter versteht man die Leitfähigkeit, die ein Elektrolyt mit Konzentration 1 mol/l zwischen zwei Elektroden ausreichender Größe mit 1 cm Abstand hat.
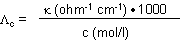
k ist die spezifische Leitfähigkeit.
Weitere Texte zum Thema „Elektrochemie“