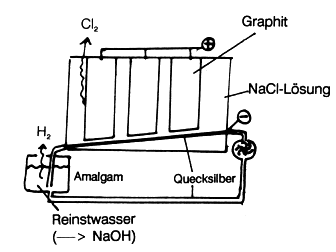
Elektrolyse von wässriger Natriumchloridlösung (Amalgamverfahren)
Mit dem Amalgamverfahren stellt man durch Elektrolyse von gesättigter Natriumchloridlösung Natronlauge, Wasserstoff und Chlor her. Man verwendet eine Quecksilberkathode und eine Anode aus Graphit.

An der Anode läuft folgende Reaktion ab:
2 Cl- à Cl2 + 2 e-
An der Kathode läuft wegen der sehr großen Überspannung von Wasserstoff an Quecksilberelektroden folgende Reaktion ab:
2 Na+ + 2 e- à 2 Na
Das Natrium bildet mit dem Quecksilber Natriumamalgam und ist so vor der Oxidation durch das
im Elektrolyten enthaltene Wasser geschützt.
In einem anderen Reaktionsraum wird das Natriumamalgam mit Wasser versetzt und verrührt.
Dadurch reagiert das Natrium mit dem Wasser, und es entstehen Natronlauge und Wasserstoff:
2 Na + 2 H2O à 2 NaOH + H2
Weitere Texte zum Thema „Elektrochemie“