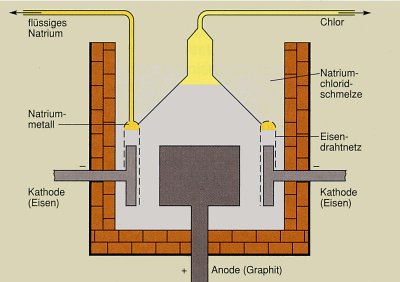
Natrium- und Chlorgewinnung durch Schmelzflusselektrolyse
Experimente:
Versuch: Schmelzflusselektrolyse von Lithiumchlorid
Natrium und Chlor werden durch Schmelzflusselektrolyse von Natriumchlorid (Kochsalz) gewonnen.
Als Anode verwendet man eine Kohleelektrode und als Kathode eine Eisenelektrode.

Die Elektrodenvorgänge sind:
Reduktion: 2 Na+ + 2 e- à 2 Na
Oxidation: 2 Cl- à Cl2 + 2 e-
Redoxreaktion: 2 Na + 2 Cl- à 2 Na + Cl2
Wegen des hohen Schmelzpunktes von Natriumchlorid (801 °C), der im technischen Verfahren allerdings durch Zugabe von Calciumchlorid deutlich gesenkt wird, verwenden wir im Modellversuch Lithiumchlorid (Schmelzpunkt 610 °C) (-> Versuch). Wir könnten natürlich auch Bleichlorid nehmen - aber das wegen seiner Giftigkeit in den Schulen nicht mehr gern gesehen. Lithiumchlorid hat den Vorteil, dass (inklusive der Produkte) alles ähnlich aussieht wie beim Natriumchlorid.
Weitere Texte zum Thema „Elektrochemie“