 |
 |
 |
 |
| Kurze Fragen - Kurze Antworten
Aus dem E-Mail-Korb von Professor Blume |
1701
F: Ich habe meinen Opalring auf unserem Kaminofen liegen gelassen. Man Mann
hat den Ofen angeheizt. Heute Morgen habe ich festgestellt, dass er (der Opal) kaum noch leuchtet. Was kann ich tun?
A: Sie können versuchen, den Stein durch Einlegen in destilliertes Wasser (oder
zusatzfreies Bügelwasser, auf keinen Fall Leitungswasser verwenden!) zu regenerieren. Dazu müssen Sie aber viel Geduld aufbringen,
denn das kann einige Tage dauern.
Der Grund für diese Maßnahme: Opal ist chemisch betrachtet ein wasserhaltiges Siliciumdioxid. Er ist aus Mikrokristallen aufgebaut,
zwischen denen sich Porenwasser befindet. Strahlt man Licht ein, so resultieren Beugung und farbgebende Interferenzen, wie sie für
dünne Schichten (wie z. B. auch für alte Museumsgläser aus der Römerzeit oder für Ölfilme
an der Tankstelle) typisch ist.
Der Wassergehalt von Opalen liegt bei 2-9 Masse%. Wenn das Wasser herausgekocht wird, ist es mit der Farbigkeit vorbei. Die Schadwirkung setzt so richtig bei Temperaturen über 70 °C. Aber zum Ausdunsten des Porenwassers bedarf es keines Ofens - es reicht schon warme Sonnenstrahlung oder das Bestrahlen mit einer Spotlampe aus. Deshalb altern alle Opale deutlich. Kenner gönnen ihnen deshalb des Öfteren ein erfrischendes Wasserbad, damit sich sein Wasserhaushalt wieder ins Gleichgewicht bringt und die Farbigkeit erhalten bleibt.
Ob Sie Erfolg haben, hängt letztlich aber von derjenigen Temperatur ab, der der Stein ausgesetzt war. Wenn erst einmal die Mikro-Struktur zerstört ist, wird wohl nichts mehr gehen.
1702
F: Warum ist Absinth so schädlich?
A: Absinth ist ein vor allem in südlichen Ländern geschätzter Weinbrand.
Man erkennt ihn daran, dass er sich beim Verdünnen milchig weiß trübt. Das war früher die Droge der Künstler. In Frankreich trinkt
man ihn z. B. als grünen Pernod®.
Absinth wird durch Brennen aus Wermutwein hergestellt. Dies ist ein gewürzter normaler Wein, dem bei der Gärung Wermut-Pflanzen (Artemisia absynthium) zugefügt werden.
Nun muss man wissen, dass Wermut eine Pflanze ist, die größere Mengen an giftigen Inhaltsstoffen aus der Reihe der Terpene enthält. Die These, diese wirkten in großer Konzentration als Nervengifte, ist umstritten, für mich aber denkbar: Denn Terpene sind ja letztlich Lösemittel, die die Markscheiden der Nervenzellen angreifen. Bei Missbrauch kommen neben der Demenz noch Leberschäden hinzu. Aber das kann auch alles auf die große Alkoholmenge zurückzuführen sein… Denn der Alkoholgehalt von Absinth liegt zwischen 45 und 75 Vol%.
Der Hauptinhaltsstoff ist das bicyclische Monoterpen Thujon.
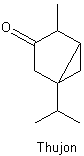
Der Name erinnert daran, dass man Thujon vor allem im Öl von Lebensbäumen (Thuja) gefunden hat. Diese Substanz ist auch in Salbei und Rainfarn enthalten.
Thujon ist in Alkohol, aber nicht in Wasser löslich. Deshalb bildet sich beim Verdünnen der alkoholischen Lösung mit Wasser die bekannte Emulsion. Den gleichen Effekt kennt man auch bei dem in Griechenland gängigen Ouzo® und bei dem türkischen Analogon Raki®. Letztere sind aber Schnäpse, die auf dem Terpen Anis beruhen.
Absinth war in Deutschland bis 1998 verboten, darf heute aber unter bestimmten Auflagen wieder verkauft werden. Außerdem kann man das Thujon weitgehend aus der Wermutpflanze entfernen. Das macht man zum Beispiel durch Extraktion mit überkritischem CO2. (Letzteres erklären wir am Beispiel des Entcoffeinierens von Kaffeebohnen.)
1703
F: Ist die Überhitzung eines Teelichtes durch ein abgebrochenes Stück Streichholz möglich?
Ich habe wie so oft mehrere Teelichter angezündet und sie auf meine Kommode gestellt: Beim Anzünden ist mir nicht aufgefallen, dass sich in einem der Teelichter ein bereits abgebrochenes Stück Streichholz befand. Als ich die Teelichter nach dem Abkühlen entsorgen wollte, verblieb unter dem Teelicht, in dem sich noch ein verbranntes Stück Streichholz befand, ein dunkler Fleck auf dem Furnier der Kommode.

(Foto: Annette)
Vielen Dank im Voraus für Ihre Antwort
Eine neugierige Schülerin
PS seit dem Ereignis stelle ich immer eine feuerfeste Unterlage unter die angezündeten Teelichter.
A: Das Streichholz hat offensichtlich mitgebrannt, also als großer Docht gewirkt.
Das hatte zur Folge, dass das Teelicht eine größere Flamme entwickelt hat als die anderen Teelichter, und dass es sich auch
entsprechend mehr aufgeheizt hat. Dafür spricht, dass der entsprechende Teelichtbecher völlig leergebrannt ist.
Normalerweise verlischt die Kerze, wenn noch etwas Wachs enthalten ist. Der Docht ist aus Gründen der Befestigung in ein rundes Metallplättchen eingelassen, brennt deswegen nicht komplett nach unten durch. Das verhindert aber auch übermäßige Aufheizungen.
Zu dem Fleck: Hierbei handelt es sich um verkohltes Furnier. Denn das geschmolzene Wachs von Teelichtern erreicht Temperaturen von weit über 350 °C. Der Becher sorgt wegen der guten Wärmeleitung von Metallen für Erhitzung auch der Unterlage - hier ist es das Furnier. Temperaturen über 300 °C sind schlicht zu heiß für ein Furnier, und deshalb sengt das an. Vor allem bei alten Furnieren, die noch mit Primitivklebern auf Knochenleimbasis fixiert sind, ist das denkbar. Da verkokelt der Eiweißanteil des Leims.
Deshalb haben Sie die einzig richtige Maßnahme ergriffen: Unter das Teelicht immer etwas wirklich gut Wärmedämmendes stellen - z. B. eine Kachel, wie wir es machen.
Selbst die mit Teelichtern beleuchteten Häuschen, die man auf dem Weihnachtsmarkt kaufen kann, haben einen Beipackzettel, auf dem hingewiesen wird, sogar noch unter den feuerfesten Häuschenboden aus Ton eine Unterlage wie einen Bierdeckel zu legen, weil die Hitze sogar durch die dicke Bodenschicht aus gebranntem Ton strahlt und den Tisch ansengen kann.
Hier noch als Ergänzung eine E-Mail
Habe selbst erlebt, dass ein ganz normales Teelicht, ohne sonstigen Inhalt, (Streichholz oder ähnliches) am Ende der Verbrennung
in der gesamten Alu-Schale vollflächig gebrannt hat.
Eine nicht brennbare Unterlage, welche zu wenig Wärme ableitet, verhindert die Überhitzung nicht!
Mein Tipp deshalb: Teelicht im Alubecher auf eine kleine Wasserpfütze (Tellerchen oder ähnliches) stellen. Die Temperatur geht
dann nicht über 100 °C, weil das Wasser erst verkochen muss.
Bitte verstehen Sie diese Mail als Dankeschön für das gesamte Team ihrer Website und nicht als Besserwisserei.
1704
F: Was ist eine Devarda-Legierung?
A: Die Devardasche Legierung ist eine Mischung aus Aluminium,
Kupfer und Zink. Die Massenverhältnisse sind
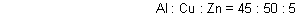
Sie wird zum Beispiel bei der Stickstoffbestimmung nach Kjeldahl eingesetzt, und zwar beim alkalischen Aufschluss. Hierbei wird eine Stickstoff-haltige Substanz zu Ammoniak reduziert, welches man abtrennt und titrimetrisch bestimmt.
Wegen des stark reduzierenden Milieus kann man auch Nitrat-Ionen aufschließen.
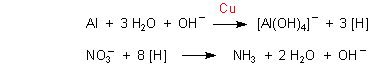
[H] bedeutet Wasserstoff in statu nascendi, also zum Beispiel atomarer Wasserstoff.
Aufgrund des alkalischen Milieus kann das Ammoniak simultan zur Entstehung direkt in eine säurehaltige Vorlage ausgetrieben werden. Sonst muss man das mit Hilfe der umständlicheren Wasserdampfdestillation machen.
Zur Funktion der Legierungsbestandteile:
Dass sich Aluminium in Natronlauge zersetzt, können Sie mit gut entfetteten Teebechern zeigen. Dabei wirkt Kupfer als Katalysator.
Das erkennen Sie, wenn Sie etwas Kupfersulfatlösung zutropfen. Klicken Sie hier. Ähnliches gilt
auch für Zink, das sich unter Komplexbildung in Natronlauge zersetzt.
1705
F1: Vielen herzlichen Dank für Ihre tolle Internetseite, die auch mir als Chemie-Laien
immer wieder Lust auf Chemie macht.
Leider habe ich eine Frage, die ich mit Hilfe meines Wissens nicht beantworten konnte: Natriumsulfit und Natriumhydrogenphosphat
wirken als als korrosionshemmende Substanzen. Wie kann man dies erklären?
Ich danke Ihnen sehr herzlich und bitte meine Anfrage zu entschuldigen.
A1: Danke für die netten Worte…
Zur Korrosion bedarf es neben Wasser (mit gelösten Elektrolyten) Säuren (genau genommen: Protonen) oder Sauerstoff. Letztere übernehmen Elektronen vom Eisen, das dann Ionen bildet und letztlich Rost ansetzen kann.
Natriumsulfit schafft einmal durch Hydrolyse ein alkalisches Milieu (wirkt also gegen Säurekorrosion) und verbraucht zweitens unter Bildung von Sulfat Sauerstoff (wirkt gegen Sauerstoffkorrosion).
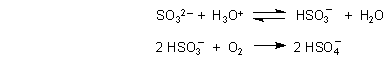
(Di)Natriumhydrogenphosphat sorgt nicht nur für schwach alkalisches Milieu, sondern auch für stabile Metallüberzüge (Bildung von schwerlöslichen Eisenphosphaten). Das bedeutet Schutz vor weiteren Angriffen. Man spricht von Passivierung.
Zur Korrosion und zum Korrosionsschutz haben wir Webseiten; z. B. auto/korrosio.htm.
F2: Vielen herzlichen Dank, dass Sie sich die Zeit genommen haben, meine Frage zu meiner
vollsten Zufriedenheit zu beantworten.