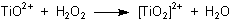
Nachweisreaktionen für Wasserstoffperoxid
Experimente:
Versuch: Nachweis von Wasserstoffperoxid mit Titanylsulfat
Versuch: H2O2-Zerfall und verschiedene Katalysatoren
Versuchsgruppe: Redoxreaktionen mit Wasserstoffperoxid
Versuch: Chromat katalysiert die Zersetzung von Wasserstoffperoxid
Versuch: Entfärbung von Bleisulfid - Wie ein Restaurator arbeitet
Es gibt verschiedene Nachweisreaktionen für Wasserstoffperoxid, was letztlich die Vielseitigkeit der
Reaktionen von H2O2 dokumentiert.
1 Nachweise mit Titanylsulfat und mit Chromat
Mit farblosem Titanylsulfat bildet sich ein tiefgelber Titan-peroxo-komplex.
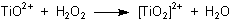
Diese Reaktion dient umgekehrt auch zum Nachweis von Titan.
Entsprechend bildet sich auch ein tiefblau gefärbter Chrom-peroxo-hydroxo-komplex aus Chromat(VI).
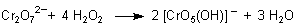
Zum Ablauf dieser Reaktion klicke hier.

(Foto: Daggi)
In beiden Fällen handelt es sich nicht um eine Oxidation, sondern um eine Komplexbildungsreaktion!
2 Katalysierte Zerfallsreaktionen (Disproportionierung)
Bei Zugabe von festem Braunstein schäumt die Mischung kräftig auf. Es bildet sich Sauerstoff.
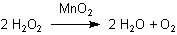
3 Reduktion von Kaliumpermanganat
Gegenüber starken Oxidationsmitteln wirkt H2O2 als Reduktionsmittel. Ein Beispiel,
das sich wegen der Farbänderung hervorragend zum Nachweis eignet, ist Kaliumpermanganat.
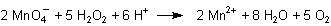
4 Oxidation von Mangan(II) zu Braunstein
Bekannter ist die Oxidationskraft von Wasserstoffperoxid. So oxidiert es in alkalischen Lösungen Mangan(II)
zu Mangan(IV), das als Braunstein (Manganoxidhydroxid) ausfällt.
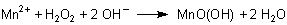
5 Oxidation von Iodid
Aus Iodid setzt H2O2 elementares Iod frei. Wichtig ist, dass die Lösung sauer sein muss,
da sonst die Oxidationskraft von H2O2 nicht ausreicht. (Klicke hier).
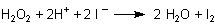
6 Oxidation von Bleisulfid
Schwarzes Bleisulfid wird schon in neutraler Lösung zu farblosem Bleisulfat oxidiert.
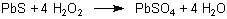
Weitere Texte zum Thema „Wasserstoffperoxid“