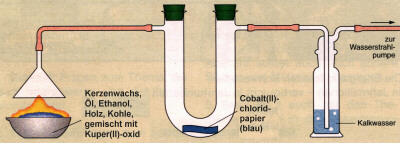
Versuch: Untersuchung von Brennstoffen auf die Elemente Kohlenstoff und Wasserstoff
Schülerversuch; 20 min.
Beim Experimentieren den Allgemeinen Warnhinweis unbedingt beachten.
Geräte
Porzellanschale, Glastrichter, U-Rohr, Waschflasche,
Stativ, Stopfen, Glasrohre, Wasserstrahlpumpe, Bunsenbrenner.
Chemikalien
Kerzenwachs, Holz, Kohle, Heizöl (F), Ethanol (F), Kupfer(II)-oxid (Xn),
Kalkwasser (C),
Cobaltchlorid-Papier (T).
Chemikalien
Die aufgeführten Brennstoffe werden jeweils in einer Porzellanschale
mit Kupfer(II)-oxid gemischt und mit der Brennerflamme entzündet. Falls die jeweilige Probe sich nicht
sofort entzünden lässt, muss sie ggf. mittels einer Heizplatte erwärmt werden.
Anschließend schiebt man die Schale, wie in der Abbildung dargestellt,
unter den Glastrichter der Apparatur und fängt die Reaktionsprodukte auf.

(Quelle: Cornelsen)
Beobachtung
Im U-Rohr kondensiert Wasser, welches mit Cobaltchlorid-Papier
nachgewiesen wird.
In der Waschflasche mit Kalkwasser bildet sich ein weißer
Niederschlag.
Auswertung
Die in Brennstoffen enthaltenen Wasserstoff- und
Kohlenstoffatome werden oxidiert:
4 H + O2 à
2 H2O
C + O2 à
CO2
Gleichzeitig wird das Kupfer(II)-oxid (Oxidationsmittel), welches den Sauerstoff für die Oxidationsreaktionen liefert, selbst zu Kupfer reduziert:
2 CuO à 2 Cu + O2
Cobaltchlorid-Papier enthält blaues Cobalt(II)-tetrachlorocobaltat(II), welches mit Wasser den rosafarbenen Hexaquocobalt(II)-chlorid-Komplex bildet:
Co[CoCl4] + 12 H2O à 2 [Co(H2O)6]Cl2
Kohlenstoffdioxid bildet mit Kalkwasser einen weißen Niederschlag aus feinverteiltem Calciumcarbonat:
CO2 + Ca(OH)2 à H2O + CaCO3 â
Literatur
R. Blume, Chemie für Gymnasien, Organische Chemie Themenheft 2, Cornelsen Verlag, Berlin 1994, 4.
H. Keune, W. Filbry, Chemische Schulexperimente, Verlag Harri Deutsch, Frankfurt a. M. 1978,
396.