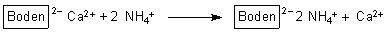
Ionenaustauscher - Ein historischer Streifzug
Experimente:
Versuch: Gartenerde als Ionenaustauscher
Seit unzähligen Jahrmillionen sind Ionenaustauscher in der festen Erdrinde, im Boden
und in Organismen tätig. Allerdings sollte dieser "wundersame" Vorgang des Ionenaustausches als
solcher erst Mitte des 19. Jahrhunderts als solcher erkannt und wissenschaftlich näher untersucht
werden.
Als möglicherweise erstes schriftliches Zeugnis für die praktische Anwendung des Prinzips des Ionenaustausch-Verfahrens zur Trinkwasseraufbereitung kann eine Textstelle aus dem Alten Testament angesehen werden (ca. 1200 v. Chr.):
| "Mose ließ Israel ziehen vom Schilfmeer hinaus zu der Wüste Schur. Und sie wanderten drei Tage in der Wüste und fanden kein Wasser. Da kamen sie nach Mara; aber sie konnten das Wasser nicht trinken, denn es war bitter. Daher nannte man den Ort Mara. Da murrte das Volk wider Mose und sprach: Was sollen wir trinken? Er schrie zu dem HERRN, und der HERR zeigte ihm ein Holz; das warf er ins Wasser, da wurde es süß." |
|
|
Der Ort Mara, an dem sich dieses Ereignis abgespielt haben soll, heißt übersetzt
Bitterquell oder Bitterbrunn (vgl. hebr. mara = bitter).
Verantwortlich für die Ungenießbarkeit des Wassers sind so genannte Bitterstoffe wie zum
Beispiel Bittersalz (Magnesiumsulfat = MgSO4· 7H2O).
Es scheint daher nicht abwegig zu vermuten, dass die "Verwandlung"
des bitteren Wassers in süßes, auf die Ionenaustauschfähigkeit
des ins Wasser gelegten alten Holzes zurückzuführen ist. (Diese Gegebenheit mag als ein Beispiel
dafür dienen, wie die Unkenntnis hinsichtlich chemischer und physikalischer Vorgänge Menschen
mitunter an "Wunder" glauben lassen können.)
Verantwortlich für den Ionenaustausch sind die Carboxyl- und Hydroxyl-Gruppen der Holzbestandteile.
Im Altertum, zu Zeiten des Aristoteles (384-322 v. Chr.), war bekannt, dass Seewasser und
auch unreines Wasser trinkbar gemacht werden konnte, wenn man es langsam durch Sand und
Erdschichten hindurchfließen ließ. Heute wissen wir, dass es sich bei diesem Vorgang hauptsächlich
um ein Filtern des Wassers handelt (vergleiche die Trinkwasseraufbereitung von Flusswasser).
Überdies wirken bestimmte Bestandteile der Erdschichten als Ionenaustauscher und tragen somit
zusätzlich zur Säuberung des Wassers bei.
Die Entdeckung der Ionenaustauscher lässt sich auf Untersuchungen der Engländer H.S.
Thompson (Landwirt), J. Th. Way (Agrikulturchemiker) und J. Spence (Apotheker)
zurückführen. Thompson fiel auf, dass im Dünger Verluste an Ammonium auftreten können.
Er veranlasste Spence daraufhin, das Verhalten wasserlöslicher Ammoniumsalze
im Boden zu analysieren. Dieser füllte eine Glassäule mit sandigem
Lehm, welcher mit Ammoniumsulfat ((NH4)2SO4)
versetzt war und versuchte dann, dieses auszuwaschen, indem er Regen simulierte und von
oben Wasser durch die gefüllte Glassäule laufen ließ.
Spence konnte im Durchlauf (Eluat) kein Ammoniumsulfat nachweisen, fand aber zu
seiner Verwunderung Gips (CaSO4· 2H2O) vor.
Bei dem beschriebenen Experiment dürfte es sich um die erste klare Angabe über einen
Ionenaustausch handeln. In Bezug auf den Mechanismus der Reaktion waren sich Thompson
und Spence jedoch, entsprechend dem damaligen Kenntnisstand, noch nicht im Klaren.
Erst Way erkannte kurze Zeit später, dass es sich bei der besagten Reaktion um einen
Ionenaustausch gehandelt hatte, wenngleich er sich nicht sicher war, welche Bestandteile des
Bodens dafür verantwortlich waren.
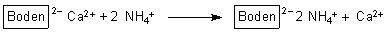
Im weiteren Verlauf seiner Untersuchungen entdeckte er, dass neben NH4+-Ionen auch
K+-, Mg2+- und Ca2+-Ionen
vom Boden ausgetauscht wurden (—> Versuch). Ferner erkannte er die große Bedeutung dieses Vorgangs
für die Pflanzenernährung.
1858 machten die Deutschen H. Eichhorn, W. Henneberg und F. Stohmann darauf
aufmerksam, dass bestimmte Tonmineralien (Beidellit, Kaolinit),
Grünsande, Zeolithe (Chabasit, Erionit, Mordenit) und
Humusstoffe für den Ionenaustausch im Boden verantwortlich sind.
Bei diesem als Basenaustausch bezeichneten Vorgang gelang es ihm ebenfalls, die Reversibilität
und Äquivalenz nachzuweisen. Eichhorn wies speziell beim Zeolithmineral Chabasit den Austausch von
Ca2+-Ionen gegen 2 Na+-Ionen nach.
Aufgrund dieser Erkenntnisse versuchte man nun natürliche Ionenaustauscher technisch zu
nutzen. 1896 wurden erstmalig natürliche Zeolithe in der Zuckerindustrie zum Ersatz
von Na+- und K+-Ionen durch Ca2+- und Mg2+-Ionen
in Zuckersäften eingesetzt.
Zu Beginn des 20. Jahrhunderts entwickelte R. Gans die ersten künstlichen Ionenaustauscher
durch Schmelzen von Quarz, Ton und Soda, wobei die wasserlöslichen Anteile anschließend ausgelaugt wurden.
Diese künstlichen Alumosilikate benannte man aufgrund ihrer Fähigkeit, bestimmte Ionen gegen andere
austauschen zu können, Permutite (vgl. lat. permutare = austauschen).
Die daraufhin gegründete Permutit AG stellte kurz darauf Permutite in großtechnischem
Maßstab her. Vor allem das Natriumpermutit ermöglichte eine bequemere, kostengünstigere und vor
allem auch eine präzisere Wasserenthärtung als bisher (z. B. Fällungsverfahren mit Ätzkalk (CaO),
Soda und Phosphaten):
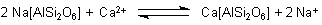
Vor allem Wäschereien waren Abnehmer des auf dieser Weise enthärteten Wassers, da hartes Wasser einen erheblichen Mehrverbrauch an Seife erforderte.
Die künstlich hergestellten Permutite eignen sich nur für den Neutralaustausch (Austausch eines Metall-Ions gegen die äquivalente Menge eines anderen Metall-Ions). Sie sind nicht in der Lage, Protonen gegen Metall-Ionen auszutauschen, da sie sich bei alkalischen und besonders sauren Reaktionen als sehr instabil erweisen.
Die Entdeckung, dass zermahlene Grammophonplatten Ionen austauschen können, inspirierte die Engländer B.A. Adams und E.L. Holmes 1935 dazu, Kunstharze mit ionenaustauschenden Eigenschaften auf dem Wege der Kondensation durch Phenolsulfonsäure und Phenyldiamin mit Formaldehyd zu synthetisieren. Dies stellte einen gewaltigen und richtungsweisenden Fortschritt in der Entwicklung der Ionenaustauscher. Die Vorteile der Kunstharz-Ionenaustauscher gegenüber den Permutiten und den natürlichen Austauschern liegen in der höheren Austauschkapazität, Austauschgeschwindigkeit, leichten Regenerierbarkeit und vor allem in der Stabilität gegenüber Säuren und Basen. Letzteres machte es möglich, Wasser vollkommen zu entsalzen, und zwar ohne den großen Energieaufwand einer Destillation.
Mit der Synthese von Kunstharz-Ionenaustauschern wurde ein Weg gefunden, die Eigenschaften der Austauscher bei der Herstellung planmäßig zu variieren. So konnten Ionenaustauscher produziert werden, die selektiv nur bestimmte Ionen austauschten (z. B. Rückgewinnung von Cadmium aus Galvanikbädern).
Anfang der 60er Jahre begann die Entwicklung von Chelatharzen und technisch brauchbaren Ionenaustauscher-Membranen zur elektrodialytischen Entsalzung von Meerwasser.
Bis heute finden die Ionenaustauscher neben ihrem Hauptanwendungsgebiet, dem Demineralisieren von Wasser, in zahlreichen Bereichen Anwendung.
Weitere Texte zum Thema „Ionenaustauscher“