Vollständiges Demineralisieren von Wasser durch Ionenaustausch
Experimente:
Versuch: Demineralisieren von Wasser durch Ionenaustausch
Versuch: Entfernung der Wasserhärte durch Kationenaustausch
Wenn Wasser durch das Erdreich fließt, löst es darin enthaltene Salze auf. In vielen Prozessen,
bei denen Wasser verwendet wird, wie z. B. beim Spülen, als Wärmeträger oder als Lösungsmittel, stören
diese gelösten Salze. Entweder kristallisieren sie beim Verdunsten aus und bilden störende
Ablagerungen, oder sie wechselwirken bzw. reagieren mit den zu lösenden Stoffen. Hier sei an die
Wasserhärte erinnert. Außerdem fördern Ionen sehr stark
Korrosionsprozesse.
Die Salze müssen also entfernt werden. Hierfür eignet sich zum einen das Destillieren und zum anderen
das Demineralisieren durch Ionenaustauscher. Ersteres ist heutzutage aber nicht mehr wirtschaftlich bzw.
konkurrenzfähig genug, um neben dem Verfahren mit Ionenaustauschern noch bestehen zu können.
Bei der Demineralisierung werden sämtliche im Wasser gelösten Salze in zwei Schritten entfernt.
1. Stufe der Entsalzung
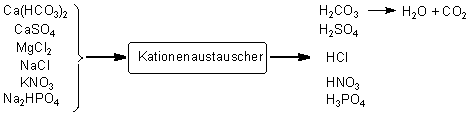
Hierfür wird das Wasser zuerst über einen Kationenaustauscher geleitet. Es werden alle Kationen
gegen Protonen ausgetauscht, wobei freie Mineralsäuren gebildet werden. (Deshalb sinkt der pH-Wert
deutlich ab.) Dieser Vorgang wird auch als Entbasung bezeichnet.

Das nach dem Kationenaustausch säure- und CO2-haltige Wasser wird in größeren Anlagen durch Einblasen von Frischluft entgast und somit weitgehend von gelöstem CO2 befreit.
2. Stufe der Entsalzung
Der saure Ablauf aus dem Kationenaustauscher wird nun über einen Anionenaustauscher geleitet.
Die Anionen der Kieselsäure, Kohlensäure und der zuvor entstandenen Mineralsäuren werden gegen
Hydroxid-Ionen ausgetauscht. Dieser Vorgang wird als Entsäuerung bezeichnet.

Die Hydroxid-Ionen verbinden sich mit den Protonen aus dem ersten Schritt und es entsteht Wasser (-> Versuch).
Die Wirksamkeit der Ionenaustauscher kontrolliert man durch Leitfähigkeitsmessungen am zuletzt austretenden Wasser.
In der Industrie verwendet man große, mit Kunstharz-Ionenaustauschern gefüllte Behälter. Entweder wird das zu demineralisierende Wasser - wie oben beschrieben - erst durch einen Kationenaustauscher und anschließend durch einen Anionenaustauscher geführt (Mehrbett-Anlage) oder aber durch einen Behälter, in dem Kationen- und Anionenaustauscher gemischt vorhanden sind (Mischbett-Anlage).
Oftmals reicht es aus, nur die Wasserhärte verursachenden Kationen (Mg2+, Ca2+) und Anionen (Carbonat, Sulfat usw.) zu beseitigen. Dieses Enthärten erfolgt mit neutralen Kationenaustauschern in der Na+-Form sowie neutralen Anionenaustauschern in der Cl--Form. Über die Wasser-Enthärtung berichten wir hier.
Bisher gibt es noch keine einheitliche Bezeichnung für Wasser, welches auf diese Art und Weise von seinen gelösten Salzen befreit wurde. Du findest Begriffe wie "entsalztes", "deionisiertes", "entmineralisiertes", "vollentsalztes" oder "demineralisiertes" Wasser. In der Pharmazie spricht man auch von "Aqua demineralisata". Auf jeden Fall ist es kein "destilliertes Wasser".