 |
| Kupfermineralien: Azurit, Malachit, Buntkupfererz,
Kupferkies
(Foto: Blume) |
Umweltschonende Aufbereitung von Kupfererzen
Experimente:
Versuch: Reinigung von Verkupferungsbädern mit Kationenaustauschern
Versuch: Abtrennung und Anreicherung von Kupfer-Ionen durch Ionenaustausch
Versuch: Anreicherung von Kupfer-Ionen mit einem flüssigen,
komplexierenden Ionenaustauscher
Versuch: Komplexierung von Kupfer(II)-Ionen durch einen chelatbildenden Ionenaustauscher
Eine Voraussetzung zur wirtschaftlichen Gewinnung von Metallen ist ein abbauwürdiges
Erzvorkommen, bei dem die gesuchten Metalle oder ihre Verbindungen in einer solchen Konzentration
vorhanden sind, dass sich die Ausbeutung der Lagerstätten lohnt. Aus diesem Grund haben sich in den
letzten Jahrzehnten starke Verschiebungen ergeben: So werden die mageren deutschen Eisenerze - z. B.
im Siegerland oder bei Salzgitter - kaum mehr genutzt, da es kostengünstiger ist, südamerikanische
Erze einzuführen. Erst wenn solche Vorkommen erschöpft sind, wird man wieder auf weniger ergiebige
Quellen zurückgreifen müssen.
Leider zeigt jedoch die Erfahrung, dass mit abnehmender Konzentration des Metalls in einem Gestein
der Aufwand zur Gewinnung größer wird, da mehr Energie zum Abtrennen der unerwünschten Begleitstoffe
aufgebracht werden muss. Zudem steigt noch die Umweltbelastung. Es ist somit anzustreben, Verfahren zu
entwickeln, um auch Erze mit niedrigem Metallgehalt so aufzuarbeiten, dass dies nicht nur möglichst billig,
sondern auch besonders umweltschonend geschieht.
Ein Beispiel ist die Gewinnung von Kupfer. Dieses Metall ist besonders wegen seiner hohen elektrischen
Leitfähigkeit, seiner Beständigkeit und als wichtiges Legierungsmetall von großer wirtschaftlicher Bedeutung.
Kupfer, das nur in geringen Mengen gediegen vorkommt, wird vor allem aus Chalkopyrit (Kupferkies, CuFeS2)
und weiter aus anderen Erzen wie Malachit (CuCO3· Cu(OH)2) gewonnen.
 |
| Kupfermineralien: Azurit, Malachit, Buntkupfererz,
Kupferkies
(Foto: Blume) |
Die weltweit bekannten Kupfervorkommen enthalten im Durchschnitt nur etwa 1-2 % Kupfer. Aufgrund
des Schwefelanteils vieler Erze sowie wegen des Gehalts an anderen, sehr giftigen Schwermetallen und
an Arsen besteht das Problem, Kupfer unter möglichst geringen Umweltbelastungen und zugleich
wirtschaftlich lohnend zu gewinnen.
Das klassische Verfahren zur Kupfergewinnung ist umweltbelastend
Ein Beispiel zur pyrometallurgischen Gewinnung von Reinkupfer ist
die Aufarbeitung von Kupferkies. Der Prozess ist in der folgenden Abbildung schematisch dargestellt.
Man kann deutlich erkennen, dass es sich hierbei um ein sehr aufwendiges Verfahren handelt.
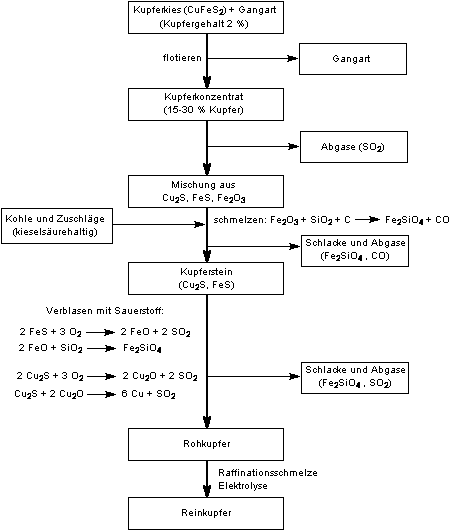
Pyrometallurgische Gewinnung von Kupfer aus Kupferkies
(Quelle: [1])
Bei den ersten vier Arbeitsgängen entstehen erhebliche Mengen Schlacke und Schwefeldioxid.
Zur Abtrennung weiterer Verunreinigungen wie Blei, Zink, Antimon, Arsen, Nickel und Eisenresten
wird das Rohkupfer einer erst oxidierenden, dann reduzierenden Raffinationsschmelze unterworfen.
Hierbei verflüchtigen sich Schwermetalle wie Zink und Blei sowie Arsen und Antimon und müssen aus
der Abluft abgeschieden werden. Nickel und Eisen verschlacken mit den beigegebenen Zusätzen. Bei
der anschließenden elektrolytischen Raffination erhält man das für technische Zwecke erforderliche,
äußerst reine Kupfer. Vorhandene Edelmetalle sammeln sich im Anodenschlamm.
Das bei der Verhüttung der Kupfererze anfallende Schwefeldioxid wird heute üblicherweise zur
Gewinnung von Schwefelsäure eingesetzt.
Umweltverschmutzungen durch Kupferhütten, die sulfidische Erze
nach diesem "klassischen" Verfahren verarbeiten, waren in der Vergangenheit üblich. So emittierte
eine Kupferschmelze in Butte Anaconda (USA) bereits 1907 täglich 18 t Arsen, 1,7 t Kupfer
und fast ebenso viel Antimon. (Über den Schwefeldioxidausstoß wird nichts berichtet.) Die Emissionen
einer anderen Hütte in Kalifornien verseuchten 2300 km2 Land mit Arsen.
Die hydrometallurgische (nasschemische) Aufarbeitung von Kupfererzen
ist umweltschonender
Zementation
Für oxidische Erze, die sich nicht durch Flotation anreichern lassen, ist eine nasschemische
Verarbeitung vorteilhaft.
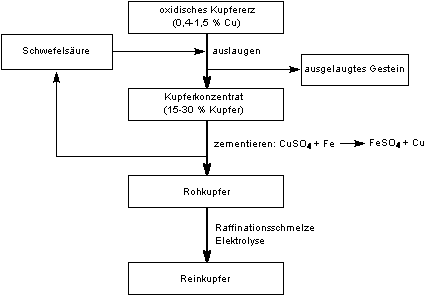
Kupfergewinnung durch Zementation
(Quelle: [1])
Der saure Extrakt wird mit Eisenschrott versetzt, wobei das Eisen in Lösung geht und das edlere Kupfer
zum Metall reduziert wird. Bei diesem Zementation genannten Prozess besteht der
Nachteil darin, dass die Schwefelsäure bei mehrmaliger Verwendung mehr und mehr neutralisiert wird und
sich mit Eisensulfat anreichert. Weiter wird elementares Eisen benötigt. Zudem muss das erhaltene Kupfer
in einem anschließenden Schritt durch Raffinationsschmelzen von Verunreinigungen
wie Eisen, Blei, Zink, Zinn, Arsen und Antimon befreit werden. Erst dann kann es durch Elektrolyse zu
Kupfer mit einem Reinheitsgrad von 99,95 % verarbeitet werden.
Selektiver Ionenaustausch
Eine neue und wesentlich einfachere Technologie vermeidet viele der oben angeführten Nachteile.
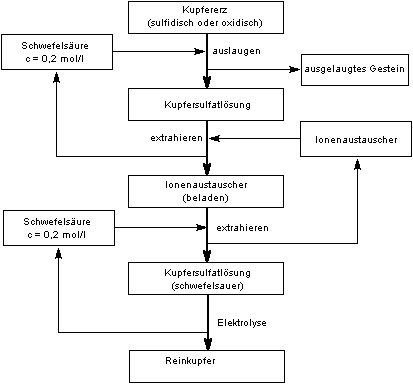
Kupfergewinnung durch Extraktion mittels Ionenaustauscher
(Quelle: [1])
Zunächst wird das Kupfererz, wie bei dem oben beschriebenen Prozess, mit Schwefelsäure behandelt.
Die erhaltene Lösung wird mit einem wasserunlöslichen, flüssigem niedermolekularen
Ionenaustauscher extrahiert, der in hochsiedenden Kohlenwasserstoffen gelöst ist. Die
dabei ablaufende Reaktion kann man am Beispiel des 2-Hydroxy-5-dodecyl-benzophenoxims betrachten.
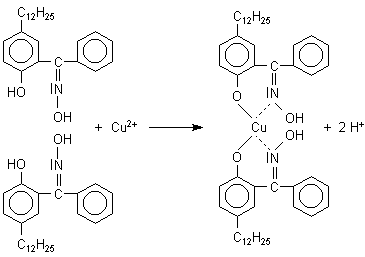
Beispiel für einen löslichen Ionenaustauscher zur Kupfergewinnung
(Quelle: [1])
Hierbei handelt es sich um einen chelatbildenden Ionenaustauscher.
Durch die selektive Wirkung des Austauschers werden dabei der wässrigen Phase nur die
Kupfer-Ionen entzogen und gegen Protonen ausgetauscht (-> Versuch).
Die vom Kupfer befreite Schwefelsäure wird erneut zum Aufschluss von frischem Erz verwendet.
Der mit Kupfer-Ionen beladene Ionenaustauscher wird mit höher konzentrierter Schwefelsäure
behandelt. Dabei werden die Kupfer-Ionen in die Säurephase überführt und zugleich angereichert.
Der Ionenaustauscher liegt danach wieder in der H+-Form vor. Aus der gewonnenen
schwefelsauren Kupfersulfatlösung wird das Kupfer elektrolytisch abgetrennt. Die hinterbliebene
Schwefelsäure dient wieder zur Regeneration von beladenem Ionenaustauscher.
Das gesamte Verfahren besteht aus drei ineinander verschachtelten Kreisprozessen. Es wird deutlich,
dass im Gegensatz zum klassischen Verfahren keine schädlichen Abgase wie Schwefeldioxid entstehen.
Außerdem lassen sich auch gering konzentrierte Kupfererze sowie Haldenmaterial Gewinn bringend
aufbereiten.
Quelle: [1]
Weitere Texte zum Thema „Ionenaustauscher“