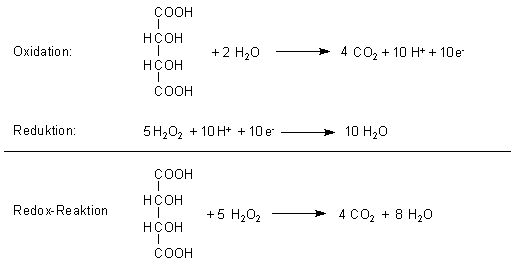
Katalytische Wirkung von Cobaltsalzen
Experimente:
Versuch: Die durch Cobalt katalysierte Oxidation von Weinsäure
Weinsäure wird durch Wasserstoffperoxid unter der katalytischen Einwirkung von
Cobaltchlorid zu Wasser und CO2 oxidiert.
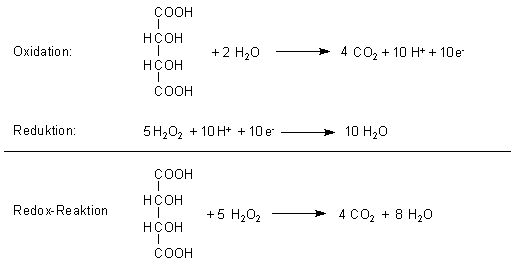
Dabei nimmt das Co2+-Ion aktiv an der Reaktion teil. Das erkennt man aufgrund der
Farbänderung während des Versuchs.
Hier ist die Schilderung des Ablaufs der Reaktion: Zunächst gibt man zur sauren
rosaroten Cobalt(II)-Lösung Weinsäure. Nach Zugabe von Wasserstoffperoxid färbt
sich die Lösung über die Mischfarbe Braun nach Grün um. Parallel dazu setzt die
Oxidationsreaktion unter Freisetzung von großen Mengen an CO2 ein. Nach
Beendigung der Reaktion (erkenntlich am Nachlassen der Gasbildung) wird die
Lösung wieder rot.
 |
| Die durch Cobalt katalysierte Oxidation von Weinsäure (Foto: Daggi)
Hierzu gibt es einen Film (9 MB) Klicke hier |
Die intermediär auftretende grüne Farbe rührt von einem dimeren
Cobalt/Weinsäure/Wasserstoffperoxid-Komplex her. Zum Verständnis des
Komplexaufbaus muss man wissen, dass die Koordinationszahl des Cobalt(II)-Ions 6
beträgt. Weinsäure und Wasserstoffperoxid sind zweizähnige Liganden.
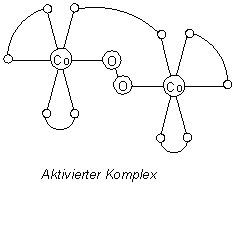
Dies ist die aktive Zwischenverbindung. In ihr sind die eigentlichen Reaktanden
Weinsäure und H2O2 sterisch so ausgerichtet, dass die oxidative Spaltung desjenigen
Weinsäuremoleküls, das innerhalb dieses Komplexes die Brücke zwischen den
Co2+-Ionen bildet, optimal ablaufen kann. Dabei werden die Co2+-Ionen
zurückgebildet. Nach der Reaktion färbt sich die Lösung deshalb wieder rot.
Dieser Versuch beweist also nicht nur das Vorliegen eines aktiven
Übergangskomplexes, sondern gibt darüber hinaus auch Einblick in den
Wirkungsmechanismus eines Katalysators. Durch diese sterische Ausrichtung wird die
Aktivierungsenergie deutlich gesenkt.
Bemerkenswert ist, dass auch Enzyme durch die Geometrie ihres aktiven Zentrums
ähnlich wirken.
Zur Chemie mit Wasserstoffperoxid haben wir eine große
Webseitengruppe.
Weitere Texte zum Thema „Katalyse“