Klassische Farbreaktionen zum Nachweis der Kohlenhydrate
Experimenteliste zu den Kohlenhydraten
Beim Experimentieren den Allgemeinen Warnhinweis unbedingt beachten.
Es gibt aus der Medizinischen Laborchemie früherer Tage eine Reihe von Experimenten zur Analytik,
die recht abenteuerliche Reaktionsmischungen zur Voraussetzung hatten. Beteiligt sind stets Aldehyde
und Phenole, die unter geeigneten Bedingungen zu Farbstoffen reagieren.
Immer wieder werden wir gefragt, was denn dabei vorgeht. Gleich vorneweg sei gesagt, dass es keine gesicherten Kenntnisse über die genauen chemischen Abläufe gibt.
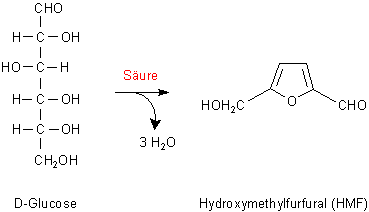
Durch konzentrierte Säuren wird den Hexosen bzw. Pentosen Wasser entzogen. Es entstehen Hydroxymethylfurfurol bzw. Furfurol (auch Furfural genannt).

Diese koppeln (protonenkatalysiert) mit zwei Molekülen einer Phenolkomponente zu Farbstoffen, die den Triphenylmethanfarbstoffen ähneln.
Die folgenden Proben sind auch heute noch wichtig, weil sich damit auch rasch nachweisen lässt, ob ein Lebensmittel Kohlenhydrate enthält. In der Labormedizin dagegen verfügt man über bessere Hilfsmittel. Besonders effektiv sind enzymatische Methoden.
Molisch-Probe
Reaktion auf alle Kohlenhydrate (bis auf Desoxyribose), auch auf Polysaccharide und auf alle
Kohlenhydrat-haltigen Verbindungen wie z. B. RNA und Glykoproteiden. Deshalb sehr unspezifischer
Nachweis.
1 ml einer 3%igen Glucoselösung wird in einem Reagenzglas mit 2 Tropfen einer 10%igen ethanolischen
Lösung (F) von sauberem a-Naphthol (Xn) vermischt.
Man unterschichtet mit 4-5 ml sauberer konzentrierter Schwefelsäure (C).
Ergebnis:
An der Berührungsstelle der beiden Flüssigkeiten entsteht ein rotvioletter Ring.
Erklärung:
Durch die Schwefelsäure wird den Hexosen bzw. Pentosen Wasser entzogen. Es entstehen Hydroxymethylfurfurol
bzw. Furfurol. Diese koppeln mit a-Naphthol zu einem Farbstoff.
Seliwanoff-Probe
Probe auf Ketosen
2 ml einer 3%igen Fructoselösung werden im Reagenzglas mit 1 ml konzentrierter Salzsäure (C) vermischt. Dazu
gibt man einige Tropfen einer 1%igen ethanolischen Lösung (F) von Resorcin (Xn) und kocht. Der Versuch wird auch
mit Glucose und mit Saccharose wiederholt.
Ergebnisse:
Mit Fructose tritt rasch eine rote Färbung ein.
Bei Glucose bleibt die Reaktion aus oder die Färbung stellt sich nur langsam ein.
Auch bei Saccharose bildet sich die rote Farbe nur langsam, weil erst einmal durch Säurehydrolyse Fructose entstehen muss.
Erklärung:
Auch hier wird aus den Kohlenhydrat-Molekülen (diesmal unter Wirkung der Protonen der HCl) Wasser abgespalten und es
entsteht Hydroxymethylfurfural (HMF).
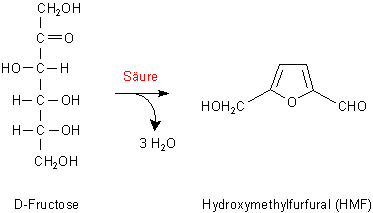
Dieser aromatische Aldehyd reagiert mit zwei aktivierten aromatischen Verbindungen wie dem Resorcin oder Naphthol.
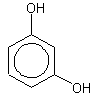
Resorcin
Dabei bildet sich wahrscheinlich ein roter Tri-Aryl-Methan-Farbstoff, der so aussehen könnte:
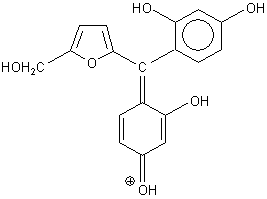
(Die Bezeichnung Aryl steht für einen beliebigen aromatischen Rest.)
Diese Reaktion beobachtet man zwar auch bei Aldosen wie Glucose. Bei Ketosen wie Fructose verläuft die Bildungs-Reaktion von Hydroxymethylfurfural jedoch wesentlich schneller. Dadurch ist die Konzentration des reaktiven Aldehyds von Anfang an hoch. Folglich ist eine Farbänderung im Falle des Vorliegens einer Ketose rasch zu erkennen.
Furfurolreaktionen
Nachweise auf Pentosen. Desoxyribose reagiert nicht, weil sie kein Furfural bilden kann.
1 Phloroglucinprobe
1 ml einer frisch hergestellten 0,5%igen Pentose-Lösung (z. B. von Arabinose) wird im Reagenzglas mit 2 ml
konzentrierter Salzsäure (C) und 0,5 ml einer 1%igen ethanolischen Lösung (F) von Phloroglucin (Xn) vermischt.
Man erhitzt langsam.
Ergebnis:
Die Lösung färbt sich rot.
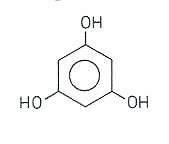
Phloroglucin
2 Orcinprobe
1 ml einer frisch hergestellten 0,5%igen Pentose-Lösung (z. B. von Arabinose) wird im Reagenzglas mit 2 ml
konzentrierter Salzsäure (C) und 0,5 ml einer 1%igen ethanolischen Lösung (F) von Orcin (Xn) vermischt. Man erhitzt
langsam.
Ergebnis:
Die Lösung färbt sich grün.
Erklärung:
Hierbei entsteht nur Furfurol. Zur Sicherheit kann man das Furfurol sogar noch in eine Vorlage abdestillieren
und hierin nachweisen. Hydroxymethylfurfurol ist nämlich nicht flüchtig.
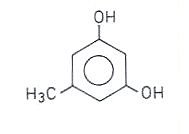
Orcin
Quelle der Nachweisreaktionen:
Physiologisch-Chemisches Praktikum; Hrsg. Physiologisch-Chemisches Institut der Universität Tübingen, 1964.
Weitere Texte zum Thema „Kohlenhydrate“