
“Enthält eine Phenylalaninquelle“: Phenylketonurie

Bild 1: Etikettenausschnitt eines Light-Getränks
Etiketten vieler Light-Getränke tragen den folgenden Warnhinweis:
"Enthält eine Phenylalaninquelle".
Der Hinweis betrifft den technischen Süßstoff Aspartam. Hinter diesem Namen verbirgt sich ein Dipeptid aus L-Asparaginsäure und dem Methylester von L-Phenylalanin: L-Asp-L-Phe-methylester.
(1)
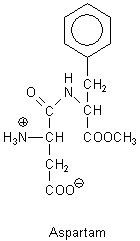
Es handelt sich um einen kalorienarmen Süßstoff, bei dessen Abbau die Aminosäure
Phenylalanin freigesetzt wird. Das sollte sich doch positiv auswirken, denn Phenylalanin gehört schließlich
zu den acht essentiellen Aminosäuren *). Diese kann unser Organismus nicht selbst herstellen. Deshalb sind wir auf ihre
Zufuhr durch die Nahrung angewiesen. Wir benötigen pro Tag ca. 2,5 g Phenylalanin.

Bild 2: Kalottenmodell von Phenylalanin
(Foto: Daggi)
Warum ist dann überhaupt der Warnhinweis vorgeschrieben? Aspartam ist gefährlich für Kinder, die unter der gar
nicht so seltenen Erbkrankheit Phenylketonurie (PKU) leiden. Diesen Kindern fehlt
ein Enzym, das beim Abbau der Aminosäure Phenylalanin mitwirkt.
Der normale Abbau von Phenylalanin
Dieser verläuft in der Leber über die Aminosäure Tyrosin. Dazu wird Phenylalanin zunächst am aromatischen Kern
hydroxyliert. Das geschieht mit molekularem Sauerstoff. Von einem Molekül O2 wird dabei ein O-Atom auf
Phenylalanin übertragen. Das andere O-Atom reagiert gleichzeitig mit einer Wasserstoff „spendenden“ Verbindung namens
Tetrahydro-Biopterin, wobei ein Molekül Wasser entsteht. Das Enzym ist somit eine mischfunktionelle Oxidase.
Man spricht auch von einer Monooxigenase oder auch Hydroxylase. Der übliche Name des Enzyms ist
Phenylalanin-Hydroxylase.
(2)
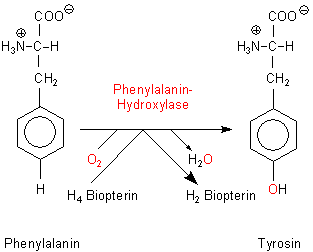
(Für den Abbau von Tyrosin gibt es eine Vielzahl von weiteren Stoffwechselwegen.)
Der atypische Abbau von Phenylalanin
Wenn wie bei den erbkranken Kindern dieses Enzym fehlt, reichert sich Phenylalanin im Blutplasma an und erreicht Konzentrationen
von 20-60 mg/100 ml. (Normal wären 1-4 mg/100 ml.) Dann schaltet der Abbau auf einen alternativen Stoffwechselweg um: Es findet
ein Transfer der Aminogruppe statt. Es bildet sich Phenylpyruvat.
(3)
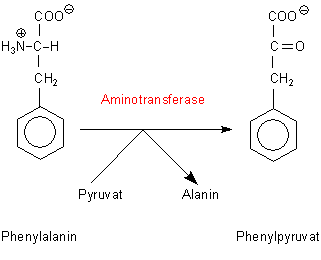
(Das entstehende Phenylpyruvat kann noch weiter verstoffwechselt werden. Es bilden sich dann Phenyllactat, Phenylacetat
und entsprechende, am aromatischen Ring hydroxylierte Verbindungen.)
Phenylpyruvat könnte als Keton nerventoxisch sein. Darauf führte man früher ein typisches Krankheitsbild der PUK zurück, die verzögerte geistige Entwicklung der betroffenen Kinder. Jedoch kann das auch damit zusammenhängen, dass bei der PUK die Serotoninsynthese aus Tryptophan gehemmt ist.
Nur mit Hilfe einer von Anfang an anhaltenden und konsequenten Steuerung der Zufuhr an Phenylalanin wird verhindert, dass sich die Symptome von PUK manifestieren.
Man kann aber auch nicht zur Gänze auf Phenylalanin verzichten, denn ein Minimum dieser essentiellen Aminosäure ist zum Leben notwendig. Zum Beispiel gibt kaum menschliche Proteine, die ohne Phenylalanin auskommen. Zu bedenken ist auch, dass über Tyrosin der Neurotransmitter Noradrenalin hergestellt wird und letztlich auch das Hormon der Nebenniere, Adrenalin, das u. a. bei der Steuerung des Kohlenhydratstoffwechsels mitwirkt.
Um das zu gewährleisten, wird das Blut von Neugeborenen sofort auf PUK untersucht. Das wird teilweise noch mikrobiologisch gemacht. Dieser nach seinem Entwickler benannte Guthrie-Test weist aber viele Fehlerquellen auf. Mittlerweile erfolgt zumindest in Deutschland der Nachweis von atypischen Abbauprodukten des Phenylalanins mit massenspektrometrischen Methoden.
______________________________________________________________________________________________________
*) Essentielle Aminosäuren:
Valin (Val), Phenylalanin (Phe), Leucin (Leu), Isoleucin (Ile), Threonin (Thr), Tryptophan (Trp), Methionin (Met), Lysin (Lys)
Weitere Texte zum Thema „Kohlenhydrate“