 |
| Bild 1: Von uns gezüchteter
Einkristall von Alaun
(Foto: Daggi) |
Wie züchtet man Einkristalle?
Experimente:
Versuchsgruppe: Züchten schöner Kristalle
 |
| Bild 1: Von uns gezüchteter
Einkristall von Alaun
(Foto: Daggi) |
Einkristalle sind ideal aufgebaute kristalline Materiestücke,
in denen das Kristallgitter in allen Richtungen die gleiche Orientierung hat.
Im Labor gelingt es sogar unerfahrenen Schülern leicht, Einkristalle zumindest von Salzen zu züchten (-> Versuchsgruppe). Diese lassen ihre Kristallsysteme und Kristallklassen leicht erkennen. Auch weißer Kandiszucker besteht aus Einkristallen. Die sind zwar hübsch, aber technisch leider ohne Bedeutung.
Technisch hergestellt weisen Einkristalle im Allgemeinen eine hohe Reinheit auf. Das
unterscheidet sie von den natürlichen: Nur ein Diamant mit natürlichen
Verunreinigungen ist ein echter!
Von Vorteil ist, dass man bei der Züchtung dieser Einkristalle auch gezielt
"Verunreinigungen" einbauen kann. Man spricht hierbei von "Dotieren". Das ist ganz
besonders in der Halbleiter-Technologie der Fall. Ohne diese Technik könnte man
keine Transistoren oder Gleichrichter bauen. Hierzu dotiert man Silicium mit Phosphor-, Arsen
sowie Antimon-Atomen (-> n-Leiter) oder mit Bor- sowie Aluminium-Atomen (->
p-Leiter).
Mit Einkristallen gelingt auch besonders gut der Blick ins Kristallgitter. Das ist besonders bei kompliziert aufgebauten Kristallen wie dem eines Proteins oder von DNA notwendig. Dann kann man sogar die Strukturen der Makromoleküle entschlüsseln.
Beispiele für interessante Einkristalle
Natürliche, wasserklare Einkristalle schätzt man z. B. beim Kalkspat (Calcit). Denn nur dieser
in dieser reinen Form zeigen sie die Eigenschaft der Doppelbrechung,
die man zur Herstellung von Polarisationsprismen benötigt ("Nicols"). (Doppelbrechung tritt
natürlich auch bei anderen kristallinen Substanzen auf. Beim Calcit ist dieses Phänomen allerdings
so stark ausgeprägt, dass es auch in dünnen Schichten bereits mit dem freien Auge sichtbar ist.)
 |
| Bild 2: Einkristalliner Kalkspat
(Foto: Blume) |
Schwierig ist es, Einkristalle von Festkörpern wie Metallen, Silicium, Rubinen oder Quarz
herzustellen. Diese braucht man aus technischen Gründen. Hier einige Beispiele:
| - | Hochbelastete Metalle reißen an den Kristallgrenzen. Bei den Turbinenschaufeln geschieht dies aufgrund hoher Temperatur und hoher Fliehkräfte wegen der Rotation der Schaufelräder. | ||
| - | Kristallgrenzen bedeuten Störung des elektrischen
Verhaltens von Halbleitern. Deshalb werden elektronisch einheitliche, einkristalline
Silicium-Platten ("Wafer") zur
Chipherstellung benötigt. Aber auch bei der Fotovoltaik [26] nutzt man diese
wegen des höheren Wirkungsgrads am liebsten.
| ||
| - | Rubine können nur als Einkristalle ihre Wirkung in der Lasertechnik als optisch aktiver Licht-Verstärker voll entfalten. | ||
| - | Kaliumbromid ist das Material von Prismen und Fenster in der Infrarot-Technik. Seine minimalen Adsorptionseigenschaften werden durch Polykristallinität gestört. | ||
| - | Quarze kann man nur dann richtig bezüglich ihrer optischen Achse beurteilen, wenn man sie rein gezüchtet hat. Denn Schnitte bezüglich dieser Achse entscheiden über die Schwingfähigkeit von a-Quarz, der zur Herstellung von Quarzuhren verwendet wird, da dies eine durch die Kristallsymmetrie bestimmte, richtungsabhängige ("anisotrope") stoffliche Eigenschaft ist. | ||
| - | Diamanten bilden im Allgemeinen von der Natur her Einkristalle, allerdings zeigen sie Verunreinigungen, die sie für viele technische Zwecke nicht geeignet erscheinen lässt. | ||
| - | Chromdioxid CrO2: Mit diesen sind magnetische Aufzeichnungsträger wie Ton- und Videobänder sowie Computer-Disketten beschichtet. |
Exemplarische Zuchtverfahren für Einkristalle
Hydrothermal-Synthese
Darunter versteht man Kristallisation von Substanzen aus wässrigen Lösungen,
die unter hohem Druck und somit auch unter hohen Temperaturen stehen. Bei dieser
Hochdruckchemie unter gleichzeitig hohen Temperaturen bildet man die natürlichen,
meist vulkanischen Entstehungsbedingungen ("hydrothermale Prozesse") vieler, auch
deutscher Mineralienlager nach. So findet man z. B. in der Gegend des
Wiehengebirges (Porta Westfalica bei Minden) und den nahegelegenen Bädern wie
Bad Oeynhausen Drusen, in denen teilweise doppelendig ausgebildete Bergkristalle
oder Zepterquarze liegen. Das betrifft auch die Hohlräume von Fossilien! Aber auch
die Gegend um Bleiwäsche im Sauerland gehört hierzu. Weiter sind die (allerdings
amorphen) Opale in Australien hydrothermalen Ursprungs.
 |
| Bild 4: Hydrothermal gebildeter
Quarz-Doppelender in einer Druse (Lippisches Bergland)
(Foto: Daggi) |
Das technische Beispiel ist vor allem der trigonale a-Quarz, aber auch der Smaragd.
Auch Chromdioxid-Kristalle werden nach diesem Verfahren hergestellt.
 |
| Bild 5: Hydrothermale Mineralienbildung in einem
Ammoniten (Macrocephalus macrocephalites ("großkopferter Großkopf"); Dogger, Porta Westfalica) (Foto: Blume) |
Konkret geht man so vor, dass man einen mit Wasser gefüllten Druckautoklaven, der
im unteren Teil feinverteilten, sauberen Naturquarz und im oberen Teil aufgehängt
Quarz-Impfkristalle enthält, erhitzt. Dabei legt man einen Temperatur-Gradienten an:
Im unteren Teil beträgt die Temperatur 400 °C, im oberen nur 380 °C. Unten löst sich
der Quarz, die Lösung steigt durch Konvektion nach oben. Hier ist sie aufgrund der
niedrigeren Temperatur übersättigt; Quarz scheidet sich an den Impfkristallen
einkristallin ab. Innerhalb von ein bis zwei Monaten bilden sich Kristalle von mehr als
einem Kilogramm Masse![19] Diese werden exakt auf ihre Symmetrie-Eigenschaften
überprüft und zur Herstellung von Schwingquarz-Plättchen entsprechend
zerschnitten.
Ziehen von Einkristallen aus Schmelzen
(Czochralski -Verfahren)
Hierzu schmilzt man das zuvor z. B. durch Zonenschmelzen
hochgereinigte Material wie Silicium in einem inerten Tiegel. Man
taucht einen wenige mm dicken Impfkristall hinein und dreht und zieht diesen, um die
Bildung von Versetzungen im Kristallgitter, die zur Polykristallinität oder zur
Zwillingsbildung führen könnten, zu unterbinden. Die so zu Beginn der Kristallisation
entstandene, versetzungsfreie Zone verbreitert man langsam auf den gewünschten
Durchmesser des Einkristalls. Die Verunreinigungen bleiben in der Schmelze
zurück. Hier wendet man die Gesetze der Schmelzpunktserniedrigung an.
Bildung von Einkristallen durch Zonenerhitzen
Zur Herstellung von Wolfram-Einkristallen zieht man z. B. einen Stab aus
Wolframpulver, der mit Bindemittel angeteigt ist, durch einen kleinen, engen
Elektro-Ofen. Bei der dort erreichten Temperatur von 2400-2600 °C orientieren sich die
Atome im Faden, ohne dass er schmilzt, zu einem meterlangen Einkristall.
Zonenschmelzverfahren
Der zuvor grob gereinigte Siliciumstab wird an einem Ende in einer schmalen Zone induktiv
erhitzt. Die Induktionsspule führt man so über den Kristall, so dass die
Schmelzzone langsam über den Stab hinweg wandert. Aus der Schmelze kristallisiert reines
Silicium als Einkristall aus. Etwaige Verunreinigungen bleiben in der Schmelze zurück.
(Vergleiche das mit der Bildung eines Eisbergs, der ja schließlich aus reinem
Süßwasser besteht, aus salzhaltigem Meerwasser!) Hier gelten die Regeln der
Schmelzpunktserniedrigung. Auf diese Weise werden die Verunreinigungen in der
Schmelze zurückgehalten, sogar angereichert und im Verlaufe des Zonenschmelzens
nach hinten transportiert. Nach Erkalten wird dieses Stück abgesägt.
Durch mehrmaliges Durchlaufen dieses Verfahrens erhält man Reinheitsgrade um 10-12
Atomprozent.
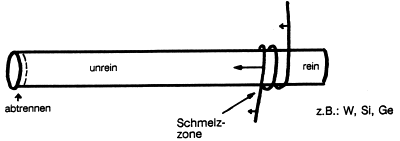
Zonenschmelzen
Diamant-Herstellung
Der Diamant ist eine eigentlich nur bei hohen Drucken und Temperaturen stabile
Kohlenstoffmodifikation. Glücklicherweise ist er aber metastabil.
Sonst würden sich die vielen Brillanten in Schmuck und Bohrköpfen rasch in Graphit
umwandeln! Vergleichbar damit ist die Bildung von unansehnlichem a-Zinn
aus glänzendem b-Zinn (-> Webseite).
Es gibt verschiedene Verfahren, um Industriediamanten herzustellen. Zunächst kann
man Graphit in Metallen lösen. Wenn diese sich bei ihrer Kristallisation
zusammenziehen, entstehen Drucke und Temperaturen, bei denen sich Graphit in
Diamant umwandelt. Auch Explosionstechniken zur Erzeugung von Schockwellen
sind im Gespräch.
Aufwachsverfahren
Bei diesem von van Akel und de Boer bereits 1924 entwickelten Verfahren geht es
um die Herstellung reinster, technisch hochwertiger Metalle durch Hitzezersetzung ihrer Iodide an
einem elektrisch beheizten Draht in einer geschlossenen Apparatur. Übrigens funktionieren auch deine
Niedervolt-Lampen und die in Autos verwendeten Halogenlampen
nach diesem Prinzip!
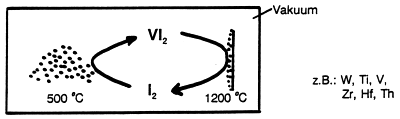
van Akel - de Boer-Verfahren
Rubinschmelze
Rubin, die rote Abart von farblosem Korund, enthält als färbendes Prinzip
0,1 - 0,7 % Chrom(III)-oxid, mit dem es leicht Mischkristalle bildet. Man erhält also
Kristalle, bei denen einige Al(III)-Ionen durch Cr(III)-Ionen ersetzt sind. Da die Rubine zu den
teuersten Edelsteinen gehören, hat man langezeit über deren Fälschung nachgedacht
und entsprechende Verfahren entwickelt. Die Fälscher dieser Rubine waren leicht mit
einer guten Lupe zu überführen: Ihre Kristalle waren einfach zu rein.
Man konnte jedoch nicht ahnen, dass eines Tages die Laser (engl. Light Amplification
by Stimulated Emission of Radiation) erfunden wurden. Der Bau dieser
monochromatischen Hochleistungs-Strahlungsquellen erforderte zu Beginn ihrer
Entwicklung genau das Material der Rubinfälschung: Große, hochreine, also
technische Rubin-Einkristalle.
Man stellt sie her, indem man die Mischung aus Aluminium- und Chromoxid durch eine
Knallgasflamme rieseln lässt.
Weitere Texte zum Thema „Kristalle“