
Die Bedeutung der UV-Absorption
durch Ozon für das Leben; Sonnenschutzmittel
Experimente:
Versuch: Wirkung von UV-Strahlen auf Lebewesen
Versuch: UV-Absorption von DNA und von Ozon im Vergleich
Versuch: Spektrum von Sonnenschutzmitteln und von Ozon im Vergleich
Der bemerkenswert hohe molare Extinktionskoeffizient
von Ozon von etwa 106 cm2 /mol [8] im
Absorptionsmaximum bei 254 nm macht verständlich, warum Ozon
auch in einer geringen atmosphärischen Konzentration für
unser Leben so wichtig ist.
Die Ozonschicht wirkt wie eine "UV-Schutzfolie",
die um die Erde herumgespannt ist und die Erde gegen die Strahlung
zwischen 220 nm und 300 nm abschirmt. Man kann das mit einer sehr
dünnen, 5 mm dicken schwarzen Folie vergleichen, die ja auch
schließlich (was niemand bezweifelt) kein sichtbares Licht
durchlässt.
Die UV-Strahlung wirkt vor allem
auf niedere Organismen (Bakterien, Einzeller) und wirkt dort als ein
starkes Mutagen (siehe Experimente, V 14). Aber auch auf die äußeren Organe von
Tier und Mensch wirkt UV-Strahlung ein. So werden ganz besonders
Haut und Augen angegriffen.
Interessant ist, dass Ozon und DNA nahezu die gleiche UV-Absorption zeigen (siehe Experimente, V 15; Bild 1). Das ist ein Hinweis auf die Bedeutung des Ozons für das Leben: Das Leben hat im Verlauf der Evolution offensichtlich seine zentral wirkenden DNA-Moleküle genau an den Bereich angepasst, in dem das Ozon die mutagene UV-Strahlung absorbiert. Dies lässt die möglichen Folgen der Ozonausdünnung für das Leben auf der Erde erahnen. (Im Bereich unterhalb von 220 nm übernehmen Sauerstoff, Stickstoff und Stickstoffoxide die Rolle des Ozons. Folglich steigt dort die Absorption der DNA deshalb wieder an.)

Bild 1: Vergleich von Ozon- und DNA-Spektrum [2]
Sonnenschutzpräparate decken
genau die vom Ozon nicht absorbierten UV-Spektralbereiche ab (siehe Experimente, V 16,
Bild 2).
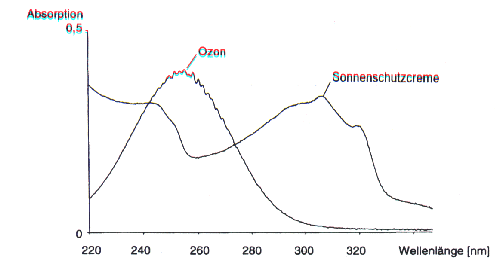
Bild 2: Spektren von Ozon und Sonnenschutzmitteln
Dieses Spektrum bedarf noch einer besonderen Erläuterung:
Sonnenschutzmittel sind aromatische Verbindungen wie etwa
Benzoesäurederivate, die im UV absorbieren. Sie tun das jedoch nicht gleichmäßig, sondern
weisen Absorptionslücken auf, bilden also "Fenster" für bestimmte UV-Strahlungsbereiche.
Der Grund: Aromatische Verbindungen besitzen im Allgemeinen drei getrennte Absorptionsgruppen.
Beim Benzol liegt je eine um 254 nm, 200 nm und >180 nm. Wenn man also Sonnenschutzmittel
konstruiert, muss man für das Füllen dieser Absorptionslücken sorgen. Deshalb müsste man eigentlich
geeignete Substanzen mischen.
Glücklicherweise hat das Ozon ebenfalls eine starke Bande im UV - wie das Spektrum zeigt.
Diese füllt bei den meisten Sonnenschutzmitteln die Lücke zwischen den Banden.
Problematisch wird es nur, wenn wie momentan der Ozongehalt der Stratosphäre abnimmt. Dann
öffnet sich dieses Fenster wieder. Durch Konzentrationserhöhung sorgt man für Bandenverbreiterung;
man kennzeichnet dann diese Mittel durch einen hohen Schutzfaktor.
Weitere Texte zum Thema „Ozon“