
Versuch: Chemolumineszenz bei der Oxidation von Pyrogallol
Lehrerversuch; 10 min.
Beim Experimentieren den Allgemeinen Warnhinweis unbedingt beachten.
Hinweis: Während der Selbsterhitzung der Flüssigkeit verdunstet ein Teil des unangenehm riechenden und giftigen Formaldehyds. Deswegen: Im Abzug arbeiten!
Geräte
Erlenmeyerkolben (500 ml), Reagenzgläser.
Chemikalien
Lösung 1: 1 g Pyrogallol in 10 ml destilliertem Wasser (Xn);
Lösung 2: 10 ml frische Formaldehyd-Lösung (w = 35-40 %) (T);
Lösung 3: 5 g Kaliumcarbonat in 10 ml destilliertem Wasser (Xn);
Lösung 4: 15 ml Wasserstoffperoxid (w = 30 %) (C, O).
Durchführung
Zunächst stellt man die vier Lösungen in Reagenzgläsern bereit. Man gießt die Pyrogallol-Lösung,
die Formaldehyd-Lösung und die Kaliumcarbonat-Lösung in dieser Reihenfolge in den Erlenmeyerkolben.
Dann wird völlig verdunkelt. Wenn sich das Auge einigermaßen an die Dunkelheit gewöhnt hat,
gießt man die Wasserstoffperoxid-Lösung auf einmal zu dem Flüssigkeitsgemisch im Erlenmeyerkolben,
wobei man das Ganze noch etwas umschüttelt.
Beobachtung
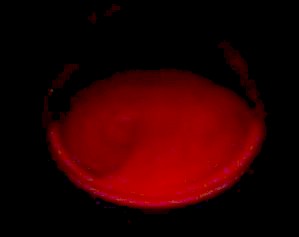
Sofort oder nach einigem Warten leuchtet die Flüssigkeit orangegelb bis rot auf, sie kocht und schäumt.
Nach einiger Zeit lässt das Leuchten nach und die Flüssigkeit kühlt sich langsam wieder auf Zimmertemperatur ab.


Chemolumineszenz bei der Oxidation von Pyrogallol durch Wasserstoffperoxid im Hellen und im Dunkeln
(Fotos: Helene)