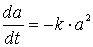
Herleitung des Konzentrations/Zeit-Gesetzes für 2 A -> B
Das Geschwindigkeitsgesetz für diese Reaktion 2. Ordnung ist
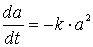
Umstellung zur Variablentrennung
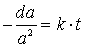
Integration
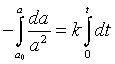
Ergebnis der unbestimmten Integration
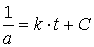
Durch Einsetzen der Integrationsgrenzen erhält man eine Form des Konzentrations/Zeit-Gesetzes für den Abbau von A
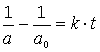
Trägt man 1/a gegen t auf, so erhält man eine steigende Gerade. Die Steigung ist k, der Ordinatenabschnitt 1/ao.
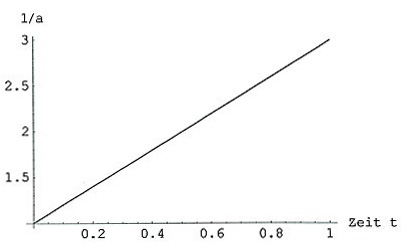
Mit dieser Linearisierung kann man zugleich nachprüfen, ob die Reaktion tatsächlich dem Typ 2 A -> B folgt.
Umstellung der Gleichung
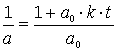
Kehrwertbildung führt zum endgültigen
Konzentrations/Zeit-Gesetz für
das Edukt A
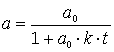
Dieses Gesetz gestattet, beim jeweiligen Zeitpunkt die verbleibende Konzentration von A zu berechnen.
Kontrollrechnungen
| t = 0 | a = a0 |
| t —> Ą | a —> 0 |
Trägt man a gegen t auf, so erhält man keine e-Funktion, sondern eine verschobene, rechtwinklige Hyperbel.
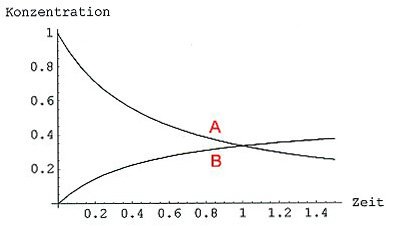
Konzentrations/Zeit-Kurven der Reaktion 2 A —> B
Zur Herleitung des Konzentrations/Zeit-Gesetzes für die Bildung des Produkts ist die
Konzentrations-Randbedingung für die jeweilige Zeit
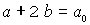
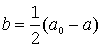
(a ist der zur Zeit t verbliebene Rest von A)
oder
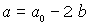
Einsetzen in das Konzentrations/Zeit-Gesetz des Edukts A
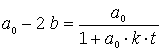
Umstellen ergibt das gesuchte
Konzentrations/Zeit-Gesetz für die Bildung des Produkts
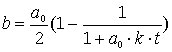
Dieses Gesetz gestattet, beim jeweiligen Zeitpunkt die Konzentration von entstandenem B zu berechnen.
Kontrollrechnungen
| t = 0 | b = 0 |
| t —> Ą | b —> a0/2 |
Trägt man b gegen t auf, so erhält man eine Sättigungskurve (siehe Bild oben).
Berechnung der Halbwertszeit
Bedingung a = ao /2 einsetzen in Konzentrations/Zeit-Gesetz für A und durch ao teilen
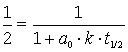
Kehrwert bilden und umstellen
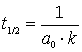
Die Halbwertszeit ist abhängig von der Anfangskonzentration des Stoffs A. Zum Lernen ist am besten die folgende Gleichung geeignet.
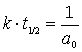
Weitere Texte zum Thema „Reaktionskinetik“