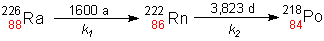
Stationäre Zustände: Beispiel radioaktives Gleichgewicht
Folgereaktionen entwickeln stationäre Zustände. Ein wichtiges Beispiel ist der radioaktive Zerfall, der durch physikalische Folgereaktionen gekennzeichnet ist. So wandeln sich in typischen Zerfallsreihen Uran-238 in Blei-206, Uran-235 in Blei-207 und Thorium-232 in Blei-208 um.
Wenn eine abreagierende oder zerfallende Substanz in einer Kette von Folgereaktionen ständig nachgeliefert wird oder die erste Substanz (wie das Uran-235) einer Zerfallsreihe sehr langsam zerfällt, resultiert daraus die Einstellung eines stationären Zustands, das Radioaktive Gleichgewicht.
Nehmen wir das Beispiel Radium-226, ein Zerfallsprodukt aus der Uran-Reihe. Das Radium-226 geht unter Emission von a-Teilchen in Radon-222 über. Letzteres bildet unter a-Zerfall Polonium-218.
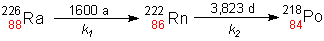
Die Zerfallskonstanten lassen sich aus den Halbwertszeiten berechnen.
Gehen wir von einer bestimmten Menge Radium aus. Es wird zunächst Radon entstehen. Die Geschwindigkeitsgleichung für die Bildung von Radon ist
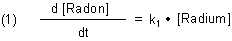
(Das Symbol [Radon] bedeutet die zur Zeit t vorliegende Atomzahl von Radon.)
Radon zerfällt seinerseits zu Polonium; die Geschwindigkeitsgleichung für den Zerfall von Radon ist
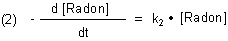
Zu Beginn steigt die Radon-Menge zwar an. Aber bald macht sich der Zerfall zu Polonium bemerkbar. Damit nähern wir uns einem stationären Zustand an, in dem gleich viel Radon-Atome gebildet werden wie zerfallen. Die Geschwindigkeiten (1) und (2) sind gleich groß. Daraus folgt:
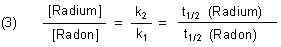
Die im radioaktiven Gleichgewicht befindlichen Atommengen radioaktiver Elemente verhalten sich wie ihre Halbwertszeiten (bzw. reziproken Zerfallskonstanten).
Beim Radium/Radon-Paar ist das radioaktive Gleichgewicht dann gegeben, wenn das Verhältnis
ist. Das heißt aber auch: Im radioaktiven Gleichgewicht kommt auf 153 000 Radium-Atome 1 Radon-Atom.
Diese Beziehungen reichen auch über verschiedene Elemente einer Zerfallsreihe. Der Grund: Zerfällt die Substanz A nur langsam, die daraus gebildete Substanz B unter Entstehung von C jedoch schnell, kann sich C trotzdem nur in dem Maße bilden, wie A zerfällt.
Das radioaktive Gleichgewicht gestattet es, aus den heutigen Konzentrationen eines betreffenden Isotops des Endprodukts Blei die verstrichene Zeit seiner Bildung aus vorhergehenden Isotopen zu berechnen (Methode zur Altersbestimmung).
Zum Schluss sei an die Madame Marie Sklodowska-Curie und ihren Mann Pierre Curie erinnert, denen wir den Einblick in die Zusammenhänge zwischen Radium, Radon und Polonium verdanken. Sie erhielten 1903 zusammen mit H. A. Bequerel den Nobelpreis für Physik für ihre Untersuchungen zur Radioaktivität. (Die Bezeichnung stammt von den Curies.) Für die Entdeckung und Isolierung von Radium und Polonium erhielt Frau Curie 1911 nach dem Unfalltod ihres Mannes zusätzlich den Nobelpreis für Chemie.
Weitere Texte zum Thema „Reaktionskinetik“