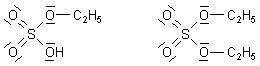
Schwefelsõureester
Schwefelsõureester bilden sich, wenn Schwefelsõure auf Alkohole einwirkt. Ihre allgemeine Formel ist R-O-SO3H. Da die Schwefelsõure ³ber zwei OH-Gruppen verf³gt, kann sie auch zwei Reihen Ester bilden:
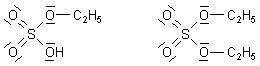
Man spricht bei den Estern auch von Sulfaten. Die Ester zwischen Ethanol und Schwefelsõure hei▀en Ethyl(hydrogen)sulfat bzw. Diethylsulfat. Der Monoester ist ein saures Sulfat und kann neutral reagierende Salze bilden.
Methyl- und Ethyl(di)sulfat gelten als Carcinogene bzw. Mutagene. Deshalb soll mit ihnen in der Schule nicht experimentiert werden. Da sie auch bei der klassischen, durch Schwefelsõure katalysierten Veresterungsreaktion gebildet werden, lohnt es sich, hierbei auf saure Ionenaustauscher als Protonenquelle zur³ckzugreifen (-> Webseite).
Schwefelsõureester bei der Herstellung von Ethen
oder von Diethylether
In der Schule ist die Herstellung von Ethen oder Ether aus Alkohol und Schwefelsõure bekannt.
Dabei bilden sich wahrscheinlich Schwefelsõureester als intermediõre Verbindungen. Daf³r spricht
Folgendes:
| - | Ethen entsteht, wenn man Schwefelsõure im ▄berschuss zugibt und auf 180 ░C erwõrmt. |
| - | Diethylether bildet sich, wenn man Ethanol im ▄berschuss zugibt und h÷chstens auf 140 ░C erwõrmt. |
Schwefelsõureester von langkettigen Fettsõurealkoholen sind wichtige
Tenside
So ist z. B. das SDS (Sodium- bzw. Natriumdodecylsulfat) ein wichtiges Reinigungsmittel.
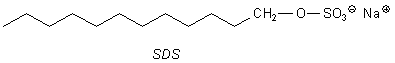
Man stellt es her, indem man den nachwachsenden Rohstoff
Palmitinsõure zum Alkohol reduziert und mit Sulfatierungsmitteln wie konzentrierter Schwefelsõure oder
Schwefeltrioxid umsetzt. Anschlie▀end wird mit Natronlauge neutralisiert.
Diese Ester-Salze reagieren in Wasser neutral. Sie bilden au▀erdem anders als normale Seifen-Anionen
mit Ca- und Magnesium-Ionen keine schwerl÷slichen Salze. SDS ist deshalb in Feinwaschmitteln wie z. B.
Fewa« enthalten. Mit ihm reinigt man auch gern empfindliche Laborgerõte - wie zum Beispiel Glaselektroden,
die man zu lange in fett- oder proteinhaltige L÷sungen getaucht hat.
Viele Naturstoffe sind Schwefelsõureester
Dazu geh÷ren die pflanzlichen Polysaccharide, zum Beispiel Carrageenane. Die bestehen
vor allem aus Galactoseresten und enthalten (wie auch viele andere, wasserbindende Polysaccharide) dar³ber
hinaus Sulfat- oder Carboxylatreste. Man nutzt sie in der Lebensmitteltechnologie als
Gelbildner.
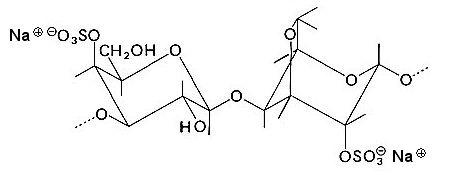
Struktureinheit von Carrageenan
Dar³ber hinaus gibt es noch mehr Substanzen: Schleimbildende Substanzen wie die Mucopolysaccharide,
zu denen letztlich auch das Chondroitinsulfat als wichtige knorpelbildende Substanz oder das
blutgerinnungshemmende Heparin (gebildet in Leber (lat. hepar; Leber) und in Leukozyten enthalten)
geh÷ren. Klicke hier und lies Frage 1475.
Die biochemische Sulfatierung erfolgt im Allgemeinen ausgehend von anorganischen Sulfat-Ionen ³ber das "aktive Sulfat", kurz PAPS.
Biochemische Schwefelsõure-Konjugate helfen beim Entgiften
Schwefelsõureester sind auch wichtig zur Ausscheidung von Fremdstoffen wie polykondensierte
aromatische Kohlenwasserstoffe (PAK). Hierbei koppelt das aktive Sulfat anstelle von Glucuronsõure oder
Glutathion (GSH) mit den enzymatisch intermediõr gebildeten hochcancerogenen PAK-Epoxiden.
Als polare Gruppen macht der resultierende saure Schwefelsõureester PAK-O-SO3H bzw. sein Anion
PAK-O-SO3- diese "Konjugate" wasserl÷slich und ausscheidbar. Vor allem werden auch Steroide
und Phenole auf diese Weise "entsorgt".
Weitere Texte zum Thema äSchwefelō