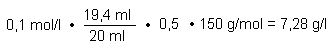Prof. Blumes Tipp des Monats Januar 2000 (Tipp-Nr. 31)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Zum ganz besonderen Jahreswechsel
Champagner und was sonst noch prickelt
 |
| Bild 1: Christel Blume und Wolfgang Below testen die Chemikalien für diesen Tipp des Monats (Foto: Daggi) |
Sekt und Champagner sind etwas, was du mit großen und kleinen Festen verbindest. Was wäre eine Prüfung ohne die Freunde, die nach mehr oder weniger gelungenem Abitur oder Staatsexamen vorm Prüfungszimmer stehen und die Korken knallen lassen? Studentische Verbindungsbrüder betonen, dass es sich nach Sektgenuss "ganz vorzöglich rölpsen" lässt. Dass du mit Sekt auch chemische Experimente machen kannst, daran wollen wir dich heute erinnern.
Was ist Sekt? Was sind seine Eigenschaften?
Unter Sekt, Champagner oder auch Schaumwein versteht man Weine, die zwei Gärungen
durchlaufen haben. Typisch ist ihr "Moussieren", d. h. das Entstehen von perlenden
Gasblasen.
Sektflaschen stehen unter einem sehr hohen Druck und gleichen kleinen Bomben. Wenn du eine
Sektflasche nicht zu langsam öffnest, kannst du Interessantes beobachten.
|
Versuch 1: Öffnen einer Sektflasche
|
Der Grund: Der Überdruck in der Flasche, der mehrere bar beträgt, wird auf den äußeren Luftdruck von einem bar entlastet. Das Flascheninnere kühlt sich ab und der bislang unsichtbare Wasserdampf kondensiert zu Nebel. (Lies hierzu die Webseite August 1999.)
Um was für ein Gas handelt es sich?
|
Versuch 2: Untersuchung des perlenden Gases
|
Es ist also Kohlenstoffdioxid. CO2 ist bekanntlich das Anhydrid der Kohlensäure. Wenn es aus dem Sekt entweicht, sollte sich der pH-Wert des Sekts in Richtung auf alkalisches Milieu verschieben. Das ist zumindest bei Sprudel der Fall.
|
Versuch 3: Verändert sich der pH-Wert von perlendem Sekt?
Ergebnis:
|
Dass sich der pH-Wert nicht gänzlich in Richtung auf das Bicarbonat-Gleichgewicht verschiebt, liegt daran, dass auch andere Säuren (besonders Weinsäure) im Sekt enthalten sind. Diese kannst du titrieren. Der Gehalt an Gesamtsäuren wird in der Literatur mit 7 bis 9 g/l angegeben. Was immer das auch bedeutet: Wir können ja mal so tun, als handele es sich nur um Weinsäure.
|
Versuch 4: Titration der Säuren im Sekt
Ergebnis:
(Der Faktor 0,5 berücksichtigt, dass die Weinsäure eine zweiprotonige Säure ist.) |
Unsere Maßanalyse ergibt, dass Sekt fast 0,1molar an titrierbaren Protonen ist. Eigentlich müsste der Sekt deshalb viel saurer schmecken. Die Protonen sind jedoch zum größten Teil fest an die Weinsäuremoleküle gebunden, da Weinsäure als schwache Säure bei einer Konzentration von 0,05 mol/l nur etwa zu 0,1 % dissoziiert ist. Außerdem werden die Protonen durch das Kohlensäuresystem abgepuffert. Deshalb sinkt der pH-Wert beim Perlen des Sekts. Anders ist es beim perlenden Sprudel, bei dem der pH-Wert mit dem Verlust von CO2 ansteigt.
Was wäre ein Sekt ohne Alkohol? Den weisen wir mit Hilfe der Komplexbildungsreaktion mit Cer(IV)-Ionen nach.
|
Versuch 5: Nachweis von Alkohol in Sekt
|
 |
| Bild 2: Ergebnis der Probe mit Cer-Ammonium-Reagenz
Glas 1: Sekt, Glas 2: Sekt + Reagenz, Glas 3: Vergleichsprobe mit Alkohollösung (Foto: Daggi) |
|
Versuch 6: Destillation von Sekt
|
Im Sekt lässt sich Zucker nachweisen. In Frage
kommen Glucose und Rohrzucker. Die Konzentrationen von Zucker variieren von nahezu zuckerfrei bis
zu süßen 100 g/l.
Ist die Konzentration äußerst gering, spricht man von ultra brut (franz. brut,
roh). Bis 20 g/l ist der Sekt brut, mit 20-30 g/l trocken/sec/dry. Ab
30 g/l spricht man von halbtrocken/demi sec/halfdry.
|
Versuch 7: Nachweis von Zuckern in Sekt
|
Mit dem restlichen Sekt stoßen wir auf die gelungenen Experimente an!
 |
| Bild 3: Wolfgang Below, Christel Blume,
Rüdiger Blume und Dagmar Wiechoczek
freuen sich über die gelungenen chemischen Experimente (Foto: Frank Schrewe) |
Wie stellt man überhaupt Sekt her?
Erfunden wurde die Technik um 1700 vom Mönch Dom Perignon, einem
französischen Kellermeister und Abteivorsteher (was früher oft dasselbe war...).
Zunächst wird der Wein einer üblichen alkoholischen Gärung
(Grundgärung) unterworfen. Lässt
man den Wein eine zweite Gärung durchlaufen, so kann man Schaumwein gewinnen.
Klassisch für die Zweitgärung ist die
Flaschengärung. Dazu mischt man alte und junge Weine aus
der Grundgärung und stellt diese Mischung durch Zugabe von in Wein gelöstem Rohr- oder
Rübenzucker auf 23 bis 26 g/l Zuckergehalt ein. Dem Wein aus der Grundgärung kann man
statt der Zuckerlösung auch Traubensaft zusetzen. Dann gibt man ein Löffelchen Hefe
hinzu und verschließt die Flaschen provisorisch. Bei dieser zweiten Gärung baut sich
ein hoher Druck (3 bis 6 bar) auf. Der Druck, der auf der Glaswand lastet, ist dem Reifendruck
eines Lkw vergleichbar! Deshalb müssen die Flaschen bekanntlich sehr starkwandig sein. Um
einer Explosion vorzubeugen, liegt die Gärungstemperatur bei 10 °C. Da arbeiten nur speziell
angepasste Hefen, und das auch nur sehr langsam. Deshalb dauern Zweitgärungen sehr
lange: 1 bis 5 Jahre. Außerdem müssen die Hefen gegen hohen Kohlenstoffdioxid-Druck
und hohe Alkoholgehalte resistent sein. Schließlich beträgt der Endalkohol-Gehalt 10,5
bis 12 Vol%!
Wie man die Hefe der Zweitgärung entfernt
Das Problem für die Flaschengärung ist, dass die Hefe nach
Gärungsende die Flüssigkeit trübt. Wie soll man aber die Hefereste entfernen, ohne
dass Kohlenstoffdioxid entweicht?
Die Schaumweinproduktion war deshalb erst möglich, nachdem man zum Entfernen der
Hefereste das Verfahren des Degorgierens entwickelt hatte (von
franz. degorger, reinigen, erbrechen). Hierzu werden die fertig gegorenen Flaschen nach
1 bis 3 Jahren zunächst so gestellt, dass ihre Mündung schräg nach unten
zeigt. Später werden sie dazu sogar noch
"gerüttelt". Damit meint man, dass die Flaschen einmal
täglich gedreht werden. Dadurch sammelt sich die Hefe am Verschluss an.
Zur Vermeidung von Verlusten an gelöstem CO2 werden die Flaschen zunächst tief
gekühlt. Dann kann man sie öffnen, ohne dass allzuviel Gas entweicht. Mit dem provisorischen
Verschluss entfernt man auch die Hefe. Oft friert man den Flaschenhals auch mit Hilfe einer
Kältemischung ein. Das sich bildende Eis enthält die Verunreinigungen; es wird samt
provisorischem Verschluss ausgeschleudert und abgeschlagen.
In beiden Fällen geht Flüssigkeit verloren. Das Auffüllen erfolgt durch sogenannten
Likör. Darunter versteht man eine Lösung von Kandiszucker in Wein,
der man ab und zu auch Cognac zusetzt. Mit diesem Likör kann man nicht nur auffüllen, sondern auch den Geschmack des Sekts
beeinflussen. Der Umfang der Zugabe ("Dosage", franz. la dose, Maß oder Dosis) richtet
sich nach Art des Sekts: Trockene Sekte enthalten wenig Likör, halbsüße und süße entsprechend mehr.
Schließlich werden die Flaschen mit Sekt noch bis auf einen Gasraum von etwa 15 ml aufgefüllt
und endgültig verkorkt. Man lässt die Flaschen noch einige Monate ruhen. Dabei baut sich erneut
Überdruck auf.
Ökonomischer kann man die Sektherstellung auch in großen Tanks aus Edelstahl ablaufen lassen (Tankgärung). Dann ist auch die Abtrennung der Hefe kein Problem: Es wird filtriert und adsorbiert. Wenn dabei Kohlenstoffdioxid verloren geht, presst man zur Not das Gas sogar noch maschinell hinein.
Und wie füllt man diesen Sekt in die Flaschen ab? Durch eine sinnvolle Konstruktion
setzt man zunächst eine Abfüllanlage für CO2 auf die Flasche (oder auf
mehrere zugleich). Die Flasche und das Füllsystem stehen dann unter dem Druck der
Sektherstellungsanlage. Dann öffnet man das Ventil für den Sekt; er fällt
regelrecht in die mit CO2 gefüllte Flasche hinein. Die Anlage gestattet
auch die gleichzeitige Einpressung des Sektkorkens, dessen Rausknallen wir so lieben. Der
Korken wird mit einer Zwinge zusammengepresst, bis er in den Flaschenhals passt. Das ist
alles nur eine Frage der Kraft der Maschine... (Versuche es mal selber! Lasse außerdem einen
frischen Sektkorken einige Tage liegen. Dann bekommt er seine ursprüngliche dicke Form
zurück.)
Natürlich werden vor allem für billigere Sektarten auch Korken aus Kunststoff
benutzt. Die sind meistens aus Polyethen (PE) gefertigt. Damit kannst du einen hübschen
Party-Versuch machen:
|
Versuch 8: Der brummende Sektkorken Schülerversuch; 10 min. Anmerkung
Geräte
Chemikalien und Material
Durchführung
|
| Klick mich an! |
 |
| Bild 4: Brennender Sektkorken |
Bleibt noch die Frage, wie schnell so ein Sektkorken fliegt. Messungen ergaben 40 km/h.
Einem solchen Geschoss kann man nicht ausweichen - Grund genug für viele Verletzungen beim
unachtsamen Öffnen von Sektflaschen.
Anmerkungen zum Moussieren
8000-12000 Bläschen steigen innerhalb der ersten Stunde aus einem Sektglas. Das
anhaltende Perlen ist nicht verwunderlich: Schließlich enthält eine Flasche Champagner
bis zu 4 Liter Kohlensäure. Diesem Moussieren wendet man besondere Aufmerksamkeit zu. Denn
die CO2-Gasperlen wirken spezifisch auf Rezeptoren im Mund und erzeugen das bekannte
prickelnd-wohlige Gefühl beim Schlürfen von Champagner. (CO2 ist ein
Gewebshormon mit starker physiologischer Wirkung, die durch den im Sekt enthaltenen Alkohol noch
verstärkt wird.)
 |
| Bild 5 (Foto: Daggi) |
Ohne Moussierpunkt geht in einem Champagnerglas nicht viel. Darunter versteht man eine raue
Stelle am tiefsten Punkt des Glases. Denn Glasrauheiten fördern das Entstehen von
Gasbläschen.
Moussierpunkte gibt es auch in Biergläsern, wie das folgende Bild zeigt.

Bild 6: Moussierpunkt bei einem Bierglas (Foto: Blume)
Hierzu haben wir einen Film (2,3 MB)
Klicke hier
Doch zurück zum Champagner: Das Behandeln von Sektgläsern mit Geschirrspülmitteln stört das Moussieren
erfahrungsgemäß sehr und ist deshalb Kennern ein Gräuel.
Stoffe, die durch die Hefe im Verlaufe der Zweitgärung in den Sekt gelangen,
fördern das Moussieren. Dazu gehören Peptide und Nucleinsäuren. Aber auch
Polysaccharide, Lipide und Fettsäuren sind für starkes Perlen förderlich. Grund
ist, dass sie sich wie Schutzhüllen um die Sektbläschen legen und sie vor zu
schnellem Platzen oder Auflösen schützen.
In diesem Zusammenhang wird immer gefragt: Nützt es etwas, wenn man in eine geöffnete Sektflasche einen Löffelstiel hängt, um den Sekt kühl zu halten und um das Moussieren zu stoppen? Sorgfältige Untersuchungen von mit großer Ausdauer gesegneten Forschern haben ergeben, dass das nicht der Fall ist. Kühlstellen und Verschließen mit einem geeigneten Korken oder Verschluss dagegen führt zu einem Druckaufbau in der Flasche und damit zum Stoppen des Moussierens. Dies ist eine Anwendung des Gesetzes von Le Chatelier auf das für Sekt grundlegende Lösungsgleichgewicht von CO2 in Wasser:
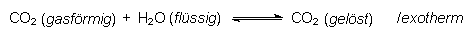
Dieses Gleichgewicht verschiebt sich mit steigendem Druck und unter Kühlung nach rechts. Umgekehrt kühlt die Lösung ab, wenn Gas austritt. Denn der Vorgang ist endotherm. Außerdem ist wie bei allen endothermen Vorgängen die Aktivierungsenergie besonders hoch. Das schränkt insgesamt weiteres Ausgasen ein; deshalb kann man Sekt überhaupt offen stehen lassen.
Was ist der Unterschied zwischen Sekt und Champagner?
Die Bezeichnung Champagner darf seit 1919
ausschließlich für Schaumweine aus der Region Champagne (genau Champagne-Ardenne,
Hauptstadt Reims) benutzt werden. Diese Schaumweine werden nur aus den Rebsorten wie Pinot
noir, Pinot gris, Meunier noir und Chardonnay erzeugt. Für die einzelnen
Champagnerarten ist die jeweilige Mischung von Mosten verschiedener Weinsorten charakteristisch.
Man bezeichnet die Resultate dieser Mischungen als Cuvée
(franz. cuver, in der Kufe gären).
Das Wort Sekt dagegen kommt vom lat. siccum,
trocken und bezeichnete ursprünglich einen trockenen Wein. Heute steht der Name für
alle Schaumweine, die nicht Champagner genannt werden dürfen. In Italien heißt der
Sekt Asti spumante (ital. spumare, schäumen). Asti ist
eine italienische Stadt und zugleich die Bezeichnung für die dort gepflegte Rebensorte.
Übrigens gibt es noch die Perlweine. Das sind
moussierende Weine mit geringem Rest-Zuckergehalt, die durch Gärung in Tanks unter Druck
hergestellt werden, aber keine Zweitgärung durchmachen. Dazu dürfte auch der
Prosecco gehören. (Hierunter versteht man trockene
Perlweine aus Venetien.) Sie dürfen nicht mit Sekt
oder Champagner verwechselt werden und müssen entsprechend deutliche Kennzeichnungen
tragen.
Lebensretter Sekt
Kein Witz: Man nutzt die belebende Wirkung von Sekt, um akut am Kreislaufversagen
Erkrankten zu helfen. Nur das CO2 muss man vorher größtenteils
herauskochen. Das ist vor allem bei einem Herzinfarkt besonders wichtig. Aber auch stillenden
Müttern empfiehlt man den Genuss von Sekt zur besseren Milchbildung. Dann rülpsen
Mutter und Kind im Chor.
Rüdiger Blume
Literatur:
[1] Römpp Chemie-Lexikon: Lebensmittelchemie, Thieme-Verlag, Stuttgart - New York.
[2] Ullmanns Enzyklopädie der technischen Chemie, Verlag Chemie, Weinheim.
[3] DER SPIEGEL 4/1991, S. 195
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 20. Dezember 2011, Dagmar Wiechoczek