Prof. Blumes Tipp des Monats Dezember 2007 (Tipp-Nr. 126)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Urotropin – Das besondere Kalottenmodell für kubische Systeme
Was hat das Thema „Kalottenmodell“ mit Weihnachten zu tun? Nun, Sie könnten sich ja zum Beispiel von der Schulpflegschaft einen Baukasten mit Kalotten schenken lassen. Die sind nämlich ziemlich teuer und deshalb nicht in allen Schulen zu finden. Oder vielleicht muss Ihr Baukasten ja mal wieder dringend ergänzt werden, denn bei häufigem Gebrauch nehmen die Kalotten unvermeidlich Schaden.
Aber zurück zum Thema: In letzter Zeit wurden mir immer wieder Fragen zu Kalottenmodellen gestellt. Offenbar befassen sich doch einige Leute damit. Zur Übung (Typ „King Size“) bauen wir doch einmal das Modell der Verbindung Urotropin. Über diese wichtige Substanz, ihre Synthese und Verwendung sowie über die Herkunft ihres Namens haben wir schon berichtet. Heute geht es ausschließlich um die Frage ihrer Struktur.
Wie ist das Molekül aufgebaut?
Die gängige chemische Bezeichnung Hexamethylentetramin sagt schon einiges über
die Struktur des Moleküls aus: Es muss danach aus sechs zweibindigen Methylengruppen,
also CH2-Gruppen (griech. héxa, sechs) bestehen, die durch vier
dreibindige Stickstoffatome verknüpft sind (griech. tétra, vier).
Man findet in der Literatur viele Möglichkeiten, dieses Molekül darzustellen. Hier ist die schlichteste Form.
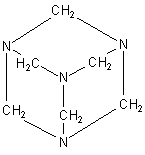
Die folgende verkürzte und angedeutet räumliche Darstellung geht schon etwas genauer auf die Bindungen und Bindungswinkel ein.
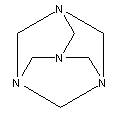
Am ehesten lässt die folgende Darstellung einen Einblick in die Struktur zu:
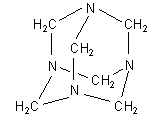
Verkürzt sieht das so aus:
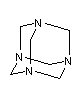
Irgendwie befriedigen einen diese Darstellungen aber nicht so richtig. Deshalb wollen wir heute ein räumliches Modell davon bauen.
Das Kugel-Stab-Modell von Urotropin
Zunächst kann man auf einen Kugel-Stab-Baukasten wie etwa von CVK (Cornelsen) zurückgreifen.
Das Bauen ist damit relativ einfach.

Bild 1 (Foto: Blume)
Aus Übersichtsgründen haben wir auf den Einbau der H-Atome verzichtet. Aber trotzdem sieht alles etwas „spirrelig“ aus.
Das Kalottenmodell von Urotropin
Am schönsten aber sind die Kalottenmodelle. Nur sie geben Aufschluss über die richtigen
Bindungsverhältnisse, denn die Kalotten (Kugelabschnitte) sind so geformt, dass sie aneinandergefügt
die richtigen Bindungslängen bzw. Kernabstände sowie Bindungswinkel zeigen.
Das Bauen gerade des Urotropinmodells ist aber ein bisschen kniffelig.
| - | Vor Beginn der Arbeit empfiehlt es sich, zuvor ein Modell zu zeichnen. |
| - | Wichtig ist dann Folgendes: Es gibt verschieden große Kalotten für dreifach gebundene Stickstoffatome! Bleiben Sie bei einer Sorte, und zwar bei der mit der dicksten Kalottenform. Sonst können Sie das Modell nicht zusammensetzen. |
| - | Nun geht es beim Zusammensetzen ziemlich eng zu… |
| - | Ein Problem taucht bald auf: Es sind aufgrund der vielen C-N-Bindungen an den C- und N-Kalotten nicht genügend Bindungsknöpfe, die die Kalotten zusammenhalten, vorhanden, so dass man auf Hilfsmittel wie doppelseitig beschichtetes Klebeband (wie z. B. Tesa-Powerstrips®) zurückgreifen muss. Zum Kleinschneiden der Strips sei Folgendes gesagt: Die Strips nicht vorher auspacken, sondern samt Umhüllung schneiden. |
Wenn wir alles richtig gemacht haben, erhalten wir ein knubbeliges Modell, das gut in eine große Männerhand passt.

Bild 2 (Foto: Blume)
Drehen wir es und betrachten es dabei genauer, so fallen uns die verschiedensten Symmetriebeziehungen auf.
Es scheint sich aber insgesamt um ein kubisches System zu
handeln. Das zeigen wir in den folgenden Abschnitten.
Die vier Stickstoffatome bilden ein Tetraeder
Die folgenden zwei Bilder zeigen das Tetraeder einmal von der Spitze her (links) und dann aus Sicht der dreieckigen
Bodenplatte (rechts).


Bild 3 (Fotos: Blume)
Diese Anblicke können wir jeweils vier Mal genießen – wenn wir das Modell entsprechend drehen. Achten Sie darauf,
wie symmetrisch die CH2-Gruppen stehen. Sie bilden miteinander immer einen Winkel von 120 °.
Die sechs Methylengruppen bilden ein Oktaeder
Wir müssen einen Körper finden, bei dem wir auf möglichst ideale Art und Weise sechs Ecken miteinander verbinden.
Diesen Körper kennen wir: Es ist das kubische Oktaeder. Es besteht aus acht (griech. octa, acht)
gleichseitigen Dreiecken, die als zentrale Bodenfläche ein Quadrat bilden. Auf dem folgenden Bild können wir das
Oktaeder von einer seiner Spitzen her betrachten.

Bild 4 (Foto: Blume)
Man erkennt auf dem Bild fünf CH2-Gruppen. Die vordere bildet die Spitze einer Oktaederhälfte, die
vier anderen bilden die quadratische Bodenfläche der Bipyramide, deren untere Spitze verdeckt ist. Auch diesen
Anblick können wir mehrmals genießen, wenn wir das Modell drehen – insgesamt sechs Mal.
Urotropin gehört zum kubischen System
Platon und Archimedes
hätten ihre Freude an der Struktur dieses Moleküls gehabt. Im folgenden Bild zeigen wir eine Skizze, wobei
wir die beiden geometrischen Körper - Tetraeder und Oktaeder - hervorheben.
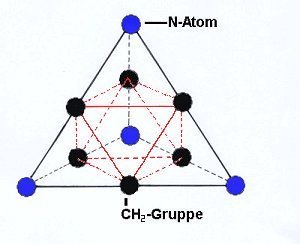
Ein Hinweis: Wir haben aus Übersichtsgründen darauf verzichtet, das Herausragen der CH2-Gruppen aus den Verbindungsachsen zwischen den N-Atomen zu berücksichtigen.
Wenn das aber auch noch mit einkalkuliert wird, erkennt man, dass das N-Tetraeder aufgrund der gewinkelten Bindungen zwischen den Atomen N-C-N vom CH2-Oktaeder durchdrungen wird. Durch die Bindungswinkelung liegt das CH2-Oktaeder nicht mehr im N-Tetraeder, sondern ragt mit seinen Spitzen über dessen Kanten hinaus.
Beim Urotropinmolekül handelt es sich um einen Durchdringungskörper eines Tetraeders mit einem Oktaeder.
Hier sehen wir dazu ein Modell. Das N-Tetraeder ist blau, das CH2-Oktaeder rot eingefärbt.


Bild 5 (Modell: Dirk Eisner; Foto: Blume)
Da man ein Tetraeder oder auch ein Oktaeder aus einem Würfel entwickeln kann, wird der Zusammenhang zum
kubischen System mehr als deutlich.
Nun darf man aber nicht meinen, dass solche kubischen Moleküle auch im kubischen Gitter kristallisieren. Urotropinkristalle gehören zum rhombischern Kristallsystem.
Für Spezialisten: Zur chemischen Nomenklatur des Urotropins
Die Nomenklatur gibt Aufschluss über einen anderen Aspekt der Verwandtschaft mit kubischen Systemen.
Die chemisch exakte Bezeichnung des Urotropins lautet
1,3,5,7-Tetra-aza-tri-cyclo[3.3.1.1,3.7]decan
Wir erkennen, dass Urotropin aus nomenklatorischen Zwecken letztlich von einem Kohlenwasserstoff abzuleiten ist. Dieser besteht aus 10 C-Atomen, ist also ein Decan (griech. déca, zehn). Es handelt sich um einen trizyklischen Kohlenwasserstoff, der aus drei miteinander verbundenen, sesselförmigen Sechseckringen besteht.
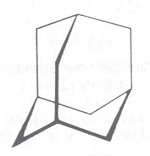
Diese Verbindung gibt es tatsächlich. Ihre chemische Bezeichnung ist
Tri-cyclo[3.3.1.1,3.7]decan
Die Nummern geben (für Laien auf etwas komplizierte Art und Weise) die Ansatzpunkte der Ringe an.
Die Struktur ist identisch mit einem Ausschnitt aus dem kubischen Kristallgitter des Diamanten. Diese Verbindung heißt deswegen auch Adamantan.
Beim Urotropin sind formal vier C-Atome (genau: CH-Gruppen) des Adamantans durch vier Stickstoffatome („aza“) ersetzt worden. Wegen der Verwandtschaft zum Adamantan findet man deshalb für Urotropin ab und zu auch die Bezeichnung
1,3,5,7-Tetra-aza-adamantan
Rüdiger Blume
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 10. Juni 2010, Dagmar Wiechoczek