3 Beschreibung einzelner Stoffklassen
3.1 Kohlenhydrate (Saccharide)
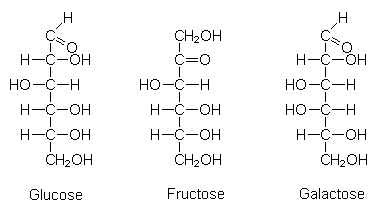
Die mengenmšŖig wichtigsten Kohlenhydrate bestehen aus den Elementen C, H, O im ungefšhren Massenverhšltnis 1:2:1. Glucose z. B. hat die Formel C6H12O6 (= "C6(H2O)6", daher die Bezeichnung Kohlenhydrate). Chemisch gehŲren die einfachen Kohlenhydrate (Zucker) zu den Aldehyden bzw. Ketonen, die zusštzlich alkoholische OH-Gruppen tragen. Bei den fŁr uns wichtigsten Monosacchariden Glucose, Fructose und Galactose handelt es sich um isomere Verbindungen.

Zucker liegen in Ringform vor, so dass die Aldehydgruppe nicht mehr ohne weiteres zu erkennen ist (Halbacetalbildung). Durch den Ringschluss kommt noch eine zusštzliche MolekŁl-Symmetrie hinzu, die die chemischen und physikalischen Eigenschaften stark veršndern kann.
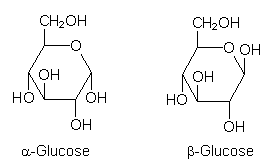
So entstehen aus a-Glucose die leicht verdaulichen und lŲslichen Nahrungsmittel Stšrke und Glykogen, aus b-Glucose die stofflich gšnzlich andere Cellulose, die als unlŲslicher, kaum quellfšhiger und unverdaulicher Ballaststoff geschštzt wird.
Man unterscheidet:
| - | einfache Zucker (Monosaccharide wie Glucose, Fructose, Galactose, Ribose, Desoxyribose), |
| - | Oligosaccharide (Disaccharide wie Rohrzucker (Saccharose), Malzzucker (Maltose) und Milchzucker (Lactose); -> Abb. 6), |
| - | Polysaccharide (Stšrke bzw. Glykogen, Cellulose und Inulin). |
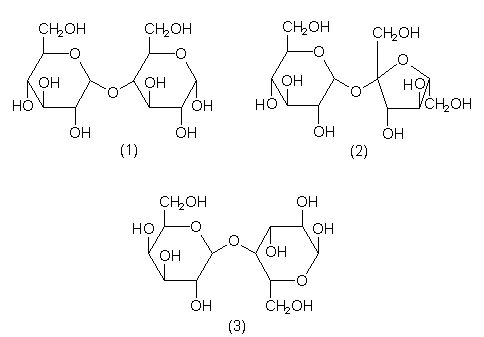
Abb. 6: Formeln von Maltose (1), Rohrzucker (2), Lactose (3)
Oligo- und Polysaccharide entstehen aus den monomeren, d. h. den einfachen Zuckern, durch Bildung von SauerstoffbrŁcken unter Abgabe von Wasser. Dieser Reaktionstyp heiŖt Kondensation.
a-Glucose + b-Glucose ———>
Maltose + H2O
a-Glucose + b-Fructose ———>
Saccharose + H2O
b-Galactose + a-Glucose ———>
Lactose + H2O
n a-Glucose ———>
Stšrke bzw. Glykogen + n H2O
n b-Glucose ———>
Cellulose + n H2O
n b-Fructose ———>
Inulin + n H2O
Stšrke besteht aus zwei Formen, dem lŲslichen Anteil (Amylose) und dem kaum lŲslichen Amylopektin. Letztere kann besonders gut Wasser einlagern, da sie neben linear verknŁpften GlucosemolekŁlen auch Quervernetzungen aufweist (Verwendung als Kleister). Das in tierischem und Pilzgewebe auftretende Glykogen ist eine noch stšrker verzweigte Form der Stšrke.
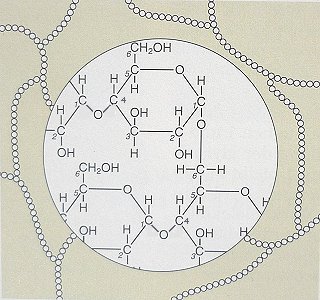
Abb. 7: (Quelle: Cornelsen)
Oligo- sowie Polysaccharide kŲnnen durch Erwšrmen in verdŁnnten Mineralsšuren wie Phosphor- oder Salzsšure in ihre Monomeren zerlegt werden. Dies spielt beim Verfahren der Holzverzuckerung zur Gewinnung von Glucose eine groŖe Rolle. Eleganter ist die Spaltung der Stšrke durch Enzyme. Diese "Amylasen" sind nicht nur im Speichel oder Darmsaft, sondern auch in keimender Gerste enthalten (Mšlzvorgang bei der Alkoholgewinnung aus Stšrke).
Aus Kohlenhydraten werden technisch und biotechnisch viele Folgeprodukte gewonnen. Diese sind z. B.:
| - | Alkohole: Ethanol, Zuckeralkohole wie Sorbit und Xylit, |
| - | Abbauprodukte der Stšrke wie Dextrine, |
| - | Glucose, |
| - | Vitamin C (Ascorbinsšure), |
| - | nichtionische Tenside, die besonders hautschonend sind und in GeschirrspŁlern verwendet werden, |
| - | essbare Folien auf Stšrkebasis mit Glycerin als Weichmacher, |
| - | Kunststoffe, die elektrisch leiten (Polypyrrol), |
| - | Cellulosederivate wie CM-Cellulose als Lebensmittelzusštze (-> 6.5.2). |
3.2 Fette und fette ÷le, Lipide
3.2.1 Chemische Eigenschaften
Fette sind Ester aus mehr oder weniger langen Fettsšuren und Glycerin (Glyceride):

Die RŁckreaktion ist die Fettspaltung (Verseifung). Diese Hydrolyse erfolgt entweder enzymatisch durch Lipasen oder technisch mit basischen Verbindungen wie Natronlauge bzw. Kalilauge. Es bilden sich die Salze der Fettsšuren, die Seifen.
Fettsšuren sind lšngerkettige Carbonsšuren. NatŁrliche Fettsšuren enthalten stets eine gerade Anzahl von C-Atomen, da sie schrittweise aus dem C2-KŲrper Essigsšure synthetisiert werden (-> 4.2.2). Die bekanntesten gesšttigten Fettsšuren sind:
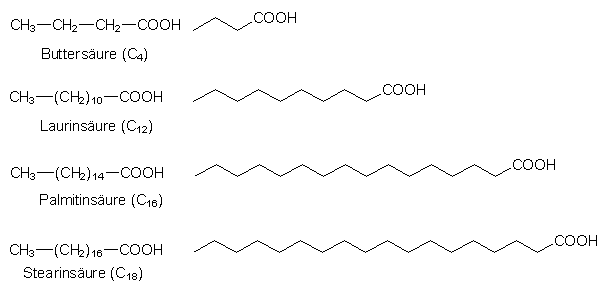
Die kŁrzeren Fettsšuren riechen ausgesprochen schlecht (Geruch nach ranziger Butter, SchweiŖ, Ziegenkšse oder Baldrian).
Besonders wichtig fŁr die Ernšhrung sind die ungesšttigten Fettsšuren:
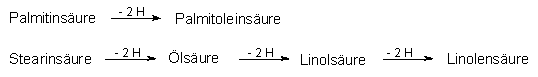
Der menschliche Stoffwechsel kann nur zwei Doppelbindungen einfŁhren, so dass die Linolensšure bereits essentieller Nahrungsbestandteil ist ("Vitamin F"). Ungesšttigte Fettsšuren sind Bestandteile von Biomembranen und auch Ausgangsverbindungen von Hormonen wie den Prostaglandinen.
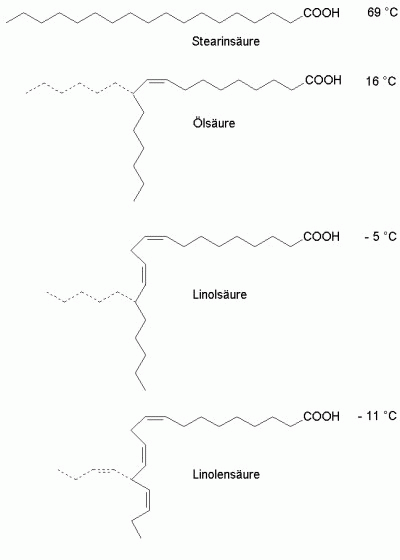
Abb. 8: Die ÷lsšurereihe und deren Schmelzpunkte
Wšhrend gesšttigte Fettsšuren bei Zimmertemperatur fest sind, sind die ungesšttigten flŁssig. ńhnliches gilt fŁr die aus ihnen aufgebauten Fette bzw. fetten ÷le. Grund hierfŁr ist das unterschiedliche KristallbildungsvermŲgen. Die linearen gesšttigten MolekŁle kŲnnen paraffinartige Kristalle bilden, haben also einen hohen Schmelzpunkt, wšhrend die mehr knšuelfŲrmigen, hochungesšttigten Fettsšuren erst bei wesentlich tieferen Temperaturen auskristallisieren kŲnnen (-> Abb. 8).
Ungesšttigte Fettsšuren findet man vor allem in PflanzenŲlen. Durch zŁchterische MaŖnahmen kann man deren Fettsšurespektrum beeinflussen (z. B. von Sonnenblumen, Sojabohnen und Euphorbia lathyris). Dies spielt vor allem bei der Gewinnung nachwachsender Rohstoffe eine groŖe Rolle.
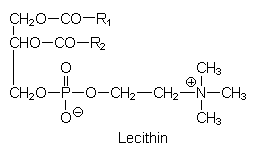
Fette sind extrem hydrophob. Zum Vermischen mit Wasser, d. h. zum ‹berwinden der Phasengrenze, benŲtigt man grenzflšchenaktive Stoffe als LŲsungsvermittler, mit deren Hilfe zumindest Emulsionen hergestellt und stabilisiert werden kŲnnen. Diese Tenside oder Detergentien verfŁgen im Allgemeinen Łber ein lipophiles und ein hydrophiles Ende:
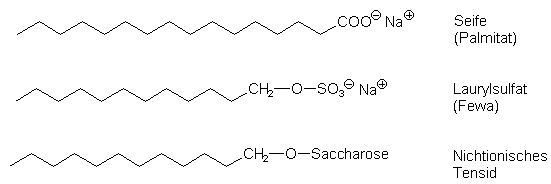
Lecithin ist ein natŁrliches Tensid. Es befindet sich in Membranen und in natŁrlichen Emulsionen wie dem Eidotter. Es ist auŖerdem ein wichtiger Phosphatspeicher fŁr die Zellen.
Fette und Fettsšuren sind wichtige nachwachsende Rohstoffe. Reste von Fetten und fetten ÷len, die nicht durch Auspressen, sondern wie Talg durch Ausschmelzen oder durch HerauslŲsen von letzten Resten nach dem Auspressen mit Benzin oder CKW gewonnen werden, werden hier verbraucht. Diese dienen anstelle petrostšmmiger Edukte vor allem zur Gewinnung von Massenchemikalien. Man synthetisiert aus ihnen Tenside, Kunststoffe und Lackrohstoffe.
3.2.2 Fettgewinnung
Fette und fette ÷le gewinnt man durch verschiedene Verfahren, die unterschiedlich wertvolle Substanzen liefern:
Ausschmelzen
Dieses vor allem bei tierischem Material angewendete Verfahren
fŁhrt wegen hoher Temperaturen zu Verlusten an ungesšttigten
Fettsšuren. Schmalz und Talg sind deshalb ernšhrungsphysiologisch
von geringer Bedeutung. Talg ist aber im Millionen-Tonnen-MaŖstab Rohstoff fŁr
die chemisch-industrielle Tensidgewinnung.
Auspressen
Kaltes Auspressen von (vor allem pflanzlichen) ÷len ist das
schonendste Verfahren zur Gewinnung ungesšttigter Fettsšuren. Da
hierbei nicht das gesamte ÷l erhalten wird, rŲstet man das Material
(z. B. Sojabohnen) vor dem Pressen zur ZerstŲrung der Zellwšnde.
Extrahieren
Hierbei lŲst man das Fett aus dem zuvor gerŲsteten und damit
entwšsserten Material mit organischem LŲsemittel heraus. Heute
verwendet man dazu niedrig siedende LŲsemittel wie Hexan. FrŁher
nahm man hierzu CKW. Das LŲsemittel wird anschlieŖend im
Vakuum abgedampft.
3.2.3 Fetthšrtung
FlŁssige fette ÷le kŲnnen gehšrtet werden. Dies geschieht durch katalytische Hydrierung, d. h. durch Addition von Wasserstoff unter hohem Druck. Katalysator ist im Allgemeinen Nickelpulver:
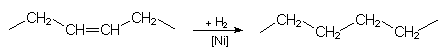
Spuren von NickelrŁckstšnden sind wegen der mŲglichen AuslŲsung von Allergien nicht unbedenklich.
3.2.4 Fettverderbnis
Fettverderbnis spielt in der Lebensmittelchemie eine groŖe Rolle:
| - | Beim Hocherhitzen von Fetten entsteht aus
Glycerin der ungesšttigte Aldehyd Acrolein. Dieser ist fŁr den
stechenden und Tršnenfluss auslŲsenden Geruch verantwortlich. Man findet diesen
Stoff Łbrigens auch in Autoabgasen oder Photosmog.
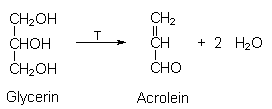 |
| - | Hydrolyse setzt die schlecht riechenden Fettsšuren frei. Sie wird durch Wasseranwesenheit und durch TemperaturerhŲhung gefŲrdert (Friteusenfett). Es bilden sich freie Fettsšuren, daher der ranzige Geruch. Der Nachweis erfolgt mit einem einfachen Sšure/-Base-Indikator, den man in das Fett bzw. eine LŲsung taucht. Die Konzentration wird titrimetrisch mit KOH bestimmt. Deren Verbrauch definiert die Fettsšurezahl. |
| - | Auch bei niedrigeren Temperaturen, wie bei -30 ºC in der KŁhltruhe, findet enzymatische Hydrolyse statt. |
| - | Ungesšttigte Fettsšuren bilden mit
Luftsauerstoff Peroxide:
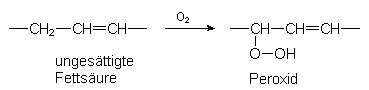 Peroxide zersetzen sich leicht beim Erhitzen, vor allem in Gegenwart von Metallen. Deshalb kann altes Fett sogar explodieren. Peroxide fŁhren weiterhin zur Quervernetzung zwischen den MolekŁlen (÷ltrocknung; -> Abb. 9). Dieser Vorgang wird durch Schwermetallsalze (Sikkative) gefŲrdert. Durch Erwšrmen von LeinŲl-Sikkativ-Gemischen, die man Łber Gewebe flieŖen lšsst, wird Linoleum hergestellt.
Abb. 9: Peroxide und Vernetzungsreaktion Peroxide kŲnnen aber auch gespalten werden. Dabei bilden sich u. a. Aldehyde, die zu Carbonsšuren weiter reagieren. 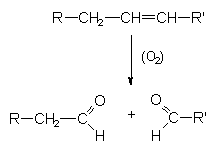 |
Fette reichern lipophile Stoffe an. Im Fettgewebe sammeln sich deshalb besonders viele flŁchtige und nichtflŁchtige CKW sowie andere LŲsemittelrŁckstšnde und Pestizide. Dies gilt auch fŁr Nahrungsmittel, die in der Nšhe von CKW-Emittenten wie chemischen Reinigungen gelagert werden. NatŁrliche Nahrungsfette enthalten aber auch die fettlŲslichen Vitamine wie A, D und E.