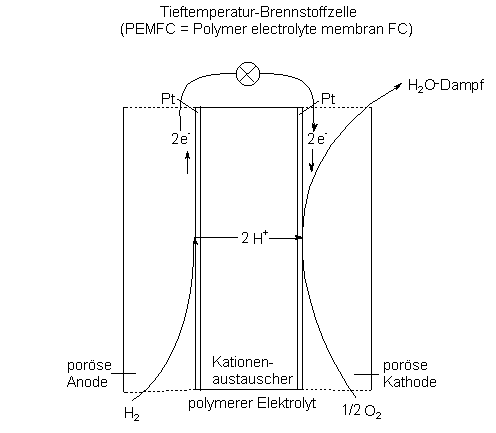
PEM-Brennstoffzelle
Polymermembran-Brennstoffzellen
Man bezeichnet diese Brennstoffzellen kurz mit PEM-FC
(abgek. engl. polymer electrolyte membrane fuel cells). Die Reaktionsr‰ume werden durch
eine Kationenaustauscher-Membran getrennt, die nur f¸r Protonen
durchl‰ssig ist. Die Membran spielt also die Rolle des Elektrolyten. Diese
Membranbrennstoffzellen werden vor allem in den Autos genutzt.
Als Membran verwendet man sulfonierte Fluorkohlenwasserstoffpolymere (teflonartig, bekannt
z. B. als Nafion(R)-Membran). Sie sind nur wenige zehntel
Millimeter dick.
Eine Untereinheit besteht aus
einer Membran, die beiderseitig mit Platin als Katalysator beschichtet ist. Auf
jeder Seite ist eine gasdurchl‰ssige Elektrode angebracht, die mit dem Platin Kontakt hat.

PEM-Brennstoffzelle
Auf der Anodenseite wird Wasserstoff eingeleitet. Dieser bekommt Kontakt mit dem Platin und gibt Elektronen an die Elektrode ab.
H2 ———> 2 H+ + 2 e-
Die dabei entstandenen Protonen wandern durch die Kationenaustauscher-Membran in Richtung Kathode. Die Elektronen wandern durch den ‰uşeren Stromleiter zum elektrischen Verbraucher und werden dann zur Kathode weitergereicht. Dort reduzieren sie den eingeleiteten Sauerstoff, der simultan samt Protonen zu Wasser reagiert:
Ω O2 + 2 e- + 2 H+ ———> H2O
Das Wasser wird mit der nicht verbrauchten Luft als Wasserdampf ausgestoşen. Dies wird durch die hohe Betriebstemperatur von 90 ∞C gefˆrdert.
Die Wirkungsgrade dieser Zellen liegen zwischen 50 und 80 %.
Nachteil ist, dass man zur Mitf¸hrung der Gase Sauerstoff und Wasserstoff im Auto eine
ausgefeilte K¸hl- und Druck-Technik entwickeln muss.
Statt mit Sauerstoff kann man aber mit Luft arbeiten. Dann ist allerdings ein hˆherer
Betriebsdruck (2 bis 5 bar) nˆtig, technisch kein Problem.
Statt mit Wasserstoff betreibt man die Brennstoffzellen-Aggregate mit Methanol oder Methan,
die leichter zu speichern sind. In diesen F‰llen m¸ssen diese Verbindungen aber erst zur
Bildung von Wasserstoff umgewandelt werden. Dazu werden berechnete Mengen des
Brennstoffs zusammen mit Wasser erhitzt und ¸ber einen Katalysator, den Reformer, geleitet.
CH3OH + H2O ———> CO2 + 3 H2
Neben Wasserstoff und CO2 entsteht auch CO, das den Katalysator der Brennstoffzelle, Platin, vergiftet. Deshalb muss das CO zuvor entfernt werden. Dies geschieht mit Hilfe von katalytischer Reduktion von CO zu Methanol, selektive CO-Oxidation oder Membrantrennverfahren, die f¸r Gasmischungen zunehmend entwickelt werden.
Weitere Texte zum Thema ÑAutoì