 |
 |
 |
 |
| Kurze Fragen - Kurze Antworten
Aus dem E-Mail-Korb von Professor Blume |
407
F: Im Chemieunterricht habe ich nie richtig verstanden, warum gerade
H+-Ionen den ätzenden Charakter einer Säure ausmachen. Im Unterricht haben wir immer nur gesagt,
dass es so ist, jedoch nie erklärt bekommen, wie diese Reaktionsfreudigkeit bei diesem Ion zu stande kommt.
Dennoch würde ich gern etwas mehr über die Hintergründe dieses Phänomens wissen.
A: Gemeinsame Stoffeigenschaft aller Säuren: Sie setzen alle Protonen
frei. Unedle Metalle werden zum Beispiel durch Protonen zersetzt, wobei brennbarer Wasserstoff entsteht. Das
ist ein Redoxvorgang, bei dem Protonen das Metall oxidieren, z. B.
Mg + 2 H+ ———> Mg2+ + H2 + Energie
Auf Protonen beruhen auch andere Wirkungen der Säuren, so der saure Geschmack, die Wirkung auf Eiweiß
(Gerinnung), die Zerstörung von Kohlehydraten und Fetten (durch Salzsäure). Hinzu kommen auch viele
katalytische Wirkungen, wie Zersetzung von Stärke und Cellulose zu Zucker. Hier wirkt sich vor allem
die Eigenschaft der Protonen aus, besonders kleine, positive Ladungsträger („Punktladungen“) zu sein.
Damit können sie Bindungen polarisieren und letztlich beim Aufbrechen mitwirken.
Darüber hinaus sind spezielle, individuelle Stoffeigenschaften von einzelnen Säuren zu betrachten. Die
sind anders begründet. Schwefelsäure zersetzt alles Organische, weil es Wasser aus dem Gewebe und aus den
Molekülen reißt. Salpetersäure ätzt, weil sie stark oxidierend wirkt, und färbt die Haut gelb, da sie mit
Eiweiß der Haut reagiert. Flusssäure greift als einzige Säure sogar Glas an!
408
F: Nachdem sich Metalle in Säuren auflösen und Salz sowie wasserstoff
bilden, habe ich als Nichtmetall S in Natronlauge gelegt. Es hat sich aufgelöst. Beim Eindampfen bildete sich
danach eine gelbe und eine weisse Phase.
A: Schwefel reagiert mit löslichen Alkalien unter Bildung von
gelblichen Polysulfiden und farblosen Verbindungen wie Thiosulfat. Beim Eindampfen (oder auch beim Ansäuern)
kann sich daraus wieder gelber Schwefel bilden. Der weiße Rückstand kann aus festem NaOH, Na-Oxid oder
Natriumsulfat (usw.) bestehen.
409
F: Ich und ein freund haten letztens eine Diskusion über Aggregatszustände,
und wir waren am Überlegen, was das Gegenteil von einer Sublimation (Fest-->Gas) ist.
A: Das Gegenteil von Sublimieren heißt Resublimieren (gasförmig -> fest).
So kann Eis direkt aus Wasserdampf gebildet werden; das kennst du als Raureif. Oder vielleicht vom Ioddampf,
der Kristalle bildet. Lasse dir das vom Lehrer zeigen.
410
F: hallo, wollte wissen woraus tränengas besteht? wer es erfunden hat?
kann man es unschädlich machen dürch chemiesche versuche?
A: Es handelt sich um bromiertes Aceton oder um Chloracetophenon
(letzteres ist das CN-Gas). Wer es erfunden hat, weiß ich nicht. Man kann es durch Kochen in Natronlauge
unschädlich machen.
F: hallo!! danke für ihre antwort! ich wollte wissen aus was cs
gas besteht! kann ich es selber in der schule herstellen? was brauche ich dafür? wie kann ich es unschädlich
machen? welche neue stoffe werden dabei hergestellt? Danke!
A: CS ist ortho-Chlorbenzylidenmalodinitril.
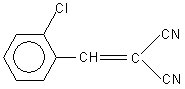
CS-Gas
In der Schule darfst du es (wie auch die anderen Tränengase) nicht herstellen. Beim Zersetzen mit NaOH entsteht (unter anderem) das entsprechende Phenol sowie die Malonsäure (als Salz). Weshalb fragst du das alles?
F: hallo, wir beschäffigen uns mit tränengase (cs gas)! ich bin
in der 11. klasse! wir haben bald eine projektwoche in der ich mit drei weitern schulern es vorstellen
wollen! und habe einige informationen gebraucht! wir wollen jetzt selber ein spray herstellen! und zwar
von zwiebeln! mit zwiebeln kann man auch leute zum tränen bringen und das haben wir jetzt auch vor das
wir das selber herstellen und wir haben dafür bis anfang Mai zeit!! wir bekommen eine note dafür in
chemie!! wenn sie informationen darüber haben, wie wir das herstellen könnten mit zwiebeln wären wir
ihnen sehr dankbar!!!!!!
A: Ihr solltet die Finger vom Tränengas lassen. Für CS-Gas benötigt
Ihr so etwas wie einen Waffenschein. Das benutzt die ESK bei Extremeinsätzen gegen uneinsichtige Gangster.
Und Zwiebelspray? Gegen wen wollt Ihr das einsetzen? Die Verletzungsgefahr ist groß. Baut euch eine Pfefferpistole,
wie sie der Räuber Hotzenplotz besitzt.