Versuch: Nachweis von Eiweißstoffen durch Erhitzen
Durchführung
Ein hitzebeständiges Glas wird zunächst mit Wasser gefüllt und dann auf einer Kochplatte
auf ca. 34-40 °C erhitzt.In der Wartezeit wird ein rohes Ei aufgeschlagen und das Eiklar
vom Eigelb getrennt.
Sobald das Wasser die passende Temperatur erreicht hat, wird das Eiklar in das Wasserbad
gegossen. Nun wird das Wasser weiter erhitzt.
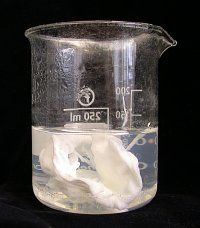
Am Ende des Versuches befindet sich darin eine weiße, feste Substanz. (Ihr kennt den Versuch:
In der Küche spricht man von einem "verlorenen Ei".)

(Foto: Daggi)
Erklärung
Das Eiklar besteht aus mehreren Eiweißstoffen. Eiweiße bestehen aus Riesenmolekülen,
zusammengesetzt aus vielen Aminosäuren.
Vorstellen kann man sich diese langen Molekülketten wie gegeneinander bewegliche Bindfäden.
Bei starker Hitze treten dieses Fäden miteinander in Verbindung, wobei die Struktur starr
wird und eine Verschiebung nicht mehr möglich ist.
Weil im Eigelb sogar mehr Eiweiß als im Eiklar enthalten ist, wird beim Eierkochen natürlich
auch dieses fest.
Das Eiweiß des Hühnereis gerinnt bei 60 °C; es flockt aus. Diese Gerinnung kann nicht wieder
rückgängig gemacht werden; man spricht deshalb auch von einer Denaturierung des Eiweiß.
Auch wir Menschen haben in unserem Blut Eiweiß. Dieses gerinnt aber schon bei einer Temperatur
von etwa 45 °C; deshalb ist hohes Fieber so gefährlich.
Nicht nur Hitze kann das Eiweiß zum Gerinnen bringen, sondern auch Säuren oder Alkohol,
Schwermetalle und Röntgenstrahlen.
Die Auswirkungen von Säure und Alkohol auf Eiweiß können in zwei weiteren Versuchen verdeutlicht werden.