Versuch: Untersuchung von Kunststoffen auf die Elemente Kohlenstoff und Wasserstoff
Sch³lerversuch; 20 min.
Beim Experimentieren den Allgemeinen Warnhinweis unbedingt beachten.
Gerõte
Porzellanschale, Glastrichter, U-Rohr, Waschflasche, Stativ, Stopfen, Glasrohre,
Wasserstrahlpumpe, Bunsenbrenner.
Chemikalien
Diverse Kunststoffproben, Kupfer(II)-oxid (Xn), Kalkwasser
(C), Cobaltchlorid-Papier (T).
Durchf³hrung
Diverse Kunststoffproben werden zerkleinert, jeweils in einer Porzellanschale
mit Kupfer(II)-oxid gemischt und mit der Brennerflamme entz³ndet.
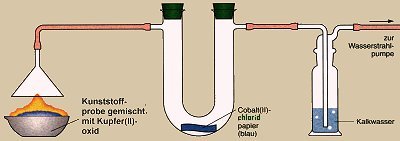
Anschlie▀end schiebt man die Schale, wie in der Abbildung dargestellt,
unter den Glastrichter der Apparatur und fõngt die Reaktionsprodukte auf.

(Quelle: Cornelsen)
Beobachtung
Im U-Rohr kondensiert Wasser, welches mit Cobaltchlorid-Papier
nachgewiesen wird.
In der Waschflasche mit Kalkwasser bildet sich ein wei▀er
Niederschlag.
Auswertung
Die in Kunststoffen enthaltenen Wasserstoff- und
Kohlenstoffatome werden oxidiert:
4 H + O2 à 2 H2O
C + O2 à CO2
Gleichzeitig wird das Kupfer(II)-oxid (Oxidationsmittel), welches den Sauerstoff f³r die Oxidationsreaktionen liefert, selbst zu Kupfer reduziert:
2 CuO à 2 Cu + O2
Cobaltchlorid-Papier enthõlt blaues Cobalt(II)-tetrachlorocobaltat(II), welches mit Wasser den rosafarbenen Hexaquocobalt(II)-chlorid-Komplex bildet:
Co[CoCl4] + 12 H2O à 2 [Co(H2O)6]Cl2
Kohlenstoffdioxid bildet mit Kalkwasser einen wei▀en Niederschlag aus feinverteiltem Calciumcarbonat:
CO2 + Ca(OH)2 à H2O + CaCO3 â
Literatur
R. Blume, Chemie f³r Gymnasien, Organische Chemie Themenheft 1, Cornelsen Verlag, Berlin 1994, 45.
H. Keune, W. Filbry, Chemische Schulexperimente, Verlag Harri Deutsch, Frankfurt a. M. 1978,
396.