 Quelle: [15]
Quelle: [15]
Versuch: Modellversuch zum sauren Regen
Schülerversuch; 20 min.
Beim Experimentieren den Allgemeinen Warnhinweis unbedingt beachten.
Geräte
Becherglas (200 ml), 2 Erlenmeyerkolben (100 ml), Plastiktüte (Inhalt ca. 5 l), Glasrohr.
Chemikalien
Autoabgase (T), Lackmusfarbstoff, destilliertes Wasser.
Durchführung
Zunächst wird eine Indikatorlösung für
Säuren und Basen hergestellt: Zu 100 ml destilliertem Wasser gibt
man wenig Lackmusfarbstoff. Die Lösung soll nur schwach violett
gefärbt sein. Anschließend wird sie gleichmäßig
auf 2 Erlenmeyerkolben verteilt.
Nun werden in einer Plastiktüte bei laufendem Motor
Autoabgase aufgefangen (Vorsicht! Die Gase nicht einatmen!).
Anschließend drückt man die Abgase mit Hilfe eines
Glasrohres, welches man vorsichtig in die Tüte schiebt, durch die Flüssigkeit in einem der beiden
Erlenmeyerkolben. Die Farben beider Flüssigkeiten werden
verglichen.
Beobachtung
Die schwach violette Flüssigkeit im Erlenmeyerkolben
hat sich durch das Lösen von Autoabgasen schwach rot gefärbt.
Auswertung
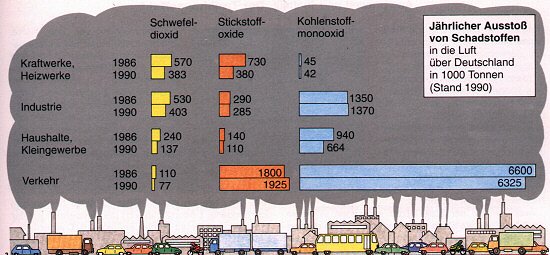
In Autoabgasen, aber auch in Abgasen von Heizkraftwerken,
Industrien und Haushalten sind verschiedene, gasförmige Nichtmetalloxide enthalten:
 Quelle: [15]
Quelle: [15]
Schwefeldioxid und Stickstoffoxide haben die Eigenschaft mit Wasser (z. B. Regen) zu Säuren zu reagieren. Dabei entstehen die schweflige Säure und die salpetrige Säure, die Bestandteile des sauren Regens sind:
SO2 + H2O ———> H2SO3 (schweflige Säure)
NO + NO2 + H2O ———> 2 HNO2 (salpetrige Säure)
Die Bildung von Säuren wird durch die Verfärbung der schwach konzentrierten Indikatorlösung angezeigt.
Literatur
R. Blume und Kollegen, Chemie für Gymnasien, D 1, Cornelsen Verlag, Berlin 1994, 128.