Die klassische Elementaranalyse - Liebigs Fünf-Kugel-Apparat
Experimente:
Versuch: Qualitative Elementaranalyse der Alkohole
Die Vorrichtung zur Elementaranalyse organischer Verbindungen wurde von Justus von Liebig (1803-1873)
im Jahre 1831 optimiert. Spätestens seit die Deutsche Post im Jahre 2003 eine Briefmarke zum Gedenken an
Liebigs 200. Geburtstag herausbrachte, sollte zumindest dem aufmerksamen Betrachter auch das optisch
bemerkenswerteste Stück der von Liebig erfundenen Apparatur bekannt sein: Es handelt sich um den
Fünf-Kugel-Apparat. Über nichts ist wohl (wenigstens was Darstellungen auf Briefmarken
angeht) soviel gerätselt worden, wie über die Funktion dieses Glasgeräts. Denn im modernen Chemie-Labor
ist es nicht mehr zu finden.
Nur wenn man alte Bücher zur Chemie durchblättert, wird man fündig. Hier ist ein Bild aus einem französischen Schulbuch aus dem Jahre 1875.

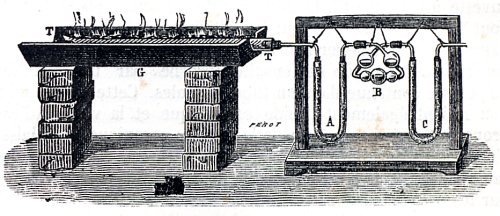
Apparatur zur Elementaranalyse von stickstofffreien Verbindungen nach J. v. Liebig
(Quelle: Langlebert)
Hier ist die Übersetzung der Beschreibung:
Das Bild zeigt den Apparat, bereit zur Analyse einer stickstofffreien Substanz.
TT ist das links verschlossene Verbrennungsrohr, das die entsprechende Substanz,
vermischt mit Kupferoxid, enthält;
G ist der Grill, auf dem man die glühende Kohle um das Rohr herumhäufelt;
A ist ein Rohr gefüllt mit Calciumchlorid oder mit Gestein, das mit Schwefelsäure
getränkt ist, um den Wasserdampf herauszuziehen ("recueillir"; herauspflücken);
B ist das Rohr mit Kugeln, die eine Lösung von Ätzkali zum Zurückhalten von
Kohlendioxid ("l´acide carbonique"; Kohlensäure) enthalten;
C ist ein Rohr, das mit Stücken von Ätzkali gefüllt ist, bestimmt dazu, die
letzten Reste von Kohlendioxid, die aus dem vorangegangenen Rohr entweichen konnten, zu absorbieren.
Am Ende des Rohres TT wird bei T etwas Kaliumchlorat aufgehäuft. Man erhitzt es zum Schluss der
Analyse, um daraus Sauerstoff freizusetzen. Der soll Reste von organischer Materie, die der Oxidation
durch das Kupferoxid entkommen ("échapper") konnten, verbrennen. Außerdem soll der Gasstrom die letzten
Reste des Kohlendioxids aus dem Verbrennungsrohr in die Rohre A, B und C treiben ("balayer"; fegen).
Zur Auswertung:
Man ermittelt die Differenz der Gewichte von A vor und nach der Messung. Das
ergibt die Menge an gebildetem Wasser, aus dem man die Menge an Wasserstoff berechnet.
Die beiden anderen Rohre B und C wiegt man zusammen vor und nach der Operation.
Die Differenz ergibt den Gehalt als Kohlendioxid, aus dem man den Gehalt an Kohlenstoff
berechnet.
Wenn die so erhaltenen Werte nicht exakt die Menge an eingewogener Substanz ergeben, berechnet man aus
der Differenz den Gehalt an Sauerstoff.
Warum die fünf Kugeln?
Zuvor eine Anmerkung: Das Oxidationsprodukt CO2 ist in Wasser schlecht löslich. Wenn es nur
durch ein einziges mit KOH gefülltes Gefäß perlen würde, würde die Absorption nur begrenzt ausfallen. Das
war dem Justus von Liebig sicherlich bekannt. Durch die Anordnung der fünf Kugeln wird die Löslichkeit
wesentlich verbessert. Denn da stehen hintereinander fünf Gasräume mit ihren Flüssigkeiten im
Austausch-Gleichgewicht.
Schauen wir einmal genauer hin. Das Bild auf der Briefmarke gibt den Zustand der Apparatur während der Analyse nicht richtig wieder: Zwei der fünf Kugeln sind nicht gefüllt. Der alte Kupferstich zeigt das schon genauer: Hier sind alle fünf Kugeln halb gefüllt. Was ist nun richtig? Glauben wir ruhig den "Alten".
Kann man so etwas überhaupt füllen? Jawohl: Durch die sinnreiche Anordnung der Kugeln werden alle nur halb gefüllt.
Um durch ein solches Gefäßsystem Gase durchzuleiten, bedarf es eines gewissen Überdrucks. Der baut sich auf
folgende Weise auf: Zunächst einmal ist das Verbrennungsrohr am linken Ende verschlossen. Die bei der Oxidation
mit CuO gebildete Gasmischung aus CO2 und Wasserdampf hat deshalb nur einen Ausweg, den durch die
Gläser A, B und C. Der Wasserdampf wird durch das CaCl2 sofort absorbiert, was außerdem durch die
Abkühlung bestens unterstützt wird.
Das übrig bleibende CO2 hat keinerlei Chance, in irgendeinen Gasraum zu entweichen. Denn es wird
in der Fünf-Kugel-Apparatur immer wieder von einer Flüssigkeit in die nächste Flüssigkeit geleitet, ja förmlich
hineingedrückt.
Er war ganz schön clever, der Liebig - pardon: der Herr von Liebig! Er soll auf seinen Titel sehr viel Wert gelegt haben...
Literatur:
J. Langlebert: Manuel de Chimie. Impr. Jules Delalain et Fils. Paris 1875 (25e Edition).
Weitere Texte zum Thema „Alkohol“