 |
| Aromatenmischung |
Bestimmung von polycyclischen, aromatischen Kohlenwasserstoffen (PAHs) in einer Testmischung mit HPLC
Beim Experimentieren den Allgemeinen Warnhinweis unbedingt beachten.
1. Problemstellung
In diesem Anwendungsbeispiel f■r die Umweltanalytik wird die Trennung von
polycyclischen, aromatischen Kohlenwasserstoffen (PAHs) an einer bekannten Testmischung vorgestellt. Zur
Identifizierung wird ein UV-Detektor eingesetzt. Es wird bei einer
Wellenlðnge von 260 nm gemessen.
2. Substanzen
Acenaphthen, Anthracen, Benzol, Biphenyl, Chrysen, Fluoren, Naphthalin,
Phenanthren, Pyren und Toluol.
3. Durchf■hrung
3.1 Probenaufarbeitung
Ca. 1 mg der festen Aromaten und 100 çl der fl■ssigen Aromaten werden in
10 ml Acetonitril gel—st. Zur Trennung der einzelnen Aromaten werden die
L—sungen im Verhðltnis 1:1 zusammengegeben und direkt injiziert.
AnschlieÔend werden die Proben bei gleichen Chromatographiebedingungen
einzeln eingespritzt, um die Retentionszeiten und somit die Reihenfolge der
Aromaten zu ermitteln.
3.2 Chromatographiebedingungen
| HPLC-System: | Shimadzu (6A/6B-Serie) |
| Sðule: | ET 150/8/4 Nucleosil 5 C18 PAH |
| FlieÔmittel: | (A) 48 % bidestilliertes Wasser
(B) 52 % Acetonitril |
| FluÔrate: | 1 ml/min |
| Zeitprogramm: | 10 min B.Conc. 52 %
16 min B.Conc. 80 % 21 min B.Conc. 100 % 28 min B.Conc. 100 % 30 min B.Conc. 52 % 30 min stop |
| Dosiervolumen: | 20 çl |
| Wellenlðnge: | 260 nm |
4. Ergebnisse
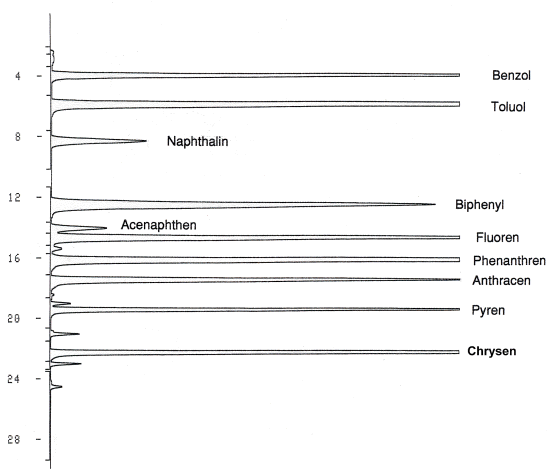
Die Abbildung zeigt ein Chromatogramm der
Aromatenmischung. Die Reihenfolge mit ungefðhren Retentionszeiten der
Aromaten ist aus folgender Tabelle zu entnehmen.
 |
| Aromatenmischung |
| Aromaten | Retentionszeit |
| Benzol
Toluol Naphthalin Biphenyl Acenaphthen Fluoren Phenanthren Anthracen Pyren Chrysen |
4,081/4,064
5,866/5,922/5,898 8,658/8,398/8,392 12,578 14,132/14,467 14,998 16,33/16,291 17,791 19,598/20,041 22,938/22,904 |
Reale Untersuchung einer Bodenprobe auf PAHs mit HPLC
1. Problemstellung
Da die polycyclischen, aromatischen Kohlenwasserstoffe (PAHs) in mehr oder
weniger hoher Konzentration in Boden, Wasser, Luft und auch in Lebensmitteln
vorkommen, gewinnt die Bestimmung dieser Aromaten immer mehr an Bedeutung.
Ein Beispiel f■r eine Analysenmethode soll das folgende Beispiel geben.
2. Substanzen
Boden, die Aromatenmischung aus dem
Vorversuch und Weichmacher (Bis(2-ethylhexyl)-phthalat).
3. Durchf■hrung
3.1 Probenaufarbeitung
10 g Bodenprobe + 10 g Na2SO4 (wasserfrei) werden mit 20 ml Cyclohexan
versetzt und 45 Minuten ins Ultraschallbad gestellt.
AnschlieÔend wird die Probe filtriert und zwei Mal mit je 10 ml Cyclohexan nachgewaschen. Die L—sungen werden vereinigt und bis zur Trockne eingedampft. Der R■ckstand wird in 5 ml Acetonitril gel—st.
Die Probenl—sung wird ■ber ein Membranfilter mit 0,45 çm Porenweite filtriert und anschlieÔend direkt in die HPLC-Anlage injiziert.
Um die einzelnen Aromaten der Bodenprobe genau identifizieren zu k—nnen, wird die Probenl—sung anschlieÔend mit den L—sungen der einzelnen Substanzen versetzt. Anhand der vergr—Ôerten Peakflðchen werden die Aromaten des belasteten Bodens bestimmt.
3.2 Chromatographiebedingungen
| HPLC-System: | Shimadzu (6A/6B-Serie) |
| Sðule: | ET 150/8/4 Nucleosil 5 C18 PAH |
| FlieÔmittel: | (A) 48 % bidestilliertes Wasser
(B) 52 % Acetonitril |
| FluÔrate: | 1 ml/min |
| Zeitprogramm: | 10 min B.Conc. 52 %
16 min B.Conc. 80 % 21 min B.Conc. 100 % 28 min B.Conc. 100 % 30 min B.Conc. 52 % 30 min stop |
| Dosiervolumen: | 20 çl |
| Wellenlðnge: | 260 nm |
4. Diskussion
Vergleichen Sie die Chromatogramme.
Wie belastet ist der untersuchte Boden?
Kann man Toluol nach dem Eindampfen zur Trockne wiederfinden?
Welche Substanzen haben Sie im Boden sicher nachweisen k—nnen?