Schwefeldioxid SO2
1 Bildung von SO2
- Verbrennen von pyrithaltiger Kohle (besonders von Braunkohle)
- Verbrennen von Biomasse (Holz, Tierabfðlle)
- Heizungsbetrieb mit nicht entschwefeltem Heiz—l
- Betrieb von Motoren mit nicht entschwefelten Treibstoffen
- Verbrennen von Gummi
- R—sten von sulfidischen Erzen
- Oxidation der Quellgase H2S und CS2
- Vulkanismus und andere geochemische Prozesse
2 Eigenschaften und Wirkungsmechanismen von SO2
- Gute Wasserl—slichkeit und Sðurebildung
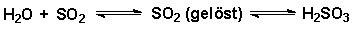
- Reduktionsmittel; leichte Oxidierbarkeit zu Schwefelsðure
HSO3- + ½ O2 ———> HSO4-
(-> Versauerung von Umweltmedien, St—rung der Sauerstoffbilanz,
Verðtzung von Lungengewebe)
- Quellgas
SO2 + 2 HO· ———> H2SO4
(-> Atmosphðrische Bildung von Schwefelsðure; Saurer Regen;
Ozonabbauende PSC)
- Reaktionen mit Aldehyden (Additionsverbindung)
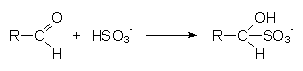
(-> St—rung von: Glykolyse, Reaktionen mit Vitamin B6 (Pyridoxal),
Synthese der Nucleinsðurebasen, -> Wachstumshemmung von Mikroorganismen)
- Ausbleichen von Farbstoffen