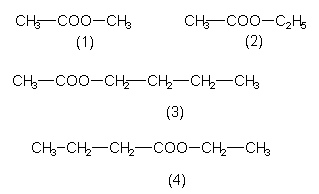
5.10 Beispiele für schonende Verfahren der organischen Chemie
Organisch chemische Industrieverfahren führen häufig zu Schadstoffen, deren Bildung oder gar Freisetzung durch geeignete Präventivmaßnahmen verhindert werden kann. Als Beispiele werden zwei Verfahren gewählt, bei denen ganz besonders große Mengen Abfallschwefelsäure entstehen, die Estersynthese und die Herstellung von Phenol. Es werden zunächst die klassischen Verfahren und dann die modernen Verfahren unter dem Gesichtspunkt der Entwicklung schadstoffarmer Technologien geschildert.
5.10.1 Herstellung von Estern
Synthetische Carbonsäureester wie Essigsäuremethylester (1), Essigsäureethylester (2) oder Essigsäurebutylester (3) sind von großer wirtschaftlicher Bedeutung. Sie werden als unpolare Lösemittel verwendet. Bestimmte Ester sind von intensiv fruchtigem Geruch und Geschmack und werden als Geruchs- und Aromastoffe vielfach verwendet. Der Buttersäureethylester (4) riecht nach Ananas.
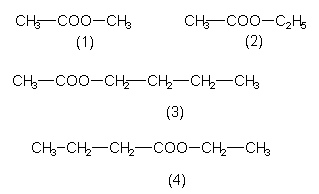
Für die industrielle Herstellung von Carbonsäureestern gibt es eine Vielzahl unterschiedlichster Syntheseverfahren. Es soll hier nur auf die sehr wichtige direkte (klassische) Estersynthese aus Carbonsäure und Alkohol eingegangen werden. Diese Synthese ist eine säurekatalysierte Gleichgewichtsreaktion:
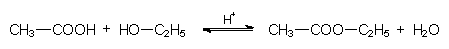
Zur quantitativen Gewinnung des Produktes ist es notwendig, das gebildete Wasser während der Reaktion möglichst vollständig zu entfernen. Ist der Ester leichter flüchtig als die Edukte, kann er abdestilliert werden.
Schwefelsäure als Veresterungskatalysator
Alkohol und Carbonsäure reagieren in Gegenwart von
konzentrierter Schwefelsäure zum Ester. Schwefelsäure erfüllt als
Katalysator und als wasserbindendes Mittel eine Doppelfunktion.
Man muss sie deshalb im Überschuss zugeben, da sie sich sonst zu
stark verdünnt und die Rückreaktion (Esterspaltung) zunimmt.
Der Nachteil dieses Verfahrens besteht darin, dass nach Beendigung der Reaktion die Schwefelsäure durch mehrmalige Extraktion der Reaktionsmischung mit Wasser entfernt werden muss. Als problematischer Abfall entsteht so eine mit organischen Verbindungen verunreinigte verdünnte Säure (Dünnsäure; -> 5.2).
Die Abfallschwefelsäure kann bei einem geringen Anteil an Verunreinigungen wieder aufkonzentriert und erneut eingesetzt werden. Andernfalls ist es möglich, die Säure bei 1000 °C thermisch zu spalten:
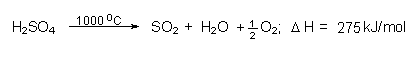
Das hierbei gebildete Schwefeldioxid wird im Kontaktverfahren wieder zu konzentrierter Schwefelsäure verarbeitet.
Alle diese Entsorgungsverfahren für Abfallschwefelsäure sind energieaufwendig und kostenintensiv. So ist die Herstellung reiner Schwefelsäure aus Abfallsäure etwa dreimal so teuer wie die Herstellung aus elementarem Schwefel. Deshalb wurden bisher erhebliche Mengen Abfallsäuren auf See verklappt.
Saure Ionenaustauscher als Veresterungskatalysatoren
Statt der Schwefelsäure kann ein saures Ionenaustauscherharz als
Katalysator eingesetzt werden. Diese festen Katalysatorharze
verändern sich in dem Reaktionsmedium kaum, wirken aber leider
auch nicht wasserentziehend. Das gebildete Wasser muss daher,
beispielsweise durch azeotrope Destillation mit einem Schlepper
wie Toluol, aus dem Gleichgewicht entfernt werden. Bei diesem
Verfahren erhält man als Abfall lediglich das Reaktionswasser, das
mit organischen Verbindungen verunreinigt ist. Der Ionenaustauscher kann vom
Reaktionsmedium einfach durch Filtration abgetrennt und direkt für die gleiche
Reaktion wiederverwendet werden.
5.10.2 Synthese von Phenol
Phenol (Benzolalkohol C6H5OH) wurde zunächst zum Desinfizieren benutzt (Carbolsäure, Lysol). Sodann trat die Verwendung bei der Herstellung des Sprengstoffs Pikrinsäure in den Vordergrund, bis die Entdeckung der Phenol-Formaldehyd-Polykondensate zu einer weiteren starken Steigerung des Bedarfs führte. Phenol ist heute eine wichtige Grundchemikalie der industriellen organischen Chemie. Es wird für die Herstellung von vielen Kunststoffen, Klebstoffen und Lacken, Farbstoffen, Pestiziden und Arzneimitteln verwendet.
In der Anfangszeit der industriellen organischen Chemie wurde Phenol lediglich aus Steinkohlenteer gewonnen (-> 5.9.2). Um den großen Bedarf zu befriedigen, wurde nach synthetischen Verfahren zur Phenolgewinnung im großen Maßstab gesucht.
Die herkömmlichen Synthesen
Bei beiden Verfahren treten erhebliche Umweltbelastungen durch
flüssige und feste Abfälle auf.
A. Phenolsynthese aus Chlorbenzol
Dieses Verfahren wurde in Deutschland bis zum Beginn der 70er
Jahre angewandt.
Das Edukt Chlorbenzol wird katalytisch aus Benzol und Chlor hergestellt. Hierbei fällt (neben mehrfach chloriertem Benzol) vor allem Chlorwasserstoffgas (HCl) an. Anschließend wird Chlorbenzol mit Natronlauge unter hohem Druck hydrolysiert. Das gebildete Natriumphenolat wird (z. B. mit dem oben erhaltenen) HCl zu Phenol umgesetzt.
Bei dieser Druckhydrolyse entstehen pro Tonne Phenol als Nebenprodukt 1,5 t Natriumchlorid. An Abwasser fallen 10 m3 an. Bedenklich sind als Nebenprodukte gebildete mehrfach chlorierte Aromaten sowie Chlorphenole.
B. Phenolsynthese aus Benzolsulfonsäure
Dieses Verfahren (-> Abb. 29) wurde in Deutschland bis zu Beginn der 60er Jahre angewandt.
Benzol wird zunächst mit einem Überschuss an konzentrierter Schwefelsäure (Oleum) sulfoniert und dann mit festem Natriumhydroxid geschmolzen (verbacken). Das Natriumphenolat wird anschließend mit Salzsäure in Phenol umgewandelt.
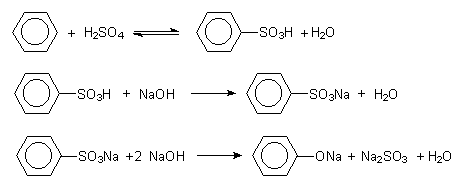
Abb. 29: Phenolsynthese aus Benzolsulfonsäure
An Nebenprodukten entstehen pro Tonne Phenol bei der Neutralisation des Oleumüberschusses etwa 2 t Natriumsulfat und 1,4 t Natriumsulfit und bei der Umwandlung von Phenolat 0,61 t NaCl. Die Abwassermenge beträgt mehr als 10 m3.
Die umweltschonende Hocksche Phenolsynthese
Wesentlich umweltverträglicher als die beiden ersten geschilderten
Synthesen ist dagegen die heute größtenteils übliche Synthese von
Phenol nach Hock (-> Abb. 30). Das Produkt entsteht in sehr hoher Ausbeute,
ohne dass große Mengen an Abwasser und nicht verwertbaren
Nebenprodukten anfallen.
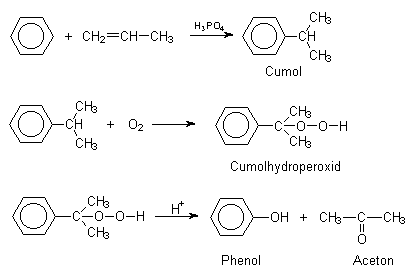
Abb. 30: Hocksche Phenolsynthese
Benzol wird in einer Friedel-Crafts-Alkylierung zunächst mit dem beim Cracken von Erdölprodukten anfallendem Propen zu Cumol umgesetzt. Letzteres reagiert mit Luftsauerstoff zu Cumolhydroperoxid, das säurekatalysiert zu Phenol und Aceton umgelagert wird.
Je Tonne Phenol entstehen 620 kg Aceton, etwa 50 kg organische Nebenprodukte und nur 0,5 m3 Abwasser. Da Aceton innerhalb der organischen Chemie ein breites Anwendungsspektrum besitzt - z. B. als Lösemittel - und auch die anderen Produkte zu verkaufsfähigen Chemikalien aufgearbeitet werden können, spricht man hier von Koppelprodukten.