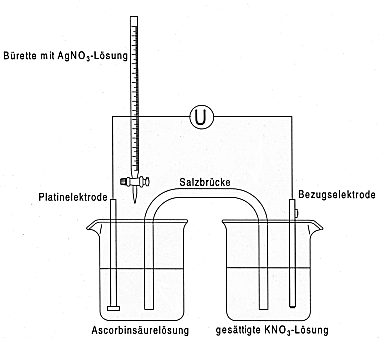
Versuch: Potentiometrische Titration der Ascorbinsäure mit Silbernitrat
Schülerversuch; 30 min.
Beim Experimentieren den Allgemeinen Warnhinweis unbedingt beachten.
Geräte
Bürette (50 oder 100 ml), geeichtes pH-Meter mit Glaselektrode, Spannungsmessgerät mit Platinelektrode
sowie mit Bezugselektrode (Silber/Silberchlorid oder ähnliches), Salzbrücke
(Glasrohr mit blasenfreier 1%iger Gelatine in gesättigter Kaliumnitratlösung.
Alternativ ein mit Kaliumnitratlösung getränktes Filterpapierröllchen).
Chemikalien, Lösungen
Ascorbinsäurelösung in Wasser (c = 0,01 mol/l), frisch zubereitete Lösung von
Silbernitrat (c = 0,01 mol/l) (Xi), Kaliumnitrat.

(Skizze: Wolfgang Below)
Durchführung
Stelle den Versuchsaufbau entsprechend der Abbildung zusammen. Der relativ
komplizierte Aufbau ist notwendig, weil das Titriermittel mit dem Chlorid, das aus
der offenen Bezugselektrode ausströmt, reagiert. Das führt nicht nur zu
Konzentrationseinbußen an Silber-Ionen, sondern auch zum Zusetzen des
Diapragmas der Bezugselektrode durch ausfallendes Silberchlorid.
Verfügt man über eine Mercurisulfatelektrode, so kann man diese direkt in die
Titrierlösung stellen! Leider werden diese Elektroden nicht mehr hergestellt.
50 ml der Ascorbinsäure-Lösung werden mit einer gleichmolaren Silbernitrat-Lösung
titriert.
Messe die Spannung. Zu Beginn muss man etwas warten, bis sich das
Elektrodengleichgewicht eingestellt hat.
Parallel zur Spannungsmessung wird der pH-Wert notiert.
Zugabe in Schritten von 10 ml bis zur Gesamtzugabe von 150 ml.
Auswertung
Zeichne in ein Diagramm die pH-Werte sowie die Spannungs-Werte (Ordinate)
gegen die ml-Zahl an Silbernitratlösung (Abszisse).