
Die Bildung von Chinhydron. Die Chinhydron-Elektrode
Experimente:
Versuch: Die Bildung von Chinhydron
Hydrochinon wird unter Einwirkung von Eisen(III)-chlorid zunächst zu orangegelbem Benzochinon
oxidiert. Vermeidet man Eisen(III)-Überschuss, so dass nicht alles Hydrochinon oxidiert wird, so
bildet sich anschließend schwarzgrünes, metallisch glänzendes Chinhydron.

Bild 1: Das Redox-Paar Hydrochinon und Benzochinon
(Foto: Blume)

Bild 2: Kristalle von Chinhydron (Foto: Helene)
Chinhydron ist ein in Wasser schwer löslicher Komplex aus Hydrochinon und Benzochinon.
Es wird zusätzlich über zwei Wasserstoffbrücken stabilisiert.
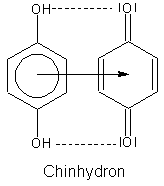
Einen solchen Komplex bezeichnet man als Charge-Transfer-Komplex (CT-Komplex) oder auch als Donator-Akzeptor-Komplex. Er beruht auf der Wechselwirkung der p-Elektronen einer elektronenreichen Komponente (Donator) und einer elektronenarmen Komponente (Akzeptor). Der Donator ist im Falle des Chinhydrons das Hydrochinon. Der +M-Effekt der beiden OH-Gruppen erhöht nämlich die Elektronendichte im aromatischen Sechsring, so dass dieser elektronenreich wird und so als Donator wirken kann. Das Benzochinon ist der Akzeptor, denn sein Sechsring weist einen Elektronenmangel infolge des -I-Effekts der beiden Sauerstoffsubstituenten auf.
Aufgrund der Wechselwirkung der p-Elektronen kommt es zu einer erleichterten Anregbarkeit durch elektromagnetische Strahlung. Daraus resultiert die auffällige Färbung aller CT-Komplexe. Weitere Beispiele für CT-Komplexe sind die aus Pikrinsäure (Akzeptor) und verschiedene Aromaten wie Anthracen (Donator).
Chinhydron ist nicht nur ein schönes Beispiel für einen CT-Komplex. Es spielt vor allem in der Elektrochemie eine wichtige Rolle. Der Grund ist, dass das Redoxpotential zwischen Hydrochinon (H2Q) und seiner oxidierten Form Chinon (Q) pH-abhängig ist.
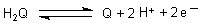
Stellt man hierzu die Nernstsche Gleichung auf, so erhält man
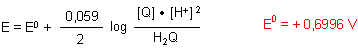
Da sich in diesem Komplex die Konzentrationen von Hydrochinon und Chinon wie 1 : 1 verhalten, folgt daraus eine direkte Abhängigkeit des Potentials vom pH-Wert.
E = E0 - 0,059 pH
Vor Einführung der komfortablen Glaselektroden hat man Chinhydron-Elektroden zur pH-Messung verwendet. Als Ableitelektrode dient ein Platin- oder Goldblech. Man verwendet die Chinhydron-Elektrode aber auch heute noch als Bezugssystem anstelle der Standardwasserstoffelektrode. Dabei ist die Chinhydron-Elektrode wesentlich einfacher zu handhaben und vor allem ungefährlicher.
Weitere Texte zum Thema „Phenole“