Vom Aldehyd zum Acetal - vom Keton zum Ketal
Aldehyde und Ketone reagieren mit Alkoholen. Es bilden sich im Fall der Aldehyde Halbacetale und Acetale (auch Vollacetale genannt). Mit Ketonen bilden sich Halbketale und Ketale. Man spricht aber in beiden Fällen von Acetalen.
Eine Reaktion mit großer Bedeutung
Die (Halb-)Acetalbildung ist von großer Bedeutung, sei es für die Natur oder für die Industrie.
Beide haben gelernt, diese Verbindungsklasse für sich nutzbar zu machen. In der Natur findet man die
Halbacetalbindung beispielsweise in Kohlenhydraten: Die beiden Acetalbildungsreaktionen ermöglichen
erst die typische Ringbildung. Vollacetale liegen bei der Verknüpfung von Monosacchariden zu Oligo-
oder Polysacchariden vor.
In der technischen und wissenschaftlichen Chemie verwendet man die Halbacetale sowie die Vollacetale (vor allem cyclische) bei Synthesen als Schutzgruppen für die Carbonylgruppe. Mit der analogen Ketalbildung durch Aceton konnte man sogar die reale Konfiguration von Zuckermolekülen aufklären.
Bildung von Halbacetalen
Die Reaktion von Aldehyden oder Ketonen mit Alkoholen stellt eine der wichtigsten nucleophilen Additionen
dar. Sie liefert Halb- und Vollacetale.

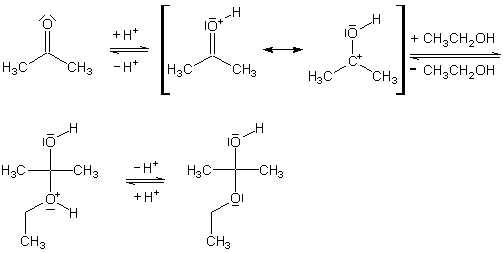
Schematische Darstellung des Reaktionsmechanismus der Halbacetalbildung
am Beispiel der Reaktion von Aceton mit Ethanol
Die Reaktion zum Halbacetal findet in saurem Milieu statt. Die Protonen der Säure dienen hier lediglich als Katalysator. Zu Beginn reagiert ein Proton mit dem Sauerstoff des Acetons; das C-Atom der Carbonylgruppe bekommt eine positive Ladung. Setzt man diese Verbindung nun mit Ethanol um, so bindet das partial negativ geladene Sauerstoffatom des Ethanols an das positiv geladene C-Atom der Carbonylgruppe. Durch die Abspaltung des an das Sauerstoffatom gebundenen Protons entsteht das Halbacetal.
Halbacetalbildung und -spaltung werden durch Säuren und vor allem auch durch Basen katalysiert; die Reaktion ist vollständig reversibel.
Bildung von Vollacetalen
Liegt Alkohol im Überschuss vor, so geht diese Reaktion über die Halbacetal-Stufe hinaus, und es bildet
sich ein Vollacetal. Die saure Katalyse ist hierfür eine notwendige Voraussetzung.
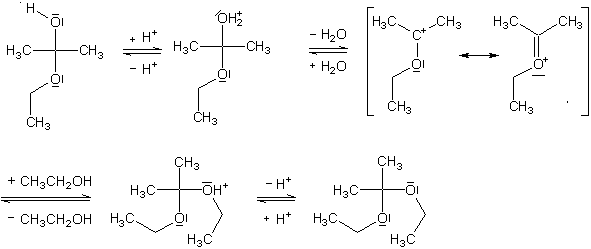
Schematische Darstellung des Reaktionsmechanismus der Acetalbildung
Acetalbildung und -spaltung werden nur von Säuren (besser: durch Protonen) katalysiert. Das Proton der Säure addiert an die Hydroxyl-Gruppe des Halbacetals, wodurch an dieser Stelle eine positive Ladung entsteht. Im nächsten Schritt spaltet ein Wassermolekül ab. Energetische Gründe hierfür liegen in der Zunahme der Entropie (Unordnung) durch die Wasserabspaltung. Die so entstehende Verbindung hat eine positive Ladung am C-Atom. Gibt man nun Ethanol hinzu, so kann sich sein partial negativ geladener Sauerstoff an das positiv geladene C-Atom anlagern. Durch die Abspaltung eines Protons erhält man schließlich das Vollacetal.
Das Vollacetal ist verglichen mit dem Halbacetal relativ stabil. Allerdings kann das Vollacetal ebenfalls gespalten werden - allerdings nur durch Säuren und dazu noch unter Aufwand von viel Energie. Das spielt eine Rolle bei der Spaltung von Cellulose durch heiße Salzsäure. Diese "Holzverzuckerung" ist Grundlage für die Bildung von "Biosprit" durch Vergärung von aus Holzabfällen gewonnener Glucose.
Weitere Texte zum Thema „Aldehyde und Ketone“