Reaktionen Nullter Ordnung
Betrachten wir eine Reaktion wie z. B. den Zerfall eines Stoffs. Erhitzt man Bromethan, so spaltet sich Bromwasserstoff ab, es entsteht Ethen:
C2H5Br ———> C2H4 + HBr
Wir verfolgen den Verlauf der Reaktion und beobachten, dass einmal die
Konzentration linear abnimmt, das andere Mal die typische Abklingkurve zeigt. Wie
kann das erklärt werden?
Im ersten Fall ist die Reaktionsgeschwindigkeit unabhängig von der Konzentration des
Stoffs. Er zerfällt nämlich an der Oberfläche eines festen Katalysators, der mit seinem
"Substrat" gesättigt ist. Das kann z. B. Zink sein, wie bei der typischen
schulchemischen Reaktion zur Herstellung von Ethen. Die Reaktionsgeschwindigkeit
hängt dann nur von der Konzentration des Katalysators ab, ist also proportional zu
seiner Oberfläche. (Das beobachten wir auch im Bereich der hohen
Substratkonzentration bei der Michaelis-Menten-Gleichung!) Wir sprechen hier von
einer Reaktion 0. Ordnung, d. h. die Reaktionsgeschwindigkeit ist unabhängig von
der Konzentration der Edukte.
dcA / dt = - k
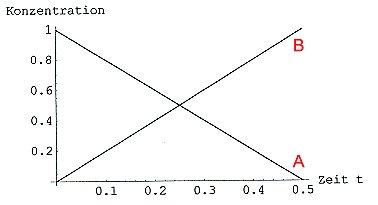
Die Integration ergibt im Konzentrations-Zeit-Diagramm eine Gerade.
cA = cA0 - k · t

Konzentrations-Zeit-Diagramm einer Reaktion 0. Ordnung
Zwischen der Halbwertszeit und der Geschwindigkeitskonstanten einer Reaktion 0. Ordnung besteht
die folgende Beziehung:
k · t½ = cA0/2
Die Halbwertszeit hängt also von der Anfangskonzentration ab - das kann man leicht verstehen.
Bei einer Reaktion ohne Katalysator reicht die Zufuhr von Energie aus, um den Zerfall von Bromethan in die Wege zu leiten. Dann sprechen wir von einer Reaktion 1. Ordnung.
Weitere Texte zum Thema „Reaktionskinetik“