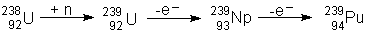
Ascorbinsäure und die Wiederaufbereitung von Kernbrennstäben
nach dem Purex-Verfahren
Vitamin C zeigt seine vielseitigen Einsatzmöglichkeiten auch in der Wiederaufbereitung von Brennstäben aus Atomkraftwerken.
Normalerweise laufen in Kernkraftwerken Spaltreaktionen ab, wie zum Beispiel von Uran-235 oder Plutonium-239. In anderen Atomkraftwerken ("Brüter") wird mit Hilfe einer anderen Kernreaktion, dem Neutroneneinfang, aus Uran Plutonium hergestellt.
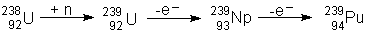
Diese exotherme "Erbrütung" des Plutoniums wird nicht nur zur Stromerzeugung genutzt. Das
entstandene Pu-239 ist zugleich ein wichtiger Rohstoff für Plutonium-Spaltreaktoren
und für Kernwaffen. Denn Pu-239 kann wie der Spaltstoff U-235 durch langsame
Neutronen in exothermer Reaktion gespalten werden.
In den Uran-Kernkraftwerken wird nur ein kleiner Teil des spaltbaren U-235 verbraucht;
zur Rückgewinnung des beträchtlichen Rests muss es von den Spaltprodukten abgetrennt werden.
Bei Brutreaktoren gilt das gleiche für das erbrütete Pu-239, das neben dem nicht umgesetzten
U-238 vorliegt. Die Abtrennung kann allein durch chemische Reaktionen erfolgen. Dazu bedarf es
einer ausgefeilten Technik. Dabei muss man immer bedenken, dass es sich um
hochgradig gefährliche Stoffe handelt, einerseits wegen ihrer Radioaktivität,
andererseits auch wegen ihrer besonders beim Plutonium extrem ausgeprägten
Toxizität. Das gängigste Trennverfahren nennt man Purex
(Plutonium-Uranium-Recovery by Extraction).
Im ersten Arbeitsschritt werden die Brennstäbe zersägt und in 130 °C heißer,
konzentrierter Salpetersäure (c = 8 mol/l) zersetzt. Es bilden sich lösliches
Plutonium(IV)-nitrat Pu(NO3)4 und lösliches Uranyl(VI)-nitrat
UO2(NO3)2.
Die anschließende extraktive Trennung erfolgt mit einem besonderem flüssigen
Extraktionsmittel, TBP 30 in reinem Kerosin (Reinstpetroleum, auch bekannt als
Jet-Treibstoff). Dabei handelt es sich um Tri-n-Butyl-Phosphat,
also um einen Phosphorsäure-ester.
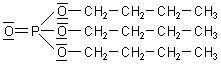
Tri-n-Butyl-Phosphat
Das TBP bildet in saurem Milieu mit Plutoniumnitrat und Uranylnitrat in Kerosin
lösliche Komplexe wie z. B. UO2(NO3)2
· 2 TBP. Damit kann man diese beiden
Metalle aus der Salpetersäure durch ein Gegenstromverfahren, das einem kontinuierlichen
Ausschütteln entspricht, abtrennen. Zurück bleiben die Spaltprodukte sowie die
anderen Actiniden. Genau genommen handelt es sich hier um einen
niedermolekularen, selektiven flüssigen Ionenaustauscher, wie er uns auch schon
bei der nasschemischen Abtrennung von Kupfer
begegnet ist.
Zur völligen Abtrennung wird dieser Prozess mehrfach wiederholt.
Im nächsten Durchgang werden die TBP-Komplexe aus der organischen Phase durch Ausschütteln mit verdünnter Salpetersäure gespalten; die Nitrate von Pu(IV) und U(VI) gehen wieder in die wässrige Phase über.
Zur Auftrennung von Uran und Plutonium wird das rote Pu(IV) zu blauem Pu(III) reduziert. Denn Pu(III)-nitrat bildet mit TBP keinen Komplex und bleibt deshalb in der wässrigen Phase. Man extrahiert anschließend erneut wie oben beschrieben, um Uran(VI) in die Kerosinphase zu transportieren und so abzutrennen.
Als Reduktionsmittel kommen in Frage: Uran(IV)-Salze, Eisen(II)-Komplexe oder - Ascorbinsäure !
Zuletzt wird Pu(III) zurückoxidiert und zur weiteren Reinigung erneut extrahiert. Es folgen Reinigung und Aufkonzentrierung von Pu(IV) durch Ionenaustausch. Auch hierzu nimmt man flüssige Ionenaustauscher wie den Bis-(2-ethylhexyl)-phosphorsäure-ester, denn feste Ionenaustauscher würden durch die starke Strahlung sofort zerstört.
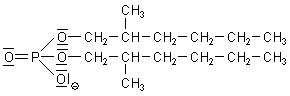
Bis-(2-ethylhexyl)-phosphorsäure-ester
Dann wird der Komplex in Pu(IV)-oxalat überführt und anschließend erhitzt
("calciniert"), wobei sich das als Brennstoff für die Kernkraftwerke geeignete
Plutonium(IV)-oxid PuO2 bildet.
Man kann aber auch aus PuO2 und UO3 direkt ohne Abtrennung Kernbrennstäbe
herstellen (Mischoxid-Kernbrennstäbe; abgekürzt MOX ).
Durch Reduktion der Oxide lassen sich natürlich auch die Metalle gewinnen.
Weitere Texte zum Thema „Ascorbinsäure“