Cyclohexan - Sessel und Wanne
Im Cyclohexan (C6H12) findet man die erste spannungsfreie
Ringstruktur in der Gruppe der Cycloalkane. Ein
Cyclohexanmolekül kann in verschiedenen Konformationen vorliegen, wobei die
Sesselform als einzige Konformation tatsächlich spannungsfrei ist.
Die Orbitale der Kohlenstoffatome sind sp3-hybridisiert. Alle C-C-Winkel entsprechen
in der Sesselform mit 111° fast dem Tetraederwinkel (109,5°). Auch die gebundenen Wasserstoffatome
stehen im "Cyclohexansessel" in gestaffelter Konformation und nicht wie beim Cyclopropan
und Cyclobutan verdeckt in Reihe. Hierdurch wird ebenfalls eine Ringspannung vermieden.
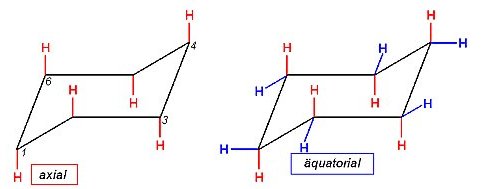
Das Zeichnen eines Cyclohexanmoleküls scheint nach all diesen Angaben sehr kompliziert. Am besten beginnt man mit zwei parallelen Linien. Dann malt man die Spitzen - eine nach oben, eine nach unten. Alle gegenüberliegenden Seiten sind paarweise parallel. Dann malt man an jedes C-Atom ein H-Atom mit einem Bindungsstrich, der senkrecht nach unten bzw. nach oben zeigt. Wir haben dabei im Blick, dass sich an den C-Atomen wegen der sp3-Orbitale Tetraeder-Konfiguration einstellen muss. Deshalb zeichnen wir noch die anderen sechs H-Atome entsprechend ein - schräg nach oben oder schräg nach unten.

6 H-Atome (rot gezeichnet) stehen senkrecht zur Molekülachse und werden deshalb als axial bezeichnet. Die anderen 6 H-Atome (blau gezeichnet) liegen in der Molekülebene und werden deshalb auch äquatorial genannt.
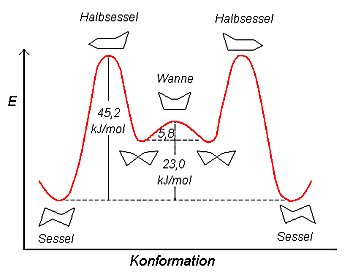
Neben der Sesselform besitzt das Cyclohexan weitere, weniger stabile Konformationen. In der Boot- oder Wannenform stehen das C1- und das C4-Atom aus der Ebene des Ringes in eine gemeinsame Richtung heraus. Hierbei können sich allerdings die Wasserstoffatome ins Gehege kommen, da sie sich räumlich annähern. Das führt zu einer Steigerung des Energieinhalts - wie das folgende Diagramm zeigt. Dazu gibt es noch zwei Halbsessel mit erzwungener Planarität sowie zwei verdrehte Formen.
Die Energiebarrieren zur Umwandlung von einer Konformation in eine andere sind so gering (45,5 kJ/mol), dass schon bei Zimmertemperatur die Umwandlung von einer Sesselform in die andere mit der unglaublichen Zahl von ca. 100 000 Mal pro Sekunde stattfindet. Die Moleküle schwingen also förmlich.
Sessel gibt es auch bei den Kohlehydraten
Diese Konfigurationen sind deshalb so wichtig, weil auch die Ringstrukturen der Einfachzucker
die gleiche Symmetrie aufweisen wie Cyclohexan. Schließlich liegt ja auch der Sauerstoff im Ring
sp3-hybridisiert vor. So unterscheiden sich die sechsatomigen Ringe (Pyranosen) verschiedener
Hexosen wie Glucose, Mannose, Fructose, Galactose usw. nur hinsichtlich der Axial- bzw. Äquatorial-Position
einiger OH-Gruppen. Das gilt auch für die Moleküle von a- und
b-Glucose. Sie unterscheiden sich nur in der Stellung der OH-Gruppe am
C-Atom 1: Bei der a-Glucose steht die OH-Gruppe axial, bei der
b-Glucose äquatorial.
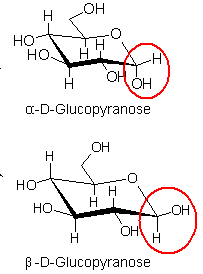
Auch diese Sesselformen können wie die des Cyclohexans in verschiedene Strukturen schwingen.
Weitere Texte zum Thema „Kohlenwasserstoffe“