 |
 |
 |
 |
| Kurze Fragen - Kurze Antworten
Aus dem E-Mail-Korb von Professor Blume |
1471
F: Ich würde Sie gerne fragen welche die effektivste Art und Weise ist mit Elektrolyse die
größte Ausbeute von Wasserstoff und Sauerstoff zu bekommen. Material, Aufbau ...
Ich habe schon einige versuche hinter mir, aber ich komme nicht ganz so recht dahinter.
A: Schade, dass Sie sich nicht vorstellen, sagen, was Sie sind und können und wofür
Sie das Info gebrauchen.
Der Begriff der „Effektivität“ ist auch klärungsbedürftig. Meinen Sie das im wirtschaftlichen Sinne oder hinsichtlich des chemischen Umsatzes (also des Faraday-Wirkungsgrads)?
Die chemisch effektivste Art der Wasserelektrolyse beruht auf vielen Komponenten, deren Zusammenspiel gründlich erprobt und dabei optimiert werden muss. Hier einige Beispiele:
1472
F: Wir hatten im Lk Chemie 13 die folgende Aufgabe gestellt: Ein gelbes und blaues T- Shirt
werden gleichmäßig mit Sonnenlicht bestrahlt. Welches T- Shirt erwärmt sich dabei stärker?
Unsere Überlegung war beim gelben T- Shirt werden Lichtwellen im Bereich blau (460 nm) absorbiert, das Restlicht als gelb wird
reflektiert.
Beim blauen T- Shirt genau umgekehrt, Lichtwellen im gelben Bereich (590 nm) absorbiert, Restlicht als blau wird reflektiert.
Es gilt: E = h x v ==> E = h x 1/Lambda, d.h. E ist indirekt proportional der Wellenlänge. Daraus schlussfolgerten wir, dass
das gelbe T- Shirt sich stärker erwärmt als das blaue T- Shirt.
Ein leistungsstarker Schüler des Kurses hat diese Logik widerlegt und kam zum genau umgekehrten Ergebnis. Er hat das Sonnenlicht polychromatisch richtig erfasst und in die Grundfarben rot, grün und blau als einstrahlende Lichtwellen aufgefasst. Beim blauen T- Shirt wird nach subtraktiver Farbmischung rote und grüne Lichtstrahlen absorbiert(als Mischfarbe ergibt sich daraus gelb) und das Restlicht als blaues Licht erfasst. Er hat aber jetzt für rotes und grünes Licht die Energien E (rot) und E (grün)errechnet und dann addiert und kommt somit zu einem anderen Ergebnis E(Gesamt).
Ich habe auch schon meine Chemiefachkollegen konsultiert ohne ein wissenschaftlich fundiertes Ergebnis. Auch unter den Physiklehrern wird sehr kontrovers mit großer Zurückhaltung diskutiert. Nach meiner Meinung kann man die überlagernden Lichtwellen nicht in diesem Fall nicht addieren, denn dann müsste gelbes Licht eine Wellenlänge über 1000 nm haben, was nicht stimmt, diese fast im Mittelwert bei 590 nm (Absorption).
Ich vermute, dass wir irgendwo einen Denkfehler haben oder eine Bedingung des Lichts falsch interpretieren. Ich hoffe ich habe mich Ihnen gegenüber verständlich ausgedrückt.
A: Erstens: Ihre folgende Äußerung ist nicht ganz exakt: “Es gilt: E = h x v ==>
E = h x 1/Lambda, d.h. E ist indirekt proportional der Wellenlänge.“
Richtig ist: n = c / l und E = h • c / l
Nun zur Absorption. Vordergründig sind Ihre Annahmen richtig:
- Wenn ein Stoff gelb aussieht, so absorbiert (subtrahiert) er aus dem weißen Licht den blauen Anteil. Der zurückgestrahlte Rest
addiert sich zu Gelb.
- Wenn ein Stoff blau aussieht, so absorbiert (subtrahiert) er aus dem weißen Licht den gelben Anteil. Der zurückgestrahlte Rest
addiert sich zu Blau.
Blaues Licht hat eine höhere Energie als gelbes. Nehmen wir an, dass die eingestrahlte Energie tatsächlich in Wärme umgewandelt wird, so sollte sich der gelbe Stoff mehr erwärmen.
Gehen wir einmal von einem Filter aus, der durchstrahlt wird. Da gibt es zwei Typen: Den Kantenfilter und den Bandenfilter.
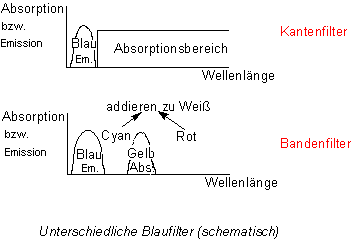
Der blaue Kantenfilter absorbiert alles Licht außer Blau. Hier haben wir nach dem Modell eine starke Aufheizung.
Der blaue Bandenfilter absorbiert nur im Bereich der Gelbbande. Die anderen Farbanteile addieren sich zu Weiß, also Blaugrün
(= Cyan) + Rot -> Weiß. Da Blau jedoch keinen komplementären Partner mehr hat (der heißt ja Gelb!), bleibt das Blau erhalten.
Hier haben wir eine schwache Aufheizung. (Zur Theorie dieser Farbmischungen haben wir eine Webseite.)
Gleiches kann man auch für eine Gruppe von Gelbfiltern „konstruieren“.
Ihre Argumentation und Berechnung basiert auf dem Bandenfilter, die Ihres Schülers auf dem Kantenfilter. Also haben Sie beide Recht. Auf keinen Fall jedoch dürfen Sie (wie Sie richtig anmerken) zur Energieberechnung die Wellenlängen addieren! Die Berechnung der Energie erfolgt nach
DE = h • c • D(1 / l)
1473
F: Meine Frage bezieht sich auf den fluoreszierenden Farbstoff Fluoreszein bzw. sein Salz
Uranin. Dieser Stoff traegt kein Gefahrensymbol und wird als biologisch unbedenklich eingestuft.
Ist es tragbar, Getraenke als Party-Gag an Halloween mit Uranin einzufaerben? Denn immerhin ist z. B. Tonic-Water chininhaltig und
dieser Stoff ist gesundheitsschaedlich eingestuft. Eignen sich eventuell noch andere fluoreszierende Farbstoffe zum Einfaerben von
Lebensmitteln?
Ich moechte nicht wissen, was Sie als Chemieprofessor dazu eigentlich sagen sollten, denn mir ist klar, dass man Nahrungsmittel
und Laborchemikalien besser getrennt lassen sollte.
Selbstverstaendlich bin ich allein fuer mein Handeln verantwortlich. Ich will mich nur bei jemandem vergewissern, der das Ganze
besser einschaetzen kann als ich.
A: Ich persönlich würde das nicht machen. Immerhin hat Fluorescein keine E-Nummer; es ist
also nicht als Lebensmittelzusatzstoff zugelassen. Das ist eigentlich erstaunlich, denn es werden schon einige Leute die gleiche Idee
gehabt haben wie Sie. Das Ganze ist wohl aber zu chemisch.
Zwar stimmt es, dass dieser Farbstoff in Lösung als gesundheitlich unbedenklich eingestuft worden ist. Mit ihm färbt man z. B.
Gewässer ein, um die Fließrichtung etwa durch Karsthöhlen festzustellen (wie bei der Donau geschehen). Oder man nutzt es in der
Augenheilkunde, zum Beispiel bei der Augendruckmessung. Auch beim Nierenfunktionstest wird der Stoff eingesetzt. Aber das heißt
nicht, dass der eine oder andere Mensch darauf anders reagiert, als es im Lehrbuch steht. Vor allem betrifft das Leute mit
Niereninsuffizienz. Bei denen bleibt der Farbstoff mehrere Tage im Körper. Was er dann anrichtet, ist allerdings nicht ganz
klar. Der Gedanke daran bringt jedoch manche Wissenschaftler zum Grübeln…
1474
F: Wir starten ein Projekt über Experimente zu Wilhelm-Busch-Geschichten und wollen mit
den Schülern Gallustinte herstellen und sie mit Vitamin C entfärben. Dies ist von der Versuchsdurchführung her keine Problem.
Ich habe nur zur Reaktion eine Frage: Läuft die Reaktion über die Reduktion von Eisen (III) zu Eisen (II) (durch Ascorbinsäure)
ab oder ist es eine Reaktion im Eisengallatkomplex?
A: Irgendwie stimmt Beides…: Denn es handelt sich um eine Reaktion zwischen Fe(III)
(allerdings im Gallat-Komplex gebunden) mit der Ascorbinsäure. Sie können das schematisch so beschreiben:
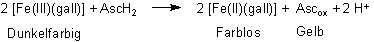
Auf jeden Fall ist nicht die Gallussäure am Redoxgeschehen beteiligt, denn sonst würde sich die Tinte ja auch so entfärben.
1475
F: Was sind Heparin und Hirudin?
A: Es handelt sich in beiden Fällen um natürliche Blutgerinnungshemmer. Ihr Wirkort in
der Blutgerinnungskaskade befindet sich dort, wo Thrombin aus Fibrinogen das Fibrin, das „verstopfende Prinzip“ des Bluts, freisetzt.
Thrombin wirkt dabei katalytisch.
Heparin und Hirudin sind Makromoleküle. Ihre Bausteine enthalten saure Reste, die im Rahmen der Blutgerinnungshemmung mit den basischen Gruppen ihrer Zielmoleküle reagieren und auf diese Weise Molekülkomplexe bilden können.
Heparin gehört zu den so genannten sauren Mucopolysacchariden, die neben Polysacchariden auch kleine Proteinanteile enthalten. Der saccharidische Teil des Makromoleküls setzt sich aus Glucuronsäure, Glucosamin, Schwefelsäure-Glucosamid (enthält eine Sulfonamidgruppe) sowie Schwefelsäureestern verschiedener anderer Zucker zusammen. Da auch das Glucosamin protoniert vorliegt, wirken alle Gruppen letztlich sauer.
Heparin wurde zunächst in der Leber gefunden (lat. hepar, Leber). Heute wird es mikrobiologisch hergestellt. Es verhindert die Umwandlung von Prothrombin in Thrombin. Wenn Thrombin bereits vorhanden ist, hemmt es stattdessen die Umwandlung von Fibrinogen zu Fibrin.
Im Körper wird Heparin enzymatisch abgebaut; das wirksame Enzym ist die Heparinase.
Hirudin stammt aus dem Speichel des Blutegels (lat. hirudo, Blutegel). Es handelt sich um ein Protein mit der
Molmasse um 10.000 u, das vorwiegend Reste von sauren Aminosäuren trägt.
Hirudin reagiert mit den alkalischen Gruppen des bei der Blutgerinnung katalytisch wirksamen Thrombins und inaktiviert es
auf diese Weise.