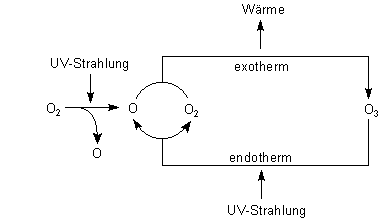
Vereinfachter stratosphärischer Ozonzyklus
Katalytische Ozonzerstörung in der Stratosphäre
Sauerstoff O2 und stratosphärisches Ozon O3 sind für unseren Planeten wichtig. Sie schützen uns vor starker Strahlung aus dem Weltall. Sauerstoff absorbiert vor allem harte Strahlung unter 215 nm, Ozon ist für die Absorption des längerwelligen UV-Bereichs "zuständig". Dabei hängen beide Mechanismen miteinander zusammen: Aus Sauerstoff bilden sich bei Bestrahlung zunächst O-Atome, die mit einem weiteren Sauerstoffmolekül Ozon bilden. Das Ozon seinerseits zerfällt bei Bestrahlung zurück in das O-Atom und ein O2-Molekül. Dabei wird die Strahlung in Wärme umgewandelt. Anschließend treffen sich O und O2 wieder unter exothermer Bildung eines O3-Moleküls.

Vereinfachter stratosphärischer Ozonzyklus
Heute ist der für uns segensreiche Mechanismus in Gefahr, weil Substanzen auftauchen, die die Reaktionen stören. Hierzu gehören die Chlorradikale, die u. a. aus den FCKW stammen. Aber zunächst einmal kann Ozon ohne Fremdbeteiligung abgebaut werden, indem es sich in exothermer Stoßreaktion mit einem Sauerstoffatom, das eigentlich ein anderes Ozonmolekül bilden sollte, quasi selbst zerstört.
O3 + O ———> 2 O2 + Energie
Das ist eine verhältnismäßig seltene, aber mögliche Reaktion.
Viel häufiger ist die Mitwirkung von Katalysatoren. Diese sind allesamt Radikale. Beispiele sind Stickstoffmonoxid NO· aus der Gruppe der NOx, das Wasserstoffradikal H·, das Hydroxyl OH·, das Chlorradikal Cl· und das Chloroxoradikal ClO·. Letztere werden beim fotochemischen Abbau der FCKW gebildet.
Bleiben wir beim wichtigen Beispiel des Chloroxoradikals ClO·. Es reagiert anstelle des Ozons mit einem Sauerstoffatom. Daraus bildet sich das Chlorradikal Cl· und ein Sauerstoffmolekül. Durch eine weitere Reaktion mit Ozon (wobei dieses zerstört wird) lädt sich das Chlorradikalsystem wieder auf. Damit schließt sich der Kreis der Katalysereaktion, und sie kann erneut beginnen.
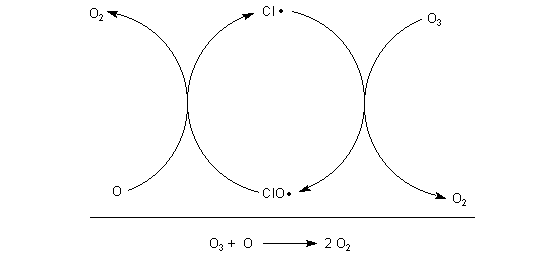
Die Bruttoreaktion entspricht der obigen Reaktionsgleichung. Insgesamt werden auf diese Art und Weise zwei Ozonmoleküle zerstört bzw. in ihrer Bildung behindert.
Die Reaktion kann aber auch so ablaufen:
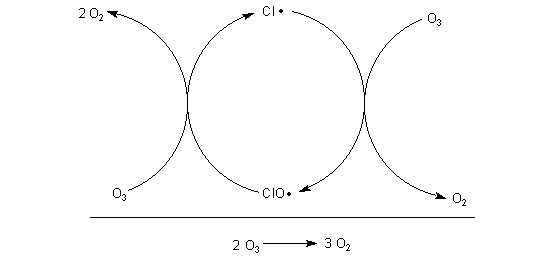
Mit einem Durchlauf des Kreisprozesses werden zwei Ozonmoleküle abgebaut.
Es ist aber (wie immer) alles viel komplizierter
Die obigen Reaktionen sind exotherm und können deshalb auch im Dunkeln ablaufen. Wir wissen
aber, dass der bedeutendste Ozonabbau im Hellen abläuft.
Wieder sind die Chlorradikale die bösen Buben. Bei Bestrahlung mit sichtbarem Licht (VIS) und UV setzen sie einen katastrophalen Katalysekreisprozess in Gang. Das zeigt das folgende Reaktionsschema. Dabei wird die Rolle des Lichts und der UV-Strahlung deutlich.
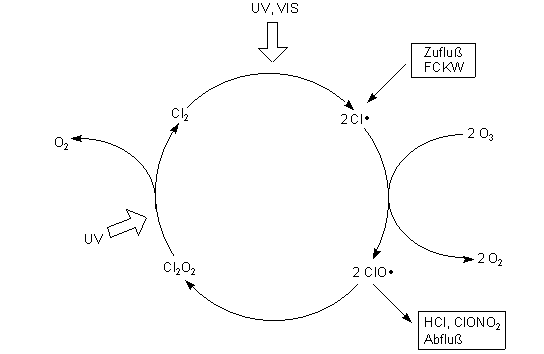
Stratosphärische Zerstörung von Ozon durch Chlor-Katalyse
Man kann den Reaktionsmechanismus auch so formulieren:
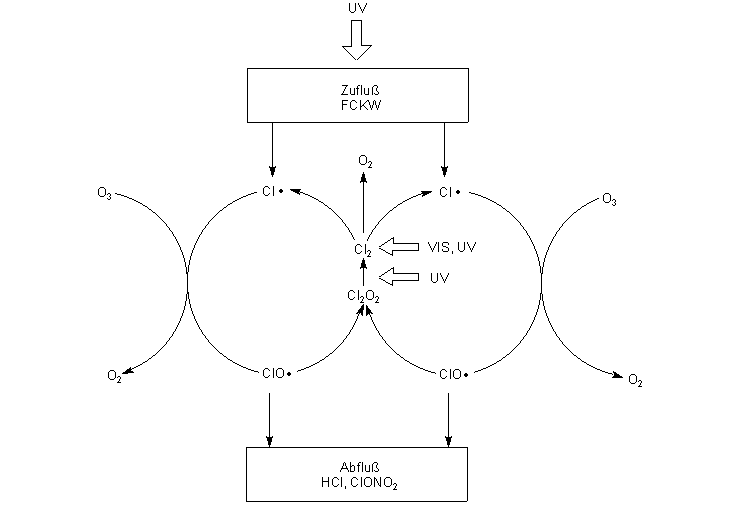
Aufgrund der Verzweigung ergibt sich eine viel höhere Abbaurate für Ozon durch Chlorradikale, als wir nach den oben formulierten, einfachen Reaktionsmechanismen erwarten sollten. Hinzu kommt noch das hier nicht berücksichtigte „Schlucken" von O-Atomen, den "Babies" der O3-Bildung, durch die Chlor(oxo)radikale.
Ein Chloratom setzt deshalb auf diese Art und Weise über 1 Million Ozon-Moleküle um. Bemerkenswert ist der ständige Zu- und Abfluss des Chlorpools.
Das ist ein Beispiel für eine homogene Katalyse, und zwar in der Gasphase. Solche Katalyseprozesse sind typisch für die Atmosphärenchemie.
Genaueres dazu findet man in unserer Webseite zum stratosphärischen Ozonabbau.
Weitere Texte zum Thema „Ozon“