|
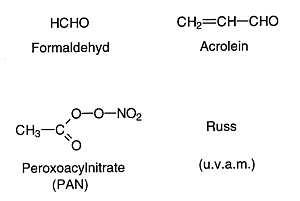
| Bild 1: Typische Schadstoffe im Photosmog |
Photosmog und bodennahe Ozonbildung
Experimente:
Versuch: Abbau von Ozon durch Benzinbestandteile
| Eine täglich aktualisierte Karte von Deutschland mit den maximalen troposphärischen Ozonwerten gibt das Umweltbundesamt http://www.umweltbundesamt.de heraus. Dazu klickt man an: Graphische Versionen/Daten und Fakten/Themengebiete/ Ozondaten:... |
Bei schönem und austauscharmen Hochdruckwetter erhält man einen atmosphärischen Zustand, den man als Photosmog bezeichnet. Photo(chemischer) Smog entsteht, wenn katalytische Mengen von Stickoxiden mit CO oder Kohlenwasserstoffen intensiver Sonnenstrahlung ausgesetzt werden. Dabei bilden sich Photooxidantien (Bild 1) und stark oxidierende Stoffe wie Ozon und Radikale. Diese Schadstoffe sind schleimhautreizend und können Asthma auslösen.

|
| Bild 1: Typische Schadstoffe im Photosmog |
Letztlich entstehen durch Crackprozesse Rußteilchen, die die Luft bräunlich trüben.
 |
| Bild 2: Photosmog über Moskau
(Foto: Blume) |
Hier liegt wohl auch ein Grund für die zunehmenden Pollenallergien: Pollen lagern die Rußteilchen an, wodurch
die Verweildauer in Lunge und auf Schleimhäuten verlängert wird und die allergene Wirkung voll greifen kann.
|
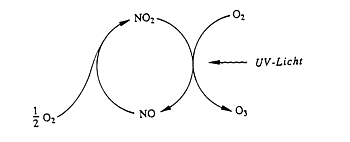
| Bild 3: Ozonbildung aus Stickoxiden und Sauerstoff |
Grundlage des Entstehens von Photosmog ist die bekannte Tatsache, dass Stickoxide mit Sauerstoff unter UV-Bestrahlung
Ozon bilden können (Bild 3). Wenn die UV-Strahlung wegfällt, laufen die Reaktionen in Richtung auf Ozon-Abbau ab. Dabei bilden sich
Gleichgewichtszustände aus, die Ozonbelastung bleibt deshalb insgesamt gering. Stickstoffmonooxid baut Ozon sogar ständig
wieder ab, während Stickstoffdioxid ozonaufbauend wirkt und dabei verbraucht wird.
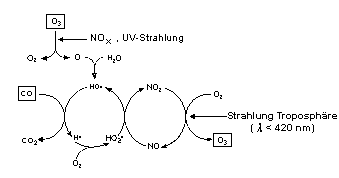
Allerdings wird diese Fotoreaktion durch Quellgase wie CO, Aldehyde sowie Kohlenwasserstoffe beschleunigt. Denn deren Oxidation ist durch zwei katalytische Kreisprozesse mit der Ozonbildung gekoppelt. Dabei wird die Konzentration von Stickstoffdioxid ständig auf hohem Niveau gehalten, und die Ozonkonzentration nimmt entsprechend stark zu. Bild 4 zeigt diesen Zusammenhang.
|
| Bild 4: Katalytische Kreisprozesse |
HO•-Radikale (Normale Konzentration: 1 Radikal auf 1018 Luftmoleküle) geben ihr Sauerstoffatom an Kohlenmonoxid
ab, wobei ein Wasserstoffradikal H• zurückbleibt. Mit Sauerstoffmolekülen bilden sich Hydroperoxidradikale HO2•,
die NO zu NO2 oxidieren. Unter Einwirkung von kurzwelligerem Licht (Wellenlängen <420 nm) oder bei hohen Sommertemperaturen
reagiert NO2 mit weiteren Sauerstoffmolekülen zu Ozon, das nun in Bodennähe seine umweltschädigenden Wirkungen ausüben kann.
Man kann diese bodennahe Ozonbildung somit durch die Minderung der Schadstoffemission (etwa durch großräumiges, langfristiges Autofahrverbot) drastisch einschränken. Hinzu kommt, dass die bodennahe Ozonbildung durch die Ausdünnung der Ozonosphäre verstärkt wird.
Die Ozonanreicherung hat aber auch schon die Alpen und andere Reinluftgebiete erreicht. (Siehe hierzu das Themengebiet Ozondaten: Jahresmittelwerte des Umweltbundesamtes.) http://www.umweltbundesamt.de
Der Grund ist, dass sich in der Nacht wegen des Fehlens von UV-Strahlung die umgekehrten Reaktionen bemerkbar machen: NOX und Kohlenwasserstoffe bauen die Ozonmoleküle ab und machen sie unschädlich (siehe Experimente, V 18). Da aber in Reinluftgebieten, anders als in Ballungszentren, der verkehrsbedingte NOX- sowie Kohlenwasserstoff-Ausstoß abends zum Erliegen kommt, entfällt die Entgiftung, so dass die Ozonkonzentration konstant hoch bleibt. So betrug 1990 die Ozonkonzentration in Hamburg 184 µg/m2 Luft, in Bad Tölz 308 µg.
Dass der Ozonwert für das Ballungszentrum geringer ist als für das Reinluftgebiet, liegt weiter nur zum Teil daran, dass Bad Tölz höher liegt. In Hamburg ist die Stadtatmosphäre durch Staub und Ruß derartig verschmutzt, dass weniger UV-Strahlung die bodennahe Luftschicht erreicht und die Ozonbildung somit reduziert wird.
Was chemisch dahinter steckt:
Es handelt sich hier um katalysierte Reaktionen in der Gasphase. Denn nicht nur feste oder gelöste Substanzen,
sondern auch Gase können Katalysatoren sein. Bei eingehender Betrachtung stellt man fest, dass z. B. Stickoxide und letztlich
auch die OH-Radikale gerade deswegen in so kleinen Konzentrationen wirken, weil sie Katalysatoren sind. Bei dem Beispiel der mit
der CO-Oxidation gekoppelten bodennahen Ozonbildung handelt es sich sogar um zwei miteinander gekoppelte Katalysekreisprozesse.
Warum gibt es bodennahes Ozon vor allem bei Hochdruckwetter?
Das hängt mit den Vorgängen in der Atmosphäre zusammen. Erinnern wir uns daran: Auslöser der Ozonbildung sind unter
anderem die Hydroxyl-Radikale, die in der Stratosphäre gebildet werden. Als unverzichtbare "Mitarbeiter" müssen sie zum
Boden gelangen.
Um zu verstehen wie das geht, betrachten wir das Entstehen von atmosphärischen Tiefs und Hochs. Denn durch ihre
Wechselbeziehung wird der Kontakt zwischen Stratosphäre und bodennaher Troposphäre ermöglicht und aufrechterhalten.
Zunächst das Tief
Heiße Luft steigt lokal wie ein heißer Ballon auf, damit sinkt der Luftdruck am Boden, es entsteht ein Tief. Die heiße Luft
ist mit Wasserdampf gesättigt, daher beobachtet man aufgrund der Abkühlung Wolkenbildung und sogar Regen. In der Stratosphäre
angelangt, wird die Luft durch Querwinde verfrachtet. Sie kühlt noch stärker ab, wird dabei dichter, also schwerer und sinkt ab.
Und nun zum Hoch
Im Sinkgebiet der kalten Luft aus der Stratosphäre steigt am Boden der Luftdruck; ein Hoch entsteht. Dabei erwärmt sich die
Luft (wie die komprimierte Luft in der Fahrradluftpumpe) adiabatisch. Wolken bilden sich nicht oder nur wenig, weil die Luft
trocken ist und außerdem immer wärmer wird. Die Sonne kann deshalb gut scheinen. Beim Absinken der Luft, die aus der Stratosphäre
stammt, werden Ozon und Hydroxyl-Radikale mitgeschleppt. Damit bietet das Hochdruckgebiet alle Voraussetzungen zur Bildung von
bodennahem Ozon.
Weitere Texte zum Thema „Ozon“