Prof. Blumes Bildungsserver für Chemie
Tipp des Monats September 2016 (Tipp-Nr. 231)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
K.o.-Tropfen chemisch betrachtet
Jens Schorn
„Man kann sie nicht sehen, nicht riechen und nicht schmecken. Das macht sie so gefährlich: K.-o.-Tropfen. Immer wieder gelingt es Tätern ganz unbemerkt, sie in die Gläser ihrer Opfer zu träufeln. Meistens sind es junge Frauen. Sie werden durch die gefährliche Flüssigkeit förmlich ausgeknockt. Die K.o.-Tropfen machen sie schwach, sie werden unfähig sich zu wehren.“[1] Bei sogenannten Knock out Tropfen handelt es sich um eine Vielzahl narkotisierend wirkender Stoffe unterschiedlicher Stoffgruppen. Insgesamt existieren über 100 verschiedene Wirkstoffe, die als „K.-o.-Mittel“ eingesetzt werden.
Der Erwerb und der Gebrauch von Benzodiazepinen, Antihistaminika und Neuroleptika sowie auch von Gamma-Hydroxybuttersäure (GHB) werden in Deutschland eindeutig nach dem Arzneimittelgesetz oder dem Betäubungsmittelgesetz geregelt.
Abb. 1: Struktur von 1,4-Butandiol (1), Gamma-Butyrolacton Das Butandiol mit seinen beiden Hydroxylgruppen wird als Diol für die Kunststoffherstellung z.B. für Polyester oder für Polyamide verwendet. Siehe auch: Kunststoffe Butyrolacton ist als interner Ester ein hervorragendes Lösemittel für die Entfernung von Farben, Graffiti und Lacken. Außerdem wird es als Weichmacher in Weich-PVC Folien eingesetzt.
Mit diesen Eigenschaften sind die beiden Stoffe für die chemische Industrie unersetzlich und fallen aus diesem Grund nicht unter das Betäubungsmittelgesetz. Beide Stoffe gelten als sogenannte Prodrugs zur Herstellung von Gamma-Hydroxybuttersäure und werden im Handel und beim Inverkehrbringen einer starken Kontrolle mittels Endverbleibserklärung gegenüber dem Lieferanten sowie einer stärkeren Beobachtung durch den Zoll unterzogen. Abb. 2: Oxidation von 1,4 Butandiol (1) zu 4-Hydroxybutyraldehyd (2) Anschließend bewirkt die Aldehyddehydrogenase (ALDH) die weitere Oxidation zu Gamma-Hydroxybuttersäure (GHB). Abb. 3: Oxidation von 4-Hydroxybutyraldehyd (3) zu Gamma-Hydroxybuttersäure (4) Die hier gebildete Gamma-Hydrxoybuttersäure (GHB) kann aber auch aus dem oben beschriebenen Gamma-Butyrolacton im Körper entstehen, wenn es missbräuchlich aufgenommen wird. Das Lacton wird durch seine gute Fettlöslichkeit schon im Mund resorbiert und gelangt sehr schnell in das menschliche Blut, sodass der Plasmaspiegel schneller ansteigt als bei der direkten Aufnahme von Gamma-Hydroxybuttersäure. Im Blut wird der innere Ester Gamma-Butyrolacton durch 1,4-Lactonase zu Gamma-Hydroxybuttersäure hydrolysiert. Abb. 4: Hydrolyse von Gamma-Butyrolacton (5) zu Gamma-Hydroxybuttersäure (6) Aus beiden Prodrugs wird also letztlich Gamma-Hydroxybuttersäure (GHB), die dann mit Hilfe von einer Transaminase zu Gamma-Aminobuttersäure (GABA) umgewandelt wird. GABA ist der wichtigste hemmende Neurotransmitter im Zentralnervensystem und entfaltet dementsprechend seine narkotisierende Wirkung. Experiment 1: Nachweis von 1,4-Butandiol mit Cerammoniumnitrat-Reagenz.
Mit Cerammoniumnitrat-Reagenz kann 1,4-Butandiol als Alkohol einfach nachgewiesen werden. Benötigt werden nur geringe Mengen des Alkohols. Man achte genau auf die Ansäuerung des Alkohols mit 12%iger Salpetersäure. Bild 1: Nachweis mit Cerammoniumnitrat
Bild 2: Positiver Nachweis von Hydroxylgruppen
Die rotorange Färbung zeigt die Hydroxylgruppe an. Es entsteht in etwa die folgende Zusammensetzung als Komplex. Bei der Verwendung von Buttersäure tritt diese Verfärbung nicht auf. Die Lösung bleibt gelblich, wie die salpetersaure Ausgangslösung. Experiment 2: Oxidation von 1,4-Butandiol mit Hilfe von Cer (IV)-Ionen.
Zum Vergleich werden je 2ml 1,4-Butandiol bzw. Ethanol mit Cerammoniumnitrat- versetzt. Hierbei darf keine Salpetersäure zugesetzt werden, da sie sonst später die pH-Wert Bestimmung beeinflussen würde. Anschließend lässt man beide Gemische bei Raumtemperatur stehen. Bild 3: Nachweis der unterschiedlich schnellen Oxidationsvorgänge bei 1,4-Butandiol (links) und Ethanol (rechts)
Die Entfärbung findet beim Diol schneller statt als beim Ethanol. In beiden Fällen findet eine Oxidation der Alkohole zum Aldehyd statt. Die Cer(IV)-Ionen werden hierbei zu Cer(III)-Ionen reduziert und oxidieren die Hydroxylgruppen zum Aldehyd oder sogar zur Carbonsäure. Bei einem Diol geht dieser Vorgang schneller, da hier bei volumenäquivalenten Mengen pro Molekül zwei Hydroxylgruppen oxidiert werden. Experiment 3: Nachweis von Oxidationsprodukten.
a) Anhand der pH-Wert Bestimmung
Bild 4: Nachweis der Carboxylgruppe durch pH-Wertmessung
Zu den Stoffen gehören Benzodiazepine, Antihistaminika, Neuroleptika aber auch die Stoffe Gamma-Hydroxybuttersäure (GHB) und deren intramolekularer Ester Gamma-Butyrolacton sowie auch das 1,4-Butandiol. Die Silbe Gamma steht hierbei für die Tatsache, dass sich an dem dritten -CH2-Kettenglied einer organischen Substanz, hier von der Carboxylgruppe aus betrachtete, eine weitere funktionelle Gruppe befindet. So könnte man das 1,4-Butandiol auch Gamma-Hydroxybutan-1-ol nennen.
1,4-Butandiol und Gamma-Butyrolacton unterliegen diesen Regelungen nicht.
Warum sind der Vertrieb und die Verwendung von 1,4-Butandiol und Gamma-Butyrolacton nicht gleichermaßen wie für andere „K.-o.-Tropfen“ geregelt?
Betrachtet man die Struktur der beiden Stoffe, so offenbaren sich dem geneigten Leser neben dem Einsatz als „K.-o-. Tropfen“ weitere Verwendungsmöglichkeiten.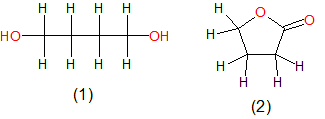
Auch findet Butyrolacton sehr verbreiteten Einsatz als Felgenreiniger und führte in der Vergangenheit in Missbrauchsfällen, in denen Felgenreiniger zum Zwecke des Berauschens getrunken wurde, zu Todesopfern. [2]
Wie stehen diese drei Stoffe chemisch im Zusammenhang?
Im Magen und in der Leber findet die Oxidation von 1,4-Butandiol zu 4-Hydroxybutyraldehyd durch das Enzym Alkoholdehydrogenase (ADH) statt. Es handelt sich hierbei um eine gestufte Oxidation eines primären Alkohols.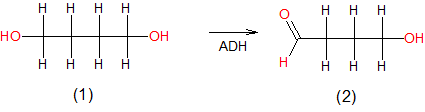
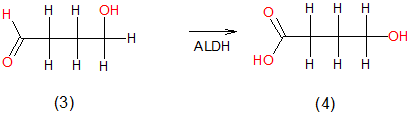
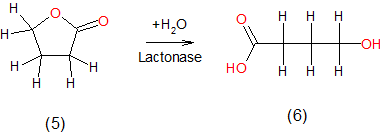
Wie kann man diese Vorgänge im Reagenzglas nachvollziehen?
Man nutzt den Nachweis lt. Tipp Nr. 1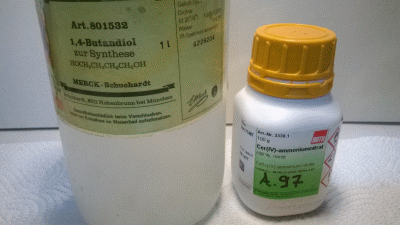
(Foto: J. Schorn)
(Foto: J. Schorn)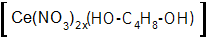
Man nutzt hier die oxidierende Wirkung von Cer(IV)-Ionen lt. Tipp Nr. 1
(Foto: J. Schorn)
Zum Nachweis der Entstehung von Carbonsäuren wird mit Hilfe von Unisol 113 Indikatorlösung der pH-Wert bestimmt. Hierzu gibt man 2 Tropfen Indikatorlösung in die vorliegenden Lösungen.
(Foto: J. Schorn)
Substanz
pH-Wert
Leitungswasser
7
Buttersäure
2
Oxidationsprodukte von 1,4-Butandiol
2
1,4-Butandiol
5
Der pH-Wert von 2 für die Oxidationsprodukte von 1,4-Butandiol zeigt die Entstehung von Carboxylgruppen an.
b) Drogentest auf Gamma-Butyrolacton und Gamma-Hydroxybuttersäure und deren Derivate
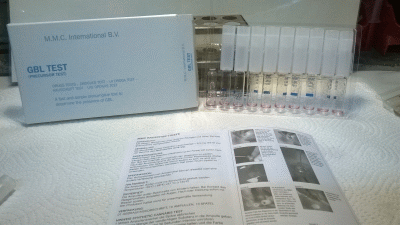
Bild 5: GBL Test Set
(Foto: J. Schorn)
Einschlägige Firmen [3],[4] bieten sogenannte Schnelltests für Drogen an. Zwei Tests zum Nachweis von Gamma-Butyrolacton und Gamma-Hydroxybuttersäure kommen hier zum Einsatz. Die fertig gelieferten Ampullen werden geöffnet und die verdächtige Substanz mit dem mitgelieferten Minispatel in jeweils eine Ampulle gegeben. Das Gemisch der Oxidationsprodukte wird in die beiden Ampullen geben, umgerührt und 30 Sekunden laut Anleitung gewartet.

Bild 6: Nachweis von Derivaten der Gamma-Hydroxybuttersäure.
Links: Oxidationsprodukte von 1,4-Butandiol
Mitte: GBL Test mit zugesetztem Oxidationsgemisch von 1,4-Butandiol
Rechts: GHB Test mit zugesetztem Oxidationsgemisch von 1,4-Butandiol
(Foto: J. Schorn)
Nur der Nachweis auf Derivate der Gamma-Hydroxybuttersäure (GHB) fällt positiv aus. Dies kann man an der rostbraunen Färbung erkennen. Der Nachweis auf Gamma-Butyrolacton ist negativ.
c) Fehlingprobe
Hier wird die Fehlingsche Probe nach gültiger Anleitung für die reduzierende Wirkung von Glukose angewendet. Nachweis von Glucose mit Fehling-Reagenz
In jeweils ein Reagenzglas wird 1,4-Butandiol bzw. das Gemisch der Oxidationsprodukte von 1,4-Butandiol geben. Anschließend erfolgt die Zugabe von Fehling I und Fehling II. Beide Ansätze werden mit dem Brenner vorsichtig erhitzt.

Bild 7: Schwach positiver Nachweis von Aldehydanteilen im Reaktionsgemisch (links)
(Foto: J. Schorn)
Mit diesen einfachen Nachweisen lassen sich die Oxidationsvorgänge vom 1,4-Butandiol über das Hydroxybutyraldehyd bis zur Buttersäure im Reagenzglas nachvollziehen. Während im menschlichen Körper die Alkoholdehydrogenase und die Aldehyddehydrogenase die oxidativen Vorgänge steuern, dient im Reagenzglas das Cer(IV)-Ion als Oxidationsmittel.
Literatur:
[1] http://www.swr.de/swrinfo/gefahr-k-urlaubsfeeling-feierlaune-und-dann-filmriss/-/id=7612/did=17849112/nid=7612/1vcvyey/
[2] http://www.ndr.de/nachrichten/niedersachsen/osnabrueck_emsland/Drogen-Experiment-mit-Felgenreiniger-war-geplant,felgenreiniger100.html
[3] https://www.self-diagnostics.com/de/substanztest-gamma-hydroxybuttersaeure-ghb.html?gclid=CLaWsez1zM0CFTUo0wodVNQGRw
[4] https://www.self-diagnostics.com/de/substanztest-gammabutyrolaceton-gbl-10-ampullen.html
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 30. August 2016, Fritz Meiners