Prof. Blumes Bildungsserver für Chemie
Tipp des Monats März 2019 (Tipp-Nr. 261)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Algebra und Chemie: Mischungsrechnen
Rüdiger Blume
(Foto: Lüttgens) In der Chemie muss immer wieder mal gerechnet werden. Klassisch unbeliebt sind stöchiometrische Berechnungen. Aber immer wieder erreichen uns auch Anfragen zur Berechnung von Mischungen und Verdünnungen. Das hat seinen guten Grund: Viele Probleme bei chemischen Laborarbeiten beruhen schlicht auf Verdünnungsfehlern. Zunächst geht es um eher semantische Probleme: Wie nennt man eine Mischung aus "50 mL Lösung A und 50 mL Lösung B"? Ich bin der Meinung: "1:2" bzw. "1+1", mein Chef ist der Meinung "1:1".

Es geht hier um das kleine Wörtchen „zu“. Entweder ist es ein Wort, das ein Verhältnis ausdrückt, also 1:2. Oder es geht um eine „Zu“gabe, also ein Liter Lösung zu einem weiteren Liter. (Das erinnert ein wenig an Probleme mit der Uhrzeit: So ist „Viertel Zwölf“ nicht gleich „Viertel vor Zwölf“…)
Einen Teil A und einen Teil B zusammenzugeben bedeutet 1:1 mischen; die Verdünnung ist dann 1/(1+1) = 1/2. Das ist der Verdünnungsfaktor. Eine Mischung im Verhältnis 1:1 gibt also eine Verdünnung von 1:2. Dann hat man z. B. eine 1molare Lösung zu einer 1/2molaren verdünnt.
Anders dagegen: Im Verhältnis 1:2 mischen bedeutet eine Mischung, die zu 1/3 Teil aus A und 2/3 Teilen aus B besteht. Der Chef liegt also richtig.
Grundsätzlich gilt aber: Um Missverständnissen von vornherein zu vermeiden, sind präzise Anleitungen hilfreich.
Andere Fragen betreffen praktische Anwendungen:
|
Ein Aquariumsbesitzer benötigt Wasserstoffperoxidlösungen für seinen Oxidator. Die Lösungen gibt es zu 3 oder 6 % oder 30 % zu kaufen. Der Tierfreund stellt fest, dass alle Sorten den gleichen Liter-Preis haben. Da er nicht unnötig Geld ausgeben will, hat er überlegt, ob er nicht die 30%ige Lösung mit destilliertem Wasser auf 6 % verdünnen kann. |
Zur Berechnung kann man zunächst den klassischen Dreisatz mit einer Unbekannten anwenden:
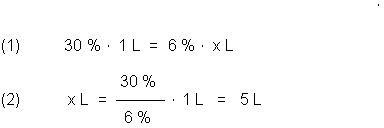
Achtung! Um zu berechnen, wieviel Wasser zu einem Liter H2O2 zuzugeben sind, muss man in diesem Fall von den fünf Litern einen Liter abziehen. Der Tierfreund muss also die 30%ige Lösung mit 4 Liter Wasser verdünnen. (Zur direkten Berechnung der zuzugebenden Lösemittel-Menge siehe weiter unten.)
Nun kann man auch das folgende, komplizierter klingende Problem angehen:
|
Ich habe eine 80%ige Milchsäure - brauche aber eine 15%ige. Wie berechne ich das Mischungsverhältnis? Z. B. für 1 Liter 15%iger Mischung? |
Die Rechnung ist:
80 % · x mL = 15 % · 1000 mL
x = 187,5 mL
Man muss somit 187,5 mL der 80%igen Milchsäure mit Wasser auf 1 Liter auffüllen. Anders formuliert: Die Zugabe an Wasser beträgt 812,5 mL. Praktisch macht man das, indem man 187,5 mL Milchsäurelösung in einen 1 L-Maßkolben gibt und diesen mit Wasser auf 1 L auffüllt. (Zur direkten Berechnung der zuzugebenden Lösemittel-Menge siehe auch in diesem Fall im Text weiter unten.)
Aus dem Dreisatz (1) kann man eine einfache mathematische Formel zur Berechnung von Mischungen herleiten
In den folgenden Gleichungen stehen C für Konzentration und V für Volumen. Statt H2O2 schreiben wir das allgemeine Stoffsymbol A. Der Sub-Index Null bezeichnet den Zustand der Lösung vor dem Mischen, der Sub-Index Mi danach. Der Sub-Index Zugabe bezieht sich auf die zuzugebende Lösungsmittel-Menge.
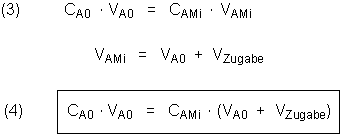
Durch algebraische Umstellung kann man mit dieser Gleichung zweierlei berechnen:
A. Konzentration von A nach der Verdünnung
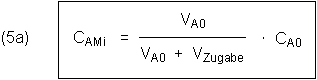
B. Erforderliche Zugabe an Lösemittel, um eine gewünschte Konzentration von A zu erhalten
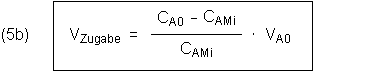
1. Wir prüfen die Gleichungen (5a, b) mit dem Beispiel der Verdünnung von 30%iger H2O2-Lösung nach:
Gleichung (5a): CAMi = [1 / (1 + 4)] · 30 = 6 %
Gleichung (5b): VZugabe = [(30 – 6) / 6] · 1 = 4 L
2. Etwas komplizierter ist es beim Beispiel der Milchsäureverdünnung. Zur Vereinfachung benennen wir den Konzentrationsfaktor (CA0 – CAMi)/CAMi in Gleichung (5b) mit f.
(5c) VZugabe = f · VA0
Wir setzen die Randbedingung VA0 + VZugabe = 1000 ein und stellen die resultierende Gleichung so um, dass VZugabe isoliert wird:
(5d) VZugabe = [f / (1+f)] · 1000
Mit CA0 = 80 % und CAMi = 15 % erhalten wir f = 4,333. Eingesetzt in (5d) folgt für die Zugabe an Wasser 812,5 mL. (Zur Erinnerung: In der ersten Berechnung oben erhielten wir 187,5 mL – allerdings für die Menge an 80%iger Milchsäure, die auf einen Liter Lösung aufgefüllt werden sollte: 187,5 mL + 812,5 mL = 1000 mL.)
Ähnliche Gleichungen kann man auch anwenden, um Mischungen aus zwei unterschiedlich konzentrierten Lösungen eines Stoffes zu berechnen
Dann lautet die Gleichung (5a):
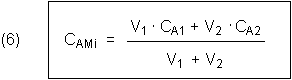
CMi ist die Mischungskonzentration. Die Sub-Indices 1 und 2 beschreiben die beiden Lösungen. Dies ist die Allgemeine Mischungsformel, die auch das Verdünnen mit reinem Lösemittel einschließt: Dazu setzt man in Gl. (6) den Term V2 · CA2 gleich Null. Dann hat man wieder einen Ausdruck, der der Gleichung (5a) entspricht.
Zum Überprüfen der Gleichungen sollte man Beispiele wählen, die man auch im Kopf ausrechnen kann. Z. B. mische man 0,5 L einer Lösung mit CA1 = 1 mol/L mit 0,5 L einer Lösung mit CA2 = 2 mol/L:
CAMi = (0,5 · 1 + 0,5 · 2) / (0,5 + 0,5) = 1,5 mol/L
Mit der Mischungsgleichung (6) kann man auch andere Mischungen untersuchen
Als Beispiel aus der Physik bietet sich das Mischen von kaltem und warmem Wasser an. Anstelle des Volumens verwenden wir hier die Massen m der unterschiedlich warmen Wasser-Proben. Deshalb können wir auch das Mischen von flüssigem Wasser mit Eis untersuchen.
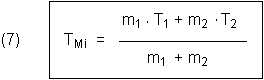
Noch eine Anmerkung:
Manche Leute schwören auf das Mischungskreuz. Das ist erfahrungsgemäß für Schüler viel schwieriger zu händeln als die oben diskutierten Formeln. Normalerweise reichen sogar die Gleichungen (5a) und (5b). Denn meistens geht es im Chemieunterricht bei Mischungen nur um das Verdünnen von Lösungen einer Substanz mit dem reinen Lösemittel.
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 26. Februar 2019, Fritz Meiners