Prof. Blumes Bildungsserver für Chemie
Tipp des Monats August 2021 (Tipp-Nr. 290)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Uwe Lüttgens
Sommerzeit – Ferienzeit. Unsere diesjährige Urlaubsreise führte uns nach Schweden bis an die norwegische Grenze, durch eine wunderschöne Landschaft mit Wäldern und ungezählten kleineren und größeren Seen. Ein Traum! Bild 1: Camping an einem der unzähligen schwedischen Seen.
Ein Traum, der jedoch schnell zum Alptraum werden kann, wenn in den Morgen- und Abendstunden die für die skandinavischen Länder berüchtigten Mücken auf ihre Blutjagd gehen. Denn Sommerzeit ist auch Mückenzeit! Bild 2: Eine Mücke hat mich entdeckt und möchte nur zu gern zustechen.
Egal, wenn man fragt, man erhält immer unterschiedliche Meinungen zur Wirksamkeit der verschiedenen Repellents: „Nimm´ dies, das Mittel hat bei mir immer geholfen. Wenigstens für ein paar Stunden.“ „Dieses Mittel brauchst du erst gar nicht versuchen, es hilft nicht! Nimm lieber jenen Wirkstoff, der hilft auf jeden Fall. Das habe ich in vielen Urlauben erprobt.“ „Keines von diesen Stoffen zur Mückenabwehr hilft wirklich, man muss die Mückenstiche einfach ertragen. Irgendwann merkt man´s nicht mehr.“ Diese drei Äußerungen mögen exemplarisch die unklare Datenlage wiedergeben, die ich vor unserem Urlaub gewonnen habe. Probieren Sie es aus. Es scheint so zu sein: Nichts Genaues weiß man nicht. Schließlich habe ich selbst zwei dieser Repellents ausprobiert, mit unterschiedlichem und nicht sehr lang anhaltendem Erfolg. Klick mich an! Bild 3: Der Unterleib füllt sich sichtbar mit Blut, nachdem das Mückenweibchen zugestochen hat.
Genauer: Damit die Eier wachsen und gedeihen können, sind Proteine wie das Hämoglobin oder Albumin notwendig sowie Eisen, das sich als zentrales Atom in der Hämgruppe des Hämoglobins befindet. Die Mücke reagiert auf Kohlenstoffdioxid, das jedes Tier und auch der Mensch ausatmen. Anlockend wirkt auch die von Säugetieren ausgehende Duftfahne, eine Komposition unterschiedlicher Ausdünstungen. Besonders anziehend für die Mücke wirken dabei Milchsäure und Ammoniak. Einmal chemisch angelockt steuern die Mückenweibchen zielsicher ihren Wirt an. Auch die kleinste freie Hautstelle bleibt nicht unentdeckt. Auch eine dünne Hose oder Jacke hält die Blutsauger nicht von einem Stich ab – es geht schließlich um das Überleben der eigenen Brut. Mit ihrem Stechrüssel, der aus zwei Kanälen besteht, durchbohren die Mücken die Haut. Durch den einen Kanal wird giftgetränkter Speichel injiziert – dieser erzeugt den Juckreiz –, durch den anderen wird das Blut abgesaugt. Körpereigenes Histamin, das dabei ausgestoßen wird, erzeugt eine Quaddel auf der Haut. Bild 4: Die für einen Mückenstich typischen Quaddeln entstehen durch Histamin, das beim Mückenstich vom Körper freigesetzt wird.
Bild 5: Inhaltsstoffe von zwei gebräuchlichen Repellents gegen Mücken, die ich auf unserer Urlaubsreise getestet habe.
Bild 6: Ein Insektenstecker, der in geschlossenen Räumen gegen Mücken helfen soll.
Drei Mechanismen für die Wirkung von Repellents werden als wahrscheinliche Hypothesen diskutiert: Bild 7: Struktur von Cuban, ein Kohlenwasserstoff, der chemisch korrekt bezeichnet Pentacyclo[4.2.0.02,5.03,8.04,7]octan heißt. Nach diesem Exkurs wieder zurück zu den Repellents. Icaridin und Prallethrin sind solche Trivialnamen, mehr oder weniger kunstvolle Worte, aus denen sich keine strukturellen chemischen Merkmale erschließen lassen. Dazu würden wir jeweils den sogenannten systematischen Namen benötigen, der von einer Behörde verbindlich aufgestellt wird. Diese heißt IUPAC, was für International Union of Pure and Applied Chemistry steht. Das möglicherweise noch immer effektivste Repellent DEET wurde 1942 von der US-Amerikanischen Agrarbehörde United States Department of Agriculture (USDA) in Zusammenarbeit mit dem US-Militär in systematischen Versuchen entwickelt. Dem für die Namengebung zuständigen Committee on Insecticide Terminology of the Entomological Society of America erschien der systematische Name Diethyltoluamid einfach zu lang [6]. Bei IR3535 handelt es sich um einen Markennamen [7], wobei IR für den englischen Begriff insect repellent stehen dürfte. Bild 8: Struktur von Icaridin (1-(1-Methylpropoxycarbonyl)-2-(2-hydroxyethyl)piperidin) Schauen wir uns die chemische Struktur schrittweise an, dann wird der von der IPAC vergebene, systematische Name verständlicher: Die Grundstruktur ist das Piperidin, ein heterocyclischer Sechsring, der aus fünf Kohlenstoffatomen und einem Stickstoffatom gebildet wird. Häufig steht diese Grundstruktur am Ende des chemisch korrekten Namens. Dieses sekundäre Amin liegt carboxyliert vor. Eingeführt wurde am Stickstoffatom, bei dem die Zählung mit 1 anfängt, eine Oxycarbonyl-Gruppe -COO-, die mit einen Ethyl-Rest -CH2CH3 verbunden ist, der am ersten C-Atom, daher wieder eine 1 vorangesetzt, eine weitere Methyl-Gruppe -CH3 trägt. So wird der erste Teil des chemischen Namens verständlich: 1-(1-Methylpropoxycarbonyl). Betrachten wir den zweiten Teilbereich. Dieser sitzt am C-Atom neben dem N-Atom, also bekommt es die Zahl 2 vorangestellt. Bei diesem Rest handelt es sich um eine Hydroxyethyl-Gruppe. Da dort die Hydroxylgruppe -OH sich am zweiten Kohlenstoffatom befindet, lautet sein Name 2-Hydroxyethyl. Die Namen beider Reste – so werden einzelne Teilbereiche organischer Moleküle allgemein bezeichnet - werden nun dem Namen des Grundkörpers, also dem Heterocyclus Piperidin, vorangestellt, beginnend mit der kleinsten Zahl, also der 1. Noch genauer betrachtet fällt auf, dass sich in dieser Struktur zwei besondere Kohlenstoffatome befinden, die vier verschiedene Reste tragen. Damit gibt es jeweils zwei Anordnungen dieser vier Reste am C-Atom, die sich wie Bild und Spiegelbild verhalten. Verbindungen mit solchen asymmetrischen Kohlenstoffatomen in ihrer chemischen Struktur nennt man chiral. Die Kohlenstoffatome selbst werden als Chiralitätszentren bezeichnet. Bild 9: Struktur von Prallethrin (2-Methyl-4-oxo-3-(prop-2-inyl)cyclopent-2-enyl-2,2-dimethyl-3-(2-methylprop-1-enyl)cyclopropancarboxylat) Der systematische Name der chemischen Struktur der öligen, braunen Flüssigkeit hört sich zunächst ähnlich erschreckend an. Wir versuchen nun genauso systematisch, ihn in seinen einzelnen Strukturmerkmale zu zerlegen. Hier fallen zwei Grundstrukturen auf, die als Carboxylat miteinander verbunden sind: Cyclopropan, ein Dreiring, sowie Cyclopenten, ein Fünfring mit einer Doppelbindung. An beiden befinden sich weitere Reste. Beginnen wir mit dem Cyclopropan. An einem C-Atom befinden sich zwei Methyl-Gruppen -CH3 am zweiten Kohlenstoffatom, also 2,2-dimethyl. Am dritten Kohlenstoffatom ist ein aus drei Kohlenstoffatomen bestehender Rest mit einer Doppelbindung gebunden. An diesem Propenyl-Rest -CHCHCH3, befindet sich am zweiten Kohlenstoffatom eine weitere Methyl-Gruppe -CH3. Diese erste Teilstruktur lautet also komplett: 3-(2-methylprop-1-enyl). Nun zur anderen Hälfte der chemischen Struktur: Am Cyclopenten befinden sich drei weitere Strukturen: Ein Sauerstoffatom am vierten Kohlenstoffatom, daher 4-Oxo – diese Struktur wird auch als Carbonyl-Rest bezeichnet –, weiterhin ein Rest aus drei Kohlenstoffatomen mit einer Dreifachbindung am dritten Kohlenstoffatom, also 3-(prop-2-inyl), und noch eine Methyl-Gruppe -CH3 am zweiten Kohlenstoffatom des Cyclopenten-Rings. Diese zweite Teilstruktur lautet also komplett: 2-Methyl-4-oxo-3-(prop-2-inyl)-cyclopent-2-en. Da die erste Teilstruktur am ersten Kohlenstoffatom über seine Carboxylgruppe -COOH mit der zweiten Struktur verknüpft ist, handelt es sich um ein Cycolpropancarboxylat. Genauer betrachtet fallen in der Struktur von Prallethrin von ebenso wie beim vorher diskutierten Icaridin chirale Kohlenstoffatome auf, die dazu führen, dass diese Substanz ebenfalls chiral ist. Bild 10: Struktur von DEET (N,N-Diethyl-3-methylbenzamid oder N,N-Diethyl-3-toluamid) Die chemische Struktur lässt sich einfacher analysieren: Die Struktur eines zwei Ethyl-Gruppen enthaltenen Amids -CON(CH2CH3)2 ist mit einem Methylbenzol-Ring 3-methylbenzamid – der auch als Toluol bezeichnet wird, daher auch 3-toluamid – an dessen dritten Kohlenstoffatom verknüpft. Bild 11: Struktur von IR3535 (Ethyl-N-acetyl-N-butyl-β-alaninat oder 3-(N-Butyl-N-acetyl-amino)propionsäureethylester) Die Struktur erinnert an die Aminosäure β-Alanin. Diese kann also als Grundstruktur bezeichnet werden: β-alaninat. Der systematische Name der Aminosäure lautet 3-Aminopropionsäure. An der Aminogruppe -NH2 sind beide Wasserstoffatome -H durch Reste substituiert. Zum einen befindet sich am Stickstoffatom N ein aus vier Kohlenstoffatomen bestehender Butyl-Rest -CH2CH2CH2CH3, zum anderen eine Acetyl-Gruppe -COCH3. Das wäre der erste Rest R1 der Aminosäure-Grundstruktur. An der Carboxyl-Gruppe -COOH der Aminosäure befindet sich eine Ethyl-Gruppe -CH2CH3, der zweite Rest R2 der Grundstruktur eines Esters R1COOR2. Wichtig und interessant in diesem Zusammenhang: Das Umweltbundesamt wirbt auf seinem Biozid-Portal [https://www.umweltbundesamt.de/biozid-portal, https://youtu.be/Mq1NtQJ6lzE] für alternative Maßnahmen, z. B. die gute alte Fliegenklatsche, zu den Insekten-Repellents, schließlich können diese gefährlich für Mensch und Umwelt sein. Bild 12: Manuelle Methoden führen dazu, dass die Mücke ein unschönes Ende nimmt.
Ob nun mit Fliegenklatsche oder mit bloßer Hand, ich habe mich jedenfalls dazu entschieden, beide „Techniken“ des Zurückstoßens, Abschießens oder Vertreibens der blutsaugenden Plagegeister zur Mückenabwehr einzusetzen, die rein mechanische sowie die chemische.

(Fotos: Lüttgens)
(Foto: Lüttgens)
Wie schützt man sich?
Vor unserer Skandinavienreise habe ich im Freundes- und Bekanntenkreis alle skandinavienerfahrenen Urlauber gefragt, was man gegen die Mückenplage machen kann. Wirksamen Mückenschutz versprechen schließlich viele Hersteller von sogenannten Insekten-Repellents, die auf die Haut aufgetragen werden können. Der Begriff Repellent stammt aus dem Lateinischen. Das Verb repellere heißt so viel wie zurückschlagen, vertreiben oder verstoßen.
Woher weiß eine Mücke, wo es Blut zu holen gibt?
Die Weibchen benötigen den kostbaren Saft, um ihre Eier in sumpfigen Feuchtgebieten oder an den Ufern überfluteter Flüsse und Bäche ablegen zu können.
(Fotos: Lüttgens)
(Foto: Lüttgens)
Welche Wirkstoffe gibt es?
In diesem Tipp seien exemplarisch vier Beispiele solcher Repellents genannt:

(Foto: Lüttgens)

(Foto: Lüttgens)
Wie wirken Repellents?
Wenn eine Mücke den Geruch von Menschen oder Tieren wahrnimmt, steuert sie ihr Opfer an. Vereinfacht gesagt: Der „Duft“ gelangt in das Riechorgan der Mücke und trifft dort auf spezielle Geruchs-Rezeptoren, die sich dabei so verändern, dass Rezeptor-Neurone aktiviert werden. Diese senden elektrische Signale an das Nervensystem weiter und „sagen“ der Mücke durch die Intensität der Wahrnehmung, wo es lang geht in Richtung Haut. Wer´s genauer mag: Die olfaktorischen Rezeptoren der Mücke sind Proteinstrukturen in der Zellmembran, die auf Duftfahne ihre Blutswirte reagieren. Duftmolekül und Proteinstruktur passen so gut zueinander, wie ein Haustürschlüssel nur für eine bestimmte Haustür passt. Diese besondere Bindung zwischen zwei solchen biochemischen Strukturen wird daher auch als Schlüssel-Schloss-Prinzip bezeichnet.
Was verbirgt sich hinter den Namen der Wirkstoffe?
Sonderbare Bezeichnungen Icaridin, Prallethrin, DEET und IR3535. Was bedeuten sie? Selbst chemieaffine Mensch können nichts daraus schließen, denn es handelt sich um reine Kunstworte, sogenannte Trivialnamen (lat. trivialis: gewöhnlich), die gerne genutzt werden. Das hat gute Gründe. Viele Trivialnamen, wie Vanillin, Chilesalpeter oder Blutlaugensalz, wurden lange vor einer systematischen und damit chemisch eindeutigen Bezeichnung verwendet. Sie wurden häufig abgeleitet aus der Herkunft oder dem Herstellungsverfahren einer Chemikalie. Ein weiterer Grund für die Nutzung von Trivialnamen: So manche chemisch korrekten Bezeichnungen sind reichlich sperrig, so dass die Kommunikation selbst unter Chemikerinnen und Chemikern nicht einfach fällt. Ein Beispiel: Cuban, ein besonders ästhetischer wirkender Kohlenwasserstoff mit der Formel C8H8, dessen acht Kohlenstoffatome so angeordnet sind, dass sie an einen sechsseitigen Würfel erinnern. Der systematische Name lautet Pentacyclo[4.2.0.02,5.03,8.04,7]octan. Ein schrecklich sperriger und fast nicht aussprechbarer Name - aber chemisch korrekt.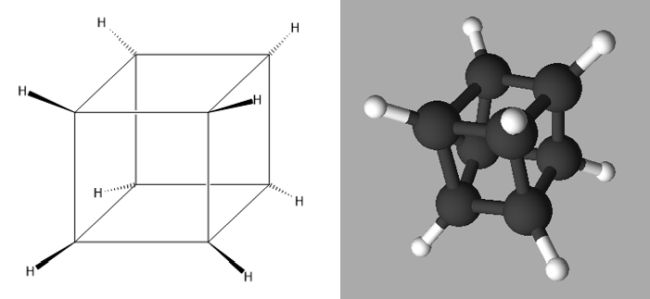
Für Spezialisten: Die vier Repellent-Wirkstoffe - chemisch betrachtet
Icaridin (1-(1-Methylpropoxycarbonyl)-2-(2-hydroxyethyl)piperidin)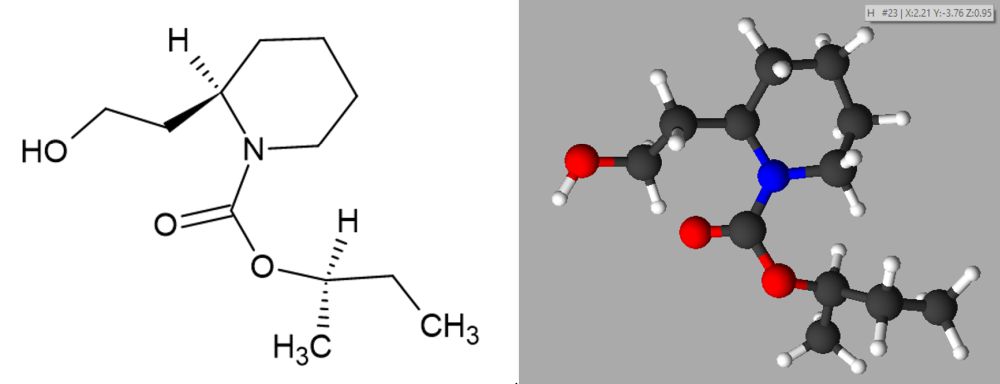
Prallethrin (2-Methyl-4-oxo-3-(prop-2-inyl)cyclopent-2-enyl-2,2-dimethyl-3-(2-methylprop-1-enyl)cyclopropancarboxylat)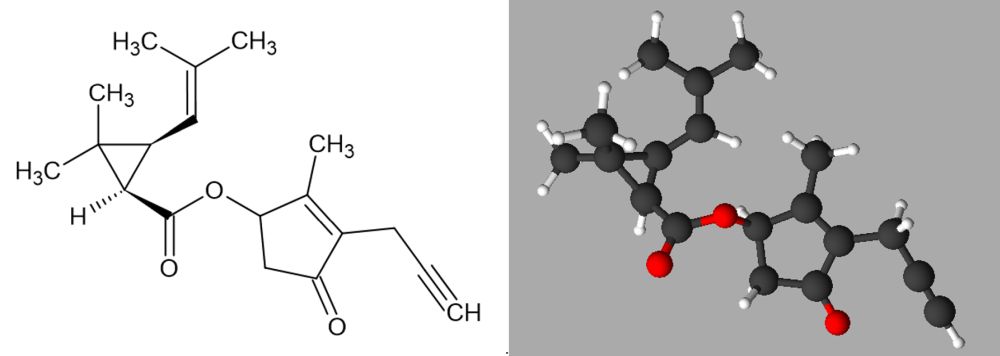
DEET (N,N-Diethyl-3-methylbenzamid oder N,N-Diethyl-3-toluamid)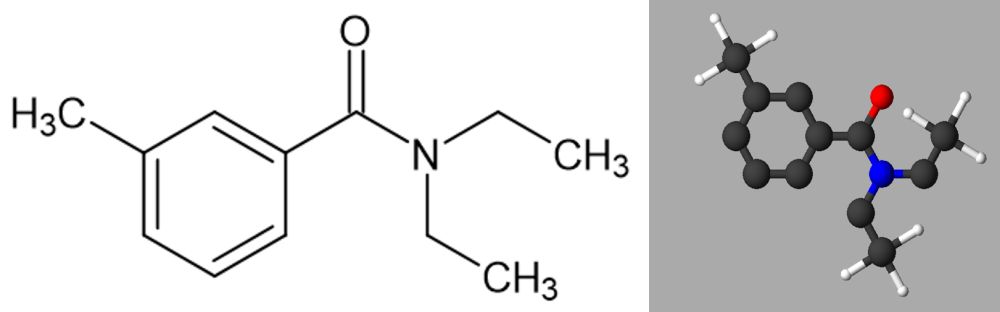
IR3535 (Ethyl-N-acetyl-N-butyl-β-alaninat oder 3-(N-Butyl-N-acetyl-amino)propionsäureethylester)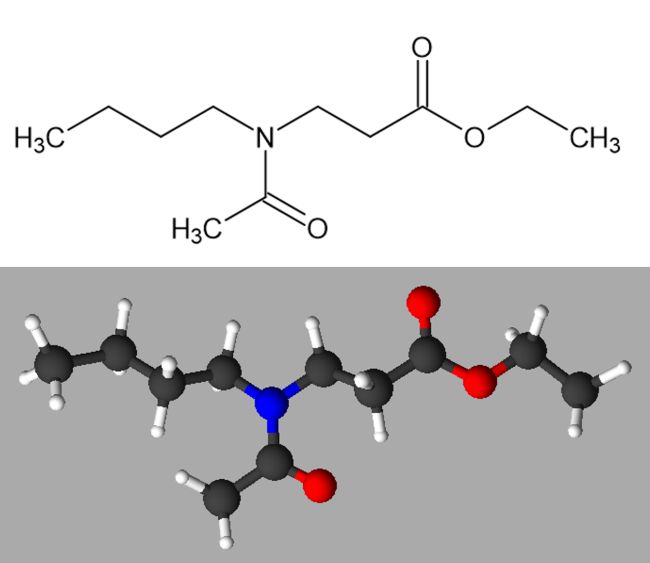
Mein Fazit
Vielleicht gibt es drei Erkenntnisse. Die erste: Systematische Namen sind nicht leicht zu verstehen und manchmal ganz schön abschreckend. Aber schrittweise kommt man zum Erfolg. Die zweite: Trivialnamen machen die Verständigung untereinander viel einfacher – für Laien und für Fachleuten. Und schließlich drittens: Unterschiedliche Meinungen über die Wirksamkeit von Mücken-Repellents helfen letztlich wenig. Ob nun dieses oder jenes Mittel wirkt, sollten alle, die sie einsetzten wollen, selbst testen.
(Foto: Lüttgens)
Literatur:
[1] https://autan.de/de-de (zuletzt abgerufen am 12.7.2021)
[2] US 622 Mygg & Fästingstift, https://www.apotekhjartat.se/produkt/us-622-mygg-fastingstift-23-g (zuletzt abgerufen am 12.7.2021)
[3] Nexa Lotte Insekten-Stecker 3in1, https://www.lovethegarden.com/de-de/produkt/nexa-lotte-insektenschutz-3in1-1-set und https://www.youtube.com/watch?v=0hRwm4l7QWw (zuletzt abgerufen am 12.7.2021)
[4] Jungle Formula, https://www.jungleformula.co.uk/products/#Outdoor-and-Camping (zuletzt abgerufen am 12.7.2021)
[5] Xu, P. et al., Mosquito odorant receptor for DEET and methyl jasmonate. Proceedings of the National Academy of Sciences 2014, 111(46), 16592-16597
[6] Matthew DeGennaro, The mysterious multi-modal repellency of DEET, Fly (Austin), 2015;9(1):45-51
[7] Insektenrepellent IR3535, https://www.merckgroup.com/de/expertise/cosmetics/care-solutions/insect-repellent/about-IR3535.html (zuletzt abgerufen am 12.7.2021)
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 28. Juli 2021, Fritz Meiners
