
Redoxreaktionen mit Wasserstoffperoxid
Experimente:
Experimente mit Wasserstoffperoxid
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Mit Wasserstoffperoxid (chemische Formel H2O2) bleicht der Friseur bekanntlich
Haare. Denn Wasserstoffperoxid ist ein starkes Oxidationsmittel. Man kann sich das Bleichmittel
kaufen und das ausprobieren. Das untersuchen wir auf die Anwesenheit von Wasserstoffperoxid.
|
Versuch 1: Nachweis von Wasserstoffperoxid in Haarbleichmitteln
|

Bild 1 (Foto: Daggi)
Nun wollen wir das Haarebleichen ausprobieren. Dazu verwenden wir eine alkalische
LŲsung von Wasserstoffperoxid. Zuvor aber ein...
Warnhinweis zum Umgang mit Wasserstoffperoxid
Der Siedepunkt von reinem Wasserstoffperoxid betršgt 150,2 įC (Normaldruck). Eine
30%ige LŲsung siedet schon bei 106 įC. Mit steigender Konzentration steigt auch der
Siedepunkt an. Wegen der Aufkonzentrierung dŁrfen die handelsŁblichen 30%igen
LŲsungen von Wasserstoffperoxid nicht erhitzt werden, da sie schlieŖlich explodieren
kŲnnen. Das gilt vor allem beim Destillieren von LŲsungen oder Reaktionsansštzen,
die H2O2 enthalten. Das muss deshalb zuvor durch geeignete Reduktionsmittel zerstŲrt
werden.
Aus dem gleichen Grunde sollte man WasserstoffperoxidlŲsungen nicht allzu lange
offen stehen lassen, da ihre Konzentration durch Wasserverdunstung zunimmt.
|
Versuch 2: Blondfšrben
|
Wir liegen richtig, wenn wir feststellen: Der Farbstoff ist oxidiert worden. Hierzu eine Reaktionsgleichung zu formulieren ist allerdings schwer. Aber wir kŲnnen es versuchen.
Farbstoff-H+ + H2O2 + OH- ———> Oxidierter Farbstoff + 2 H2O
Nun nehmen wir eine andere farbige Substanz: Kaliumpermanganat. Wir behandeln sie ebenfalls mit Wasserstoffperoxid.
|
Versuch 3: Entfšrben von Kaliumpermanganat mit Wasserstoffperoxid
|
Das starke Oxidationsmittel Kaliumpermanganat wird entfšrbt. Das kann nur heiŖen, dass es reduziert worden ist.
Die Reaktionsgleichung ist:
2 MnO4- + 5 H2O2 + 6 H+ ———> 2 Mn2+ + 8 H2O + 5 O2
Wie kommt das? Gibt es einen Unterschied bei den beiden Reaktionen des Wasserstoffperoxids? Untersuchen wir das mal der Reihe nach.
Wasserstoffperoxid ist zunšchst einmal ein starkes
Oxidationsmittel
Das gilt aber nur gegenŁber Reduktionsmitteln, zu denen auch viele der klassischen
Farbstoffe gehŲren. Durch sie wird Wasserstoffperoxid reduziert.
Die Reaktionsgleichung der Reduktion von Wasserstoffperoxid ist
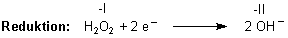
(Genau genommen wird nur der im H2O2 gebundene Sauerstoff reduziert. Liegt er im Wasserstoffperoxid in der Oxidationsstufe -I vor, so ist seine Oxidationszahl im Hydroxid-Ion -II.)
Wasserstoffperoxid kann auch als Reduktionsmittel wirken
Der Versuch 3 mit Kaliumpermanganat hat gezeigt: Wasserstoffperoxid wird
oxidiert, es muss in diesem Fall also Reduktionsmittel sein.
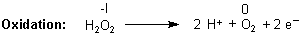
Dabei wird Sauerstoff freigesetzt.
(Genau genommen wird nur der im H2O2 gebundene Sauerstoff oxidiert. Liegt er im Wasserstoffperoxid in der Oxidationsstufe -I vor, so ist seine Oxidationszahl im SauerstoffmolekŁl 0.)
‹brigens ist auch die Fehlingsche Probe mit Wasserstoffperoxid (-> Versuch) positiv.
Wasserstoffperoxid zersetzt sich selbst
Es ist bekannt: Wasserstoffperoxid-LŲsungen sind nicht stabil. Sie zersetzen sich.
Die Selbstzersetzung ist exotherm und verlšuft bei Raumtemperatur recht langsam,
da sie aktiviert werden muss. Allerdings erwšrmt sich die LŲsung bei zunehmender
Zersetzung selbst! Das fŁhrt dazu, dass sich die Reaktion aufschaukelt. Bei hohen
Temperaturen verlšuft die Selbstzersetzung so rasch, dass sogar Explosionsgefahr
besteht! Deshalb bewahrt man Wasserstoffperoxid zweckmšŖigerweise im
KŁhlschrank auf. Das ist eine Anwendung der RGT-Regel.
Die Selbstzersetzung wird durch die Gegenwart eines Katalysators gefŲrdert. Durch ihn wird die Aktivierungsenergie gesenkt, so dass die Reaktion auch schon bei tiefer Temperatur in groŖem Umfang ablaufen kann.
|
Versuch 4: Katalytische Selbstzersetzung von Wasserstoffperoxid
|
Besonders wirksam ist der Biokatalysator Katalase mit dem systematischen Namen H2O2 : H2O2-Oxidoreduktase. ‹ber dieses Enzym berichten wir auf einer besonderen Webseite. Dort sind auch Versuchsanleitungen zu finden.
Zur Herleitung der Zersetzungsgleichung teilen wir die Redox-Reaktion formal in die Reduktion und die Oxidation auf und addieren dann die beiden Gleichungen.
Reduktion: H2O2 + 2 e- ———> 2 OH-
Oxidation: H2O2 ———> O2 + 2 H+ + 2 e-
Redox-Reaktion: H2O2 + H2O2 ———> 2 OH- + 2 H+ + O2
Mit 2 OH- + 2 H+ —> 2 H2O folgt daraus die bekannte Zersetzungsgleichung des Wasserstoffperoxids.
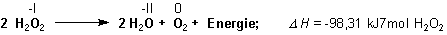
Auf der Eduktseite links hat der Sauerstoff zweimal die Oxidationszahl -I, auf der Produktseite rechts die Oxidationszahlen -II und 0. Solche Reaktionen nennt man Disproportionierung.
Zur Verringerung dieser Selbstzersetzungsgefahr setzt man den LŲsungen Inhibitoren zu. Diese wirken also als negative Katalysatoren; das kŲnnen zum Beispiel Harnstoff oder Barbitursšure sein.
Durch Variation des pH-Werts kann man die Redoxreaktionen
von Wasserstoffperoxid steuern
Das kann man zunšchst anhand von Chrom(III)-Verbindungen zeigen.
|
Versuch 5: Variation des pH-Milieus bei der Oxidation von Chrom(III)-Verbindungen
mit Wasserstoffperoxid
|

Bild 2 (Foto: Daggi)
Nur in der alkalischen LŲsung findet eine Reaktion statt; sie fšrbt sich aufgrund der Chromatbildung gelb.
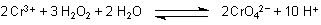
Bei der Reaktion bilden sich Protonen, die das Gleichgewicht hemmen. Um die abzufangen, muss die LŲsung alkalisch sein.
Das Gleiche zeigen wir anhand des Stempelfarbstoffs Kristallviolett.
|
Versuch 6: Entfšrben von Kristallviolett mit Wasserstoffperoxid
|
Die Entfšrbung liegt nicht an der Zugabe an Natronlauge - diese Reaktion ist zwar auch mŲglich, geht viel langsamer vonstatten.
Zum Schluss ein Hinweis fŁr Spezialisten
Zu den Bedingungen, unter denen Wasserstoffperoxid als Oxidations- oder als
Reduktionsmittel wirkt, und zur pH-Wert-Abhšngigkeit der Standardpotentiale des
Wasserstoffperoxids gibt es bestimmte Regeln. Um die zu verstehen, schreiben wir
die oben gezeigten Reaktionsgleichungen etwas anders:
Wasserstoffperoxid ist Oxidationsmittel
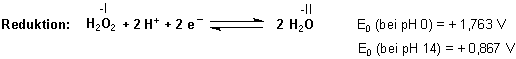
Wasserstoffperoxid ist Reduktionsmittel
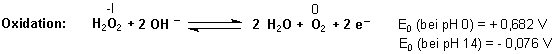
Den beiden Reaktionsgleichungen entnehmen wir folgende Regeln:
| 1 | Je niedriger der pH-Wert seiner LŲsungen ist, desto hŲher ist die Oxidationskraft von Wasserstoffperoxid gegenŁber ausgesprochenen Reduktionsmitteln. |
| 2 | Je hŲher der pH-Wert seiner LŲsungen ist, desto hŲher ist die Reduktionskraft von Wasserstoffperoxid gegenŁber ausgesprochenen Oxidationsmitteln. |
So weit, so gut. Aber diese Regeln sind jedoch Łberhaupt nicht mit unseren Experimenten und den daraus gewonnenen Ergebnissen vereinbar. Sie scheinen ihnen sogar vŲllig zu widersprechen!
| - | Die organischen Farbstoffe des Haares und das Kristallviolett werden nur im Alkalischen oxidiert. |
| - | Kaliumpermanganat wird nur im sauren Milieu reduziert. |
Die Erklšrung: Die o. a. Regeln gelten nur fŁr die Halbzellenpotentiale des Wasserstoffperoxids! Und diese darf man keinesfalls isoliert betrachten. Man muss ihnen vielmehr das spezifische pH-abhšngige Verhalten der Reduktionsmittel bzw. Oxidationsmittel, mit denen Wasserstoffperoxid reagiert, gegenŁberstellen:
| - | Das Kristallviolett und andere organische Farbstoffe benŲtigen alkalisches Milieu, weil bei der Oxidationsreaktion Protonen entstehen, damit sich die chinoide Struktur oxidierter Benzolderivate ausbilden kann. |
| - | Beim Permanganat werden Protonen benŲtigt, um im Verlauf der Reduktionsreaktion den Sauerstoff des MnO4--Ions (formal als O2-) abfangen zu kŲnnen. |
Erst dann kommt man zu den pH-Abhšngigkeiten der Reaktionen von Wasserstoffperoxid, die wir bei unseren Experimenten beobachtet haben. Trotz der o. a. Regeln halten wir somit fest: NatŁrlich kann Wasserstoffperoxid auch im alkalischen Milieu oxidierend wirken (und auch im sauren Milieu reduzierend).
Zur Chemie mit Wasserstoffperoxid haben wir eine groŖe
Webseitengruppe.