4 Einige Grundlagen zur Biochemie der Nahrungsmittelverwertung
Nach der Besprechung der wichtigsten Stoffklassen der Lebensmittelchemie schließt nun ein kurzer, exemplarischer Exkurs in die Biochemie an. Er soll Verständnis schaffen für die wichtigsten Abläufe, deren Komplexizität und Regelung sowie Verwundbarkeit.
4.1 Biochemie der Verdauung
Die von den Pflanzen produzierten Nährstoffe, die den heterotrophen Organismen als Ausgangsverbindungen zur eigenen Biosynthese oder zur Energieumwandlung dienen, liegen im allgemeinen als größere Moleküle vor und müssen zunächst in die kleinsten sinnvollen Bausteine zerlegt werden. Nur diese können resorbiert werden. Dies ist vernünftig, da viele Kohlenhydrate und Proteine Allergene sind. Lipide können Biomembranen nicht passieren.
Aus Kohlenhydraten entstehen letztlich Glucose, Fructose und Galactose, aus Proteinen Aminosäuren, aus Fetten Glycerin und Fettsäuren. Ort der Umwandlung ist der Verdauungstrakt, neben Lunge und Haut die dritte große stoffliche Kontaktfläche des Körpers mit der Umwelt.
Verdauungsvorgänge sind exotherm. Hierbei wird die Energie wieder frei, die bei der Synthese der Makromoleküle aufgewandt werden musste. Die Spaltung erfordert aber eine hohe Aktivierungsenergie. Diese wird durch Enzyme stark abgesenkt. Die meisten Verdauungsenzyme sind Hydrolasen, d. h. sie spalten ihr Substrat unter Einlagerung von Wasser:
Amylose + n H2O ———> Maltose oder Glucose
Protein + n H2O ———> Aminosäuren
Fett + 3 H2O ———> Glycerin + Fettsäuren
4.1.1 Verdauung der Kohlenhydrate
Diese beginnt im Mund. Speichel enthält Amylasen, die Stärke zu Oligosacchariden bis herunter zum Disaccharid Maltose zerlegen.
Im Magen spaltet die starke Salzsäure einen Teil der Disaccharide wie Maltose und Saccharose in die Monosaccharide.
Im Dünndarm erfolgt der endgültige Abbau von Stärke und verzweigtem Glykogen zu Maltose. Die hier wirkenden Amylasen stammen aus der Bauchspeicheldrüse (Pankreas).
Die Maltose wird durch die Maltase aus der Dünndarmwand in Glucose zerlegt. Daneben gibt es die analog wirkenden Enzyme Saccharase und Lactase.
Die Monosaccharide Glucose, Fructose und Galactose werden von den Zellen der Darmwand resorbiert und so in die Blutbahn geschleust.
4.1.2 Verdauung der Fette
Die Fettverdauung erfolgt ausschließlich im Dünndarm durch die Lipase des Pankreas. Voraussetzung hierfür ist die Emulgierung der Lipide. Diese erfolgt unter Einwirkung von körpereigenen Tensiden (-> 6.5.1), den stark grenzflächenaktiven Gallensäuren. Diese sind chemisch mit dem Cholesterin eng verwandt (daher der Name Cholsäuren).
Die Lipase spaltet die Ester in Fettsäuren und Glycerin. Die Gallensäuren erleichtern auch das Einschleusen der Fettsäuren sowie der fettlöslichen Vitamine (A, D, E und K) in das Gewebe.
4.1.3 Verdauung der Eiweiße
Die Hydrolyse von Proteinen erfolgt durch Proteasen, die als inaktive Vorstufen in den Bildungszellen gespeichert werden. Proteasen können nur denaturierte Proteine angreifen. Denaturierung erfolgt entweder durch Kochen oder durch die Einwirkung der starken Salzsäure im Magen (c(HCl) = 0,1 M, entsprechend einem pH-Wert von 1-2). Diese Salzsäure wirkt auch desinfizierend. Da sie bei Kleinkindern fehlt, sind diese besonders von Magen- und Darminfektionen bedroht.
Im Magen findet sich das bekannte Pepsin, das als halbspezifische Peptidase die Proteinmoleküle neben aromatischen Aminosäuren spaltet. Pepsin ist ein Protein, das gegen Salzsäure unempfindlich ist.
Im Dünndarm wird die HCl zunächst durch Bicarbonatpuffer neutralisiert und ein schwach basisches Milieu eingestellt. Hier wirken die von der Bauchspeicheldrüse produzierten Proteasen Trypsin (greift neben Arg oder Lys an) und Chymotrypsin (wirkt wie Pepsin).
Die entstandenen Bruchstücke (Oligopeptide) werden durch verschiedene hochspezifische Exopeptidasen und anschließend durch Dipeptidasen in die einzelnen resorbierbaren Aminosäuren zerlegt.
4.2 Stoffwechselbeispiele
Was wird letztlich aus der Nahrung? Grundsätzlich können fast alle Stoffe zum Aufbau körpereigener Biomasse dienen, z. B. Aminosäuren zur Synthese von körpereigenen Proteinen. Jedoch werden die meisten Stoffe vollständig abgebaut. Ausscheidungsprodukte sind zunächst nicht resorbierte Verbindungen oder unveränderte Ballaststoffe, überschüssiges Lösungsmittel Wasser, Mineralstoffe und Zusatz- oder Inhaltsstoffe wie die Farbstoffe. Andere Stoffe stammen aus dem Endabbau der Nahrungsmittel: CO2, H2O, Ammonium-Ionen und Harnstoff. Außerdem wird Energie freigesetzt.
4.2.1 Energieumsatz bei biochemischen Reaktionen
Bevor auf die einzelnen chemischen Reaktionen eingegangen werden soll, muss etwas zum Energieumsatz bei biochemischen Abläufen gesagt werden. Nur Energie versetzt uns in die Lage, mechanische Arbeit zu leisten und biochemische Synthesen körpereigener Stoffe durchzuführen.
Der Anteil an der insgesamt freigesetzten Energie bei einer chemischen Reaktion ("Reaktionsenthalpie"), der Arbeit zu leisten vermag, ist die nutzbare Energie, die sog. Freie Energie. Unter Arbeit versteht man in diesem Zusammenhang das Knüpfen neuer chemischer Bindungen, Bildung elektrischer Spannungszustände (Nervenfunktionen) oder Ausübung mechanischer Arbeit. Freisetzung von Wärme ist Verlust von chemischer Arbeit, also von Freier Energie. Wärme dient letztlich der Steigerung der Entropie, der Tendenz, Unordnung zu bilden und Zustände so zu nivellieren, da sie ohne Potential sind und deshalb keine Arbeit mehr zu leisten vermögen. Die Zelle ist deshalb bestrebt, chemische Reaktionen möglichst ohne große Wärmeverluste ("isotherm") durchzuführen. (Im Abschnitt 4.2.4 wird noch einmal ausführlich darauf eingegangen.)
Prozesse, die unter Freisetzung von Freier Energie ablaufen, nennt man exergon. Der umgekehrte Fall ist endergon. Es ist wichtig, dass die Begriffe nicht mit exotherm und endotherm verwechselt werden dürfen. So kühlt sich Salz beim Lösen ab, ohne dass der Lösungsvorgang mittendrin aufhört. Er ist endotherm und dürfte gar nicht spontan ablaufen. Da sich aber der Ordnungszustand des Systems ändert, ist der Prozess exergon und kann spontan ablaufen.
Prozesse, die im Körper z. B. zur Energieumwandlung dienen, sind Oxidationen, also stille Verbrennungen. Zum Einleiten der den biochemischen Reaktionen analogen Reagenzglas-Reaktionen ("in vitro") sind im Allgemeinen hohe Aktivierungsenergien notwendig, worauf dann schlagartig eine große und ungesteuerte Energiemenge durch Verbrennung frei wird.
Man denke an das Verbrennen von Zucker. Zucker lässt sich ohne dauerndes Erhitzen (Aktivieren) nicht in Brand setzen. Streut man jedoch Zigarettenasche über den Zucker, brennt er nach dem Anzünden von selbst weiter; der Aufwand an Aktivierungsenergie ist wesentlich geringer. Zigarettenasche wirkt also als Katalysator.
In biochemischen Abläufen werden Aktivierungsenergien durch die Tätigkeit der Enzyme so drastisch gesenkt, dass die Wärmeverluste minimal sind und isotherme Verhältnisse annähernd erreicht werden können.
Das Grundprinzip stoffwechselphysiologischer Vorgänge ist das Aufteilen einer chemischen Reaktion in möglichst viele, durch Enzyme katalysierte Einzelschritte. Dabei ist der Aufwand an Aktivierungsenergie für alle Einzelschritte zusammen geringer als für die einzelne, aber ungesteuert ablaufende in vitro-Reaktion. So wird die Ausbeute an nutzbarer Energie optimiert. Zusätzlich können an möglichst vielen Stellen Steuerungsmechanismen wirksam werden.
Als Beispiel soll die Oxidation von Glucose dienen:
Formal ist der Vorgang, ob er nun im Reagenzglas, über der Bunsenbrennerflamme oder in der Zelle abläuft, der gleiche. Nur sind die Wege von Edukt zu Produkt gänzlich verschieden.
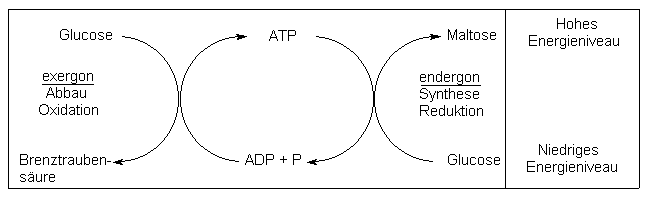
Verbrennt man ein Mol Glucose direkt in vitro, erhält man 2874 kJoule Wärmeenergie, mit der man nur wenig anfangen kann. Grund ist, dass Zellen Wärme nicht speichern und für Synthesen einsetzen können. Durchläuft die Glucoseoxidation aber die gleich zu schildernden Reaktionssequenzen, so ist der Wärmeverlust nur noch 61 %, die nutzbare Energie beträgt 39 % (Wirkungsgrad). Die nutzbare Energie wird als chemische Verbindung, als ATP, gespeichert. Wenn jetzt im Körper eine chemische Reaktion abläuft, bei der Energie gebraucht wird, z. B. der Aufbau eines Polysaccharids oder Proteins aus den Monomeren, so wird pro Bindung simultan dazu ein ATP-Molekül gespalten. Die Spaltungsenergie des ATP dient zumindest zu einem gewissen Teil zur Synthese des Biomoleküls (-> Abb. 31).

Abb. 31: Gekoppelte biochemische Reaktionen
Dieses Prinzip der gekoppelten Reaktionen ist typisch für biochemische Abläufe. Es entspricht in gewisser Weise dem Donator/Akzeptorprinzip wie bei den Säure/Base- oder Redoxreaktionen.
Die chemische Reaktionsgleichung der biochemischen Oxidation von Glucose lautet deshalb:
(Beachten Sie den reduzierten Wert von D H.)