| Klick mich an! |
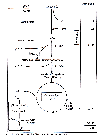 |
| Abb. 32: Kurzer ‹berblick Łber den Abbau der Glucose |
| Klick mich an! |
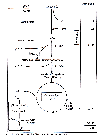 |
| Abb. 32: Kurzer ‹berblick Łber den Abbau der Glucose |
4.2.2 Oxidativer Abbau der Glucose bis zu Acetyl-CoA
Der oxidative Abbau der Glucose zu Kohlendioxid und Wasser
umfasst die folgenden Reaktionsgruppen (-> Abb. 32):
A. Glykolyse
Die Glykolyse ist der oxidative, aber anaerobe Abbau von Glucose zu Brenztraubensšure und reduzierenden ńquivalenten [H]:
Folgende Punkte sind zum Verstšndnis der chemischen Ablšufe wichtig:
| 1. | Jeder Reaktionsschritt wird durch mindestens ein Enzym katalysiert. |
| 2. | Die Oxidation erfolgt nicht durch Reaktion
mit Sauerstoff, sondern durch schrittweises Abspalten von
Reduktionsšquivalenten [H]. Diese werden vom Substrat auf NAD+
(Nicotinsšureamiddinucleotid) Łbertragen und liegen
anschlieŖend gebunden als NADH vor:
Substrat-H2 + NAD+ ———> Substrat (ox) + NADH + H+ Primšres Oxidationsmittel der Biochemie ist also NAD+ und nicht Sauerstoff. |
| 3. | Die Oxidationsenergie wird durch Bildung von ATP aus ADP und Phosphat abgefangen. |
| 4. | Sauerstoffatome, die in die Substrate eingebaut werden, stammen aus dem Wasser, das an Doppelbindungen addiert wird. Kohlendioxid entsteht bei Decarboxylierungen. |
Der Ablauf der Glykolyse kann kurz wie folgt dargestellt werden (-> Abb. 33):
Glucose wird mit dem Blut ins Gewebe transportiert. Unter
Mitwirkung des blutzuckersenkenden Hormons Insulin wird sie unter
gleichzeitiger Phosphorylierung durch ATP in die Zelle eingeschleust.
Es folgt Isomerisierung der Glucose zu Fructose. Mit
einem weiteren ATP bildet sich Fructose-1,6-diphosphat. Bis hierhin
ist ATP ausschlieŖlich investiert worden.
| Klick mich an! |
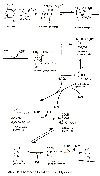 |
| Abb. 33: Chemische Reaktionen der Glykolyse |
Dieser Zuckerester wird gespalten in zwei C3-Segmente, die miteinander im chemischen Gleichgewicht stehen und von denen sich die Komponente Glycerinaldehyd-3-phosphat oxidativ in Glycerinsšure-3-phosphat umwandelt.
Die Oxidation von Glycerinaldehyd erfolgt unter gleichzeitiger Bildung eines Sšureanhydrids zwischen der gebildeten Glycerinsšure und Phosphorsšure. Dieses wird unter ATP-Bildung gespalten, es bildet sich Glycerinsšure-3-phosphat. Es erfolgt Umlagerung zu Glycerinsšure-2-phosphat und anschlieŖend Wasserabspaltung (Dehydratisierung) zu Phosphorenolbrenztraubensšure. Diese stellt aufgrund des sauren Charakters von Enolen ebenfalls ein energiereiches Sšureanhydrid mit Phosphorsšure dar, das wieder unter ATP-Bildung gespalten wird. Es resultiert das Endprodukt der Glykolyse, die Brenztraubensšure.
Die Bilanz der Glykolyse ist (P bezeichnet Phosphat oder Phosphorsšure):
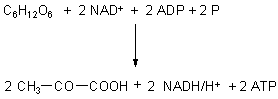
B. RŁckgewinnung von NAD+. Gšrung und Atmung
Als Problem macht sich bei der Glykolyse rasch das Anhšufen von NADH und somit der Mangel am Oxidationsmittel NAD+ bemerkbar, da dessen Konzentration in der Zelle gering ist. Damit sollte die Glykolyse nach kurzem Anlaufen zum Stillstand kommen. Die Zellen mŁssen folglich stšndig NAD+ regenerieren. Dies ist grundsštzlich auf zwei Wegen mŲglich, deren Richtung vom Redoxmilieu des Reaktionsortes abhšngt:
a) Bei Sauerstoffmangel (anaerobes Milieu, z. B. im eutrophierten See, im DŁnndarm oder im schlecht durchbluteten Muskel) wird NAD+ aus NADH durch Reduktion von End- oder Zwischenprodukten der Glykolyse zurŁckgebildet (Gšrung). Diese vertreten den Sauerstoff als Oxidationsmittel, wobei sie selbst reduziert werden. Dabei ist der Energiegewinn nur minimal. Einige Beispiele hierfŁr sind:
Acetaldehyd + NADH + H+ ———>
Ethanol + NAD+
Pyruvat + NADH + H+ ———>
Milchsšure + NAD+
Glycerinaldehyd + NADH + H+ ———>
Glycerin + NAD+
Die Produkte werden an das šuŖere Milieu abgegeben, wobei sie als nunmehr reduzierende Stoffe die Umgebung noch anaerober einstellen. So kann ein See schlieŖlich "umkippen".
Bakterien kŲnnen an dieser Stelle auch Sulfat-Ionen reduzieren, wobei sie den fŁr anaerobe Umgebungen typischen Schwefelwasserstoff bilden:
Andere Wege fŁhren vom Nitrat zum giftigen Nitrit, was auch im Darm von Kleinkindern ablšuft:
b) Bei Sauerstoffanwesenheit (aerobes Milieu) wird NAD+ durch Oxidation von NADH mit Hilfe von freiem Sauerstoff zurŁckgebildet (Atmung):
Dieser Weg (die Atmungskette; -> 4.2.4) ist energetisch wesentlich effektiver als die Gšrung.
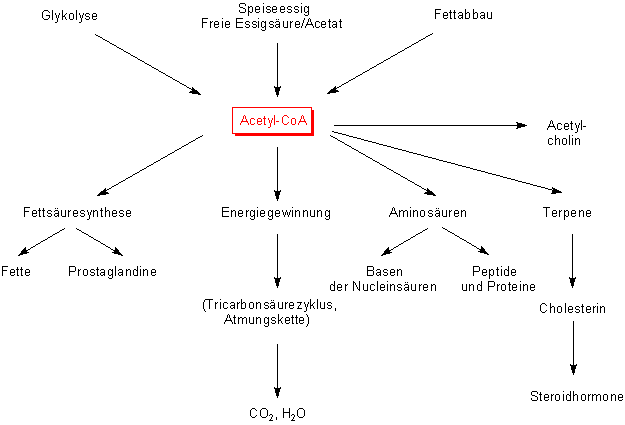
Abb. 34: Stoffwechselschaltstelle Acetyl-CoA
C. Aktivierte Essigsšure
Aktivierte Essigsšure (im Biochemikerjargon Acetyl-CoA genannt) stellt eine wichtige Schaltstelle im Stoffwechsel dar (-> Abb. 34). Sie entsteht auch beim Abbau der Fettsšuren, bei der Oxidation von Glycerin und Ethylalkohol sowie beim Abbau von Aminosšuren. Andererseits ist die aktivierte Essigsšure wiederum Grundbaustein fŁr Fettsšuren. Hier liegt der Zusammenhang zwischen zuviel Nahrung, Alkohol und dem Fettansatz begrŁndet. (Das Glycerin fŁr die Fettsynthese wird ebenfalls aus der Glykolyse abgezweigt.) Aktivierte Essigsšure ist auch Grundbaustein fŁr die Synthese von Cholesterin, Nebennierenrinden- und Sexualhormonen sowie Prostaglandinen. In den Pflanzen bilden sich aus aktivierter Essigsšure Terpene, Carotinoide, Kautschuk und Lignin.
Aktivierte Essigsšure ist nicht nur Synthesebaustein, sondern wird weiterhin zur Energieumwandlung oxidativ abgebaut. Auch dabei werden Reduktionsšquivalente [H] und ATP gebildet, und zwar wesentlich mehr, als bislang im Verlauf der Glykolyse entstanden sind. Dies geschieht mit Hilfe des Citronensšurezyklus. Dieser wird auch Tricarbonsšurezyklus genannt.
4.2.3 Citronensšurezyklus (Tricarbonsšurezyklus)
Die Oxidation von Essigsšure (bzw. Acetyl-CoA) wird durch die folgende Gleichung beschrieben:
Auch diese Oxidation lšuft schrittweise ab, um die Energieausbeute zu optimieren. Die Reaktionssequenz ist einer der schŲnsten biochemischen Katalyse-Kreislšufe, der Citronensšurezyklus (-> Abb. 32 und 35).
Der Kreislauf dient dazu, Essigsšure zu CO2 und Reduktionsšquivalenten [H] abzubauen und das StartmolekŁl Oxalessigsšure zurŁckzugewinnen.
Die Reaktionen kŲnnen kurz wie folgt beschrieben werden (-> Abb. 35):
Aktivierte Essigsšure wird auf Oxalessigsšure Łbertragen, wobei sich Citronensšure bildet. In den nšchsten zwei Schritten wird Citronensšure zu Isocitronensšure umgelagert. Diese wird mit NAD+ oxidiert, wobei eine instabile Verbindung gebildet wird, die unter Bildung von a-Ketoglutarsšure CO2 abspaltet (decarboxyliert).
Die Ketoglutarsšure wird erneut unter Mitwirkung von NAD+ oxidativ decarboxyliert, wobei Bernsteinsšure entsteht. (Hierbei wird die Oxidationsenergie erstmals direkt als ATP abgefangen.) Aus Bernsteinsšure werden zwei H-Atome abgespalten. Diese Dehydrierung fŁhrt zu Fumarsšure. (Das Oxidationsmittel ist diesmal FAD.)
An Fumarsšure wird ein MolekŁl Wasser addiert: ńpfelsšure entsteht. (Dies ist ein Beispiel fŁr nichtoxidative EinfŁhrung eines Sauerstoffatoms. Der Sauerstoff hat seine Oxidationszahl nicht gešndert.) ńpfelsšure wird mit NAD+ zu Oxalessigsšure oxidiert. Damit ist der Zyklus geschlossen.
| Klick mich an! |
 |
| Abb. 35: Citronensšurezyklus |
Zwischenbilanz des Glucoseabbaus:
Der Abbau der Glucose ist bis jetzt folgendermaŖen verlaufen (ab Acetyl-CoA muss alles doppelt gezšhlt werden):
Die Reduktionsšquivalente [H] liegen als NADH + H+ (bzw. FADH2) vor.
| Klick mich an! |
 |
| Abb. 36: Reaktionsschema der Atmungskette |
4.2.4 Die Endoxidation. Atmungskette
AbschlieŖend wird der als [H] vorliegende Wasserstoff mit Atmungssauerstoff zu Wasser oxidiert. Dabei wird der grŲŖte Teil des Energiegehaltes unserer Lebensmittel ausgeschŲpft. (Der evolutionšre Grund wird gewesen sein, dass hier ein Mittel gefunden wurde, den zellschšdigenden Sauerstoff abzubauen.) Das hierfŁr zustšndige Zellorgan ist das Mitochondrium mit der Atmungskette, deren Reaktionsschema die Abb. 36 zeigt.
Zur Oxidation von Wasserstoff sind drei Wege denkbar und realisiert:
1. Knallgasreaktion
Der Vergleich mit der Verbrennung von Wasserstoff, bei der nur
wertlose Licht- und Wšrmeenergie entstehen, liegt nahe. Die
Reaktion bei dieser Knallgasreaktion lšuft lawinenartig und deshalb
ungesteuert ab (-> Abb. 37a). Denken Sie an die Knallgasexplosionen
von Lakehurst, Cape Kennedy oder Tschernobyl:
2. Atmungskette
Dagegen erfolgt die Oxidation von NADH mit Hilfe einer komplizierten
enzymatischen Reaktionssequenz, der Atmungskette (-> 37b):
(Der Wert der freigesetzten Energie ist geringer, weil NADH bereits eine oxidierte Form von Wasserstoff ist.)
Die Ausbeute an nutzbarer Energie wird gesteigert, indem der Redoxprozess zwischen NADH/H+ und O2 in einer Serie von Reaktionsschritten zerlegt wird, wobei die Wege fŁr Wasserstoff und Elektronen getrennt verlaufen.
Von den maximal mŲglichen 218 kJoule werden etwa 130 kJoule als chemische Energie (Freie Energie) in Form von 3 Mol ATP abgefangen. Die restliche Energie wird als KŲrperwšrme freigesetzt. Das bedeutet einen Wirkungsgrad von Łber 60 %.
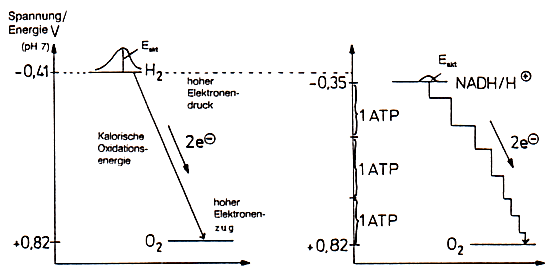
Abb. 37a, 37b: Energieschema der Knallgasreaktion und der Atmungskette im Vergleich
3. Brennstoffzelle
Ein technisch verwirklichter Kompromiss zwischen beiden Reaktionsablšufen
ist die Knallgaszelle, bei der die Oxidation von H2 und die
Reduktion von O2 getrennt an zwei katalytisch wirkenden
Edelmetalloberflšchen ablaufen (-> Abb. 38). Zwischen beiden
Elektroden baut sich die Spannung 1,23 V auf, bei Kurzschluss oder
Einschalten eines Verbrauchers flieŖt Strom. In diesen sog.
Brennstoffzellen kann man bei vorsichtiger FŁhrung Wirkungsgrade
von fast 100 % erreichen. (Als Reduktionsmittel verwendet man
anstelle von Wasserstoff auch Glucose, Milchsšure oder sogar
Kohlenwasserstoffe.)
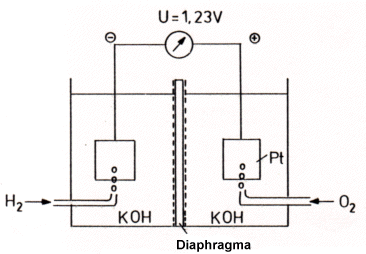
Abb. 38: Knallgaszelle
Die Reaktionen der Atmungskette
Zunšchst wird NADH durch FMN oxidiert, FMNH2 durch Ubichinon (-> Abb. 36). Ab dieser Stelle verlaufen Elektronentransport und Protonentransport getrennt:
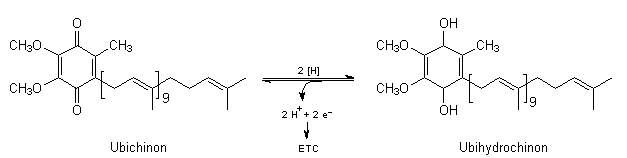
Abb. 39: Feinmechanismus der Redoxreaktionen von Ubichinon
Beide (sowohl H+ als auch e¯) werden letztlich auf Sauerstoff Łbertragen. Das Transportsystem fŁr die Elektronen besteht aus einer ganzen Reihe (ETC) von eisenhaltigen Proteinen, den Cytochromen, deren Eisen-Ionen beim Elektronentransport nur einem Ladungswechsel unterliegen:
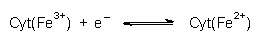
Dabei erfolgt eine Abschwšchung des stark negativen Potentials der Elektronen durch stufenweise Anhebung Łber Fe3+/Fe2+-Redoxgleichgewichte mit dem Ziel, die dabei freiwerdende potentielle Energie als ATP abzufangen.
An letzter Stelle steht die Cytochromoxidase mit dem Cyt a/a3, einem Fe- und Cu- haltigen Enzym. Hier erfolgt die Reduktion des finalen Elektronenakzeptors, des Sauerstoffs:
Das negative Sauerstoff-Ion reagiert mit den Protonen zu Wasser, einem der Endprodukte des Glucoseabbaus:
Endbilanz der Glucoseoxidation
Pro Mol Glucose wurden je 6 Mol Wasser und CO2 sowie 38 Mol ATP gewonnen:
4.2.5 Zusammenhšnge des Citronensšurezyklus mit
anderen Stoffwechselwegen
Mit dem Citronensšurezyklus sind andere Stoffwechselwege verwoben. Dies gilt besonders fŁr Aminosšuresynthese, -umbau und -abbau sowie fŁr den Stoffwechsel der Nucleinsšurebasen als auch fŁr den Harnstoffzyklus. Als Ausscheidungsprodukte entstehen vor allem Ammonium-Ionen und Harnstoff. Letzterer entsteht im Harnstoffzyklus, der Łber Asparaginsšure/Oxalessigsšure mit dem Citronensšurezyklus verbunden ist, nach folgender formaler Reaktion:
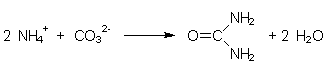
4.2.6 Regelung einiger Reaktionen
Die Reaktionen des Abbaus von Glucose und die Endoxidation
werden vor allem energetisch und stofflich gesteuert. Beispiele sind
unter vielen anderen:
Die Atmungskette wird aktiviert durch:
4.2.7 Einige Beispiele fŁr Vergiftungsmechanismen
| - | Nitrophenol als SchilddrŁsenhormon-Analoges entkoppelt die Atmungskette; es wird nur Wšrme produziert. |
| - | Arsenat konkurriert in der Atmungskette mit
Phosphat um den ATP-Syntheseplatz, ohne aber eine Bindung
einzugehen; Wšrmefreisetzung ist die Folge.
Arsenat hemmt auch die oxidative Decarboxylierung von a-Ketoglutarsšure. |
| - | CO, H2S, CN¯ komplexieren irreversibel das Eisen-Ion in der Cytochromoxidase, so dass ein Wertigkeitswechsel nicht mehr mŲglich ist. |
| - | Fluorid-Ionen hemmen den Citronensšurezyklus. Dies betrifft auch Bakterien (Kariesprophylaxe). |