Alkane, die „störrischen Ketten"
Alkane sind gesättigte Kohlenwasserstoffe und deshalb wenig geneigt, Reaktionen einzugehen.
Das besagt auch eine andere Bezeichnung für sie: "Paraffine" (lat. parum affinis; wenig geneigt).
Neben der Verbrennung mit Sauerstoff gehen sie nur noch mit den Halogenen
Fluor, Chlor und Brom Verbindungen ein. Doch selbst für diese Reaktionen ist die vorherige,
energieaufwendige Bildung von Halogen-Radikalen Voraussetzung. Genaueres hierzu findet man auf der
Seite Fotohalogenierung der Alkane.
Die Moleküle der Alkane sind sehr einfach aufgebaut. Alle C-Atome sind durch kovalente Einfachbindungen
miteinander verknüpft. Sie bilden entweder unverzweigte Ketten oder Ketten mit einer oder mehreren
Verzweigungen. Die weiteren Valenzen sind mit Wasserstoff abgesättigt. Die allgemeine Summenformel
der Alkane ist
CnH2n+2
Cycloalkane enthalten je Ring zwei Wasserstoffatome weniger.
CnH2n
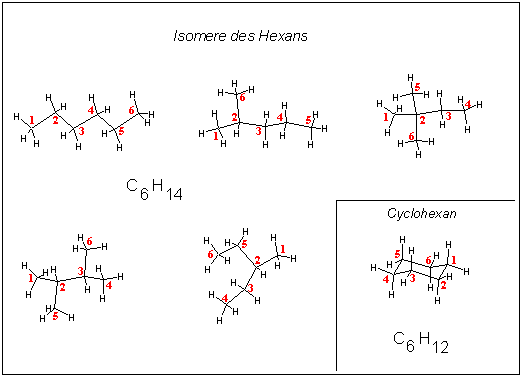
Am Beispiel verschiedener Hexane, die sechs C-Atome im Molekül besitzen, kann man die Gültigkeit dieser allgemeinen Summenformel leicht überprüfen.

Ab dem Butan (C4H10) können die Molekülstrukturen der Alkane auch verzweigte Ketten sein. Bei diesen Verbindungen, welche die gleiche Bruttoformel, aber unterschiedliche Konstitution (lat. constitutio = Beschaffenheit) besitzen, spricht man von Isomeren. Da sich die einzelnen Isomere chemisch und physikalisch unterscheiden, besitzt jedes Isomer eine eigene, genaue Bezeichnung. Die Namen für oben stehende Hexanisomere kann man auf der Isomerie-Webseite finden.
Die unverzweigt-kettigen Kohlenwasserstoffe nennt man n-Alkane (n steht für normal). Die verzweigten Ketten sind Isoalkane oder i-Alkane (i für isomer).
Die physikalischen Eigenschaften (Schmelzpunkt, Siedepunkt, Löslichkeit) der n-Alkane verändern sich kontinuierlich mit zunehmender Anzahl der CH2-Gruppen ("Methylen-Gruppen"). Man spricht von einer homologen Reihe. Weiteres zu der homologen Reihe der n-Alkane findet man hier.
Weitere Texte zum Thema „Kohlenwasserstoffe“