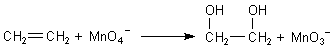
Die Baeyer-Probe - ein Nachweis für Alkene
Experimente:
Versuch: Baeyer-Probe auf Doppelbindungen
Gibt man zu einer wässrigen oder sodaalkalischen Kaliumpermanganatlösung (KMnO4)
die Probe eines ungesättigten Kohlenwasserstoffs und durchmischt gut, färbt sich die rosa-violette
Kaliumpermanganatlösung relativ schnell braun (-> Versuch).
Auch diese Reaktion ist wie die Bromaddition eine elektrophile
(elektronensuchende) Addition an die π-Elektronen der Doppelbindung. Sie ist unter dem Namen
Baeyer-Probe bekannt. Mit ihr kann man Alkene nachweisen, ohne giftiges Brom benutzen
zu müssen. Hierbei ist das Produkt ein Diol, also ein zweiwertiger Alkohol. Aus Ethen entsteht
so Glykol.
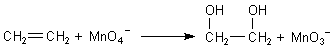
Das Permanganat ist ein sehr starkes Oxidationsmittel, das bei dieser Reaktion zwei Sauerstoffatome an den Kohlenwasserstoff überträgt. Das Permanganat wird dabei reduziert.
Die Addition verläuft hier ganz anders als bei der Reaktion mit Brom oder Wasser.
Der eigentliche Übergangszustand ist ein Molekül, in dem das Permanganat über zwei seiner
Sauerstoffatome gebunden vorliegt. Dieser Komplex wird durch Wassermoleküle aus der Lösung aufgespalten,
wodurch ein Diol-Molekül entsteht.
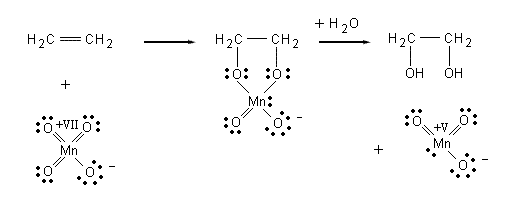
Aus den instabilen MnO3--Ionen bildet sich Braunstein (MnO2). Dabei entsteht auch Manganat-(VI). Dieses ist ein schönes Beispiel für eine Disproportionierungsreaktion. Bei entsprechender Reaktionsführung kann man hierbei sogar die verschiedenen Farben der Mangan-Spezies beobachten: Manganat(V) ist blau, Manganat(VI) grün und Braunstein (wie der Name sagt) braun.
Durch die kovalenten Bindungen im Übergangszustand ist diese Reaktion stereospezifisch. Die gebildeten OH-Gruppen stehen immer an derselben Seite der C-C-Bindung (cis-ständig). Diese Reaktion ist somit im Gegensatz zur trans-Addition mit Brom eine cis-Addition.
Weitere Texte zum Thema „Kohlenwasserstoffe“